
| A. | 46g NO2和N2O4混合氣體中含有原子數為3NA | |
| B. | 標準狀況下22.4 L HF中含原子數為2NA | |
| C. | 1L 1mol/L醋酸溶液中離子總數為2NA | |
| D. | 7.1g氯氣與足量NaOH溶液反應轉移的電子數為0.2NA |
分析 A、NO2和N2O4的最簡式均為NO2;
B、標況下HF為液體;
C、醋酸為弱電解質,不能完全電離;
D、求出氯氣的物質的量,然后根據氯氣和堿的反應為歧化反應來分析.
解答 解:A、NO2和N2O4的最簡式均為NO2,故46g混合物中含有的NO2的物質的量為1mol,故含3NA個原子,故A正確;
B、標況下HF為液體,故不能根據氣體摩爾體積來計算其物質的量,故B錯誤;
C、醋酸為弱電解質,不能完全電離,故溶液中的離子個數小于2NA個,故C錯誤;
D、7.1g氯氣的物質的量為0.1mol,而氯氣和堿的反應為歧化反應,故0.1mol氯氣反應轉移0.1NA個電子,故D錯誤.
故選A.
點評 本題考查了阿伏伽德羅常數的有關計算,難度不大,應注意掌握公式的運用和物質的結構.


 應用題作業本系列答案
應用題作業本系列答案科目:高中化學 來源: 題型:選擇題
| A. | Fe2+、Na+、SO42-、NO3- | B. | Na+、K+、Al3+、NO3- | ||
| C. | K+、Mg2+、Cl-、SO42- | D. | NH4+、Cl-、K+、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 蒸發:應使混合物中的水分完全蒸干后,才能停止加熱 | |
| B. | 蒸餾:開始蒸餾時應先加熱再開冷凝水;蒸餾完畢,應先關冷凝水再撤酒精燈 | |
| C. | 分液:下層液體從分液漏斗下口放出后,再將上層液體從下口放出到另一燒杯 | |
| D. | 量取:用規格為10mL的量筒量取8.0mL液體 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
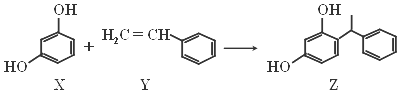
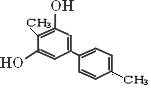
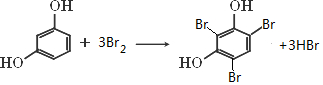
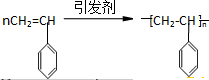
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氯氣是一種有毒的氣體 | |
| B. | 氯氣、氯水、液氯是同一種物質 | |
| C. | 氯氣能與水發生反應 | |
| D. | 氯氣是一種黃綠色,有刺激性氣味的氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
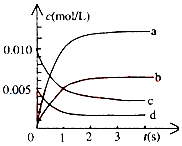 在2L密閉容器中,800℃時反應2NO(g)+O2(g)?2NO2(g)體系中,n(NO)隨時間的變化如表:
在2L密閉容器中,800℃時反應2NO(g)+O2(g)?2NO2(g)體系中,n(NO)隨時間的變化如表:| 時間(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 高中化學教材介紹了鈉、鎂、鋁、鐵、氯、硫、氮、硅等元素及其化合物的知識,(1)以上元素中在自然界有游離態存在的是N、S、Fe元素(填元素符號).
高中化學教材介紹了鈉、鎂、鋁、鐵、氯、硫、氮、硅等元素及其化合物的知識,(1)以上元素中在自然界有游離態存在的是N、S、Fe元素(填元素符號).查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 溫度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常數 | 1.7 | 1.1 | K | 0.6 | 0.4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | pH=4 時,醋酸的電離常數Ka≈1.8×10-5 | |
| B. | B點時,c(CH3COOˉ)=c(CH3COOH) | |
| C. | B點時,在溶液中滴入酚酞試劑,溶液顯紅色 | |
| D. | C點時,c(CH3COOˉ)>c(Na+)>c(H+)>c(OHˉ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com