
【題目】有四種微粒的結構示意如下,下列說法錯誤的是( )
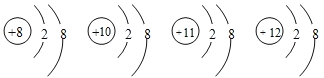
A.它們屬于不同種元素
B.它們的核外電子排布相同
C.它們都是離子
D.它們都具有稀有氣體原子的穩定結構
科目:高中化學 來源: 題型:
【題目】按如圖裝置進行實驗(a、b電極均為Cu電極),實驗開始觀察到靈敏電流計的指針發生偏轉。 下列有關說法正確的是

A. b極電極反應為Cu - 2e-=Cu2+B. 溶液中Cu2+穿過交換膜發生遷移
C. 電流計指針偏轉幅度將保持不變D. 外電路轉移的電子最多為0.02 mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)在①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金剛石,⑦(NH4)2SO4,⑧乙醇中,由極性鍵形成的非極性分子有_______(填序號,以下同),含有金屬離子的物質是__,分子間可形成氫鍵的物質是________,屬于離子晶體的是__,屬于原子晶體的是__,①~⑤五種物質的熔點由高到低的順序是__。
(2)A,B,C,D為四種晶體,性質如下:
A.固態時能導電,能溶于鹽酸
B.能溶于CS2,不溶于水
C.固態時不導電,液態時能導電,可溶于水
D.固態、液態時均不導電,熔點為3500 ℃
試推斷它們的晶體類型:A.__;B.__;C.__;D.__。
(3)下圖中A~D是中學化學教科書上常見的幾種晶體結構模型,請填寫相應物質的名稱:A.__;B.__;C.__D.____。
.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Fe2O3 在高爐高溫下可以發生下列反應:Fe2O3+CO=2FeO+CO2,形成的固體混和物(Fe2O3、FeO)中,元素鐵和氧質量比用 mFe︰mO 表示 21︰a。
(1)若 mFe︰mO=21︰8,計算 Fe2O3 被 CO 還原的百分率_____________;
(2) Fe2O3 和 CO 的反應分兩步進行:Fe2O3→Fe3O4→FeO,當 6<a<8,若 mgFe2O3 參與反應,計算消耗 m(CO)的質量_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】
(一) 現代鋁的精煉研究方向是減低能耗。如圖 :室溫下通過電解在陰極沉積純鋁,A1Br3 在苯(簡寫 ArH)中可以生成[A12Br5ArH]+和 Br-。

(1)陽極的材料________;
(2)寫出陰極沉積鋁的電極方程式__________________________________________;
(二)鄰硝基苯甲酸是重要的醫院中間體,最新合成方法是鄰硝基甲苯和高錳酸鉀在相轉移催化劑季銨鹽(Q+X-)氧化、酸化合成,其原理如下:

相轉移催化原理如下:

有關物質的物理性質如下表:
物質 | 鄰硝基苯甲酸 | 高錳酸鉀 | 芐基三乙基氯化銨(C6H5-CH2CH2)N(C2H5)3Cl | 聚乙二醇 | 四丁基溴化銨(C4H9)4NBr | NH4Cl |
水 | 難溶 | 易溶 | 可溶 | 任意比互溶溶 | 可溶 | 易溶 |
有機物 | 易溶 | 難溶 | 易溶 | 易溶 | 易溶 | 難溶 |
下列說法不合理的是________;
A.相轉移催化劑作用主要決定于 Q+的物理化學性質
B.反應中為了防止溫度劇烈升高,投料應該分批加入
C.Q+X-是通過增大反應接觸面積提高反應速率
D.增大壓強可以提高鄰硝基甲苯氧化的反應限度
E.工業使用季銨鹽(Q+X-)可以提高鄰硝基苯甲酸產率
(2)四丁基溴化銨(C4H9)4NBr 萃取水中的高錳酸鉀的方程式為:KMnO4(aq) +Q+X-(aq) →Q+ MnO4- (aq) +KX(aq),寫出平衡常數 k 的表達式________________;設n(Q+X-):n(鄰硝基甲苯)=x,理論證明當 x=5%鄰硝基甲酸產率 y 得到最大值,請畫出 y 隨 x 變化的示意圖________________ 。
(3)實驗表明,當溫度 100℃、反應時間 2.5h,n(KMnO4): n(鄰硝基甲苯)=3:1,催化劑用量相同,Q+X-反應的催化效果如下:
相轉移催化劑 | 芐基三乙基氯化銨 (C6H5-CH2CH2) N(C2H5)3Cl | 聚乙二醇 | 四丁基溴化銨 (C4H9)4NBr |
產率% | 46.7 | 20.0 | 53.1 |
芐基三乙基氯化銨比四丁基溴化銨催化效果差的原因_____________________________;工業生產不用聚乙二醇做催化劑的主要原因____________________________________ ;
(4)(C4H9)4NBr 為催化劑,鄰硝基甲苯和高錳酸鉀反應,測得溶液酸堿性對產率、反應時間影響如圖 ,下列推測合理的是________。

A.溶液堿性強產率降低是因為季銨鹽發生水解反應
B.pH=2 高錳酸鉀一定發生副反應
C.選擇 pH=7、適當升溫可以提高產率
D.工業可以選擇濃硝酸替代高錳酸鉀做氧化劑,減緩對設備的腐蝕
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子在指定條件下一定能大量共存的一組是:( )
A. c(H+)/c(OH—)=105的溶液中:Na+、ClO-、K+、Cl-
B. 由水電離出的C(H+)=1×10-13mol/L的溶液中:NH4+、Fe2+、Cl-、SO42-
C. 使酚酞變紅色的溶液中:NO3-、Cl-、Ca2+、Na+
D. 使甲基橙變紅色的溶液中:NO3-、Al3+、NH4+、SO42-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】含氯的物質與人們的生活密切相關。已知氯元素常見的化合價有-1、0、+1、+3、+5、+7六種,其不同價態的物質間可相互轉化。回答下列問題:
(1)氯原子的原子結構示意圖___;氯離子的電子式___。
(2)氯氣能使濕潤的有色布條褪色,起到漂白作用的物質是____(寫名稱),漂粉精的主要有效成分是___(寫化學式)。
(3)實驗室制取氯化氫的化學方程式____。
(4)工業上將含有氯氣的尾氣通過___進行處理,在處理時發生的反應中氯氣作為____。
a.氧化劑 b.還原劑 c.既是氧化劑又是還原劑 d.既不是氧化劑又不是還原劑
(5)寫出氯氣的兩種用途____、____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,pH=11的氨水和NaOH溶液分別加水稀釋100倍,溶液的pH隨溶液體積變化的曲線如下圖所示。據圖判斷錯誤的是( )

A. a的數值一定大于9
B. Ⅱ為氨水稀釋時溶液的pH變化曲線
C. 稀釋后氨水中水的電離程度比NaOH溶液中水的電離程度大
D. 完全中和相同體積的兩溶液時,消耗相同濃度的稀硫酸的體積:V(NaOH)<V(氨水)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有部分前四周期元素的性質或原子結構如下表:

(1)B單質分子中,含有________個![]() 鍵和__________個
鍵和__________個![]() 鍵,元素B的氣態氫化物的空間型為________________。
鍵,元素B的氣態氫化物的空間型為________________。
(2)C單質的熔點____________A單質的熔點(填“高于”或“低于”),其原因是:_______________
(3)寫出元素D基態原子的電子排布式:______________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com