
【題目】(1)已知某元素的原子結構示意圖: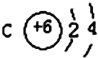 則可知:該元素原子的電子層數為:______,最外層電子數為:______,該元素在周期表的位置是第______周期第______族。
則可知:該元素原子的電子層數為:______,最外層電子數為:______,該元素在周期表的位置是第______周期第______族。
(2)已知某元素的原子結構示意圖: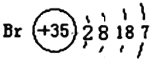 則可知:該元素原子的電子層數為:______,最外層電子數為:______,該元素在周期表的位置是第______周期第______族。
則可知:該元素原子的電子層數為:______,最外層電子數為:______,該元素在周期表的位置是第______周期第______族。
科目:高中化學 來源: 題型:
【題目】反應A+B→C(反應放熱)分兩步進行:①A+B→X(反應吸熱),②X→C(反應放熱)。下列示意圖中,能正確表示總反應過程中能量變化的( )
A. 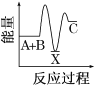 B.
B. 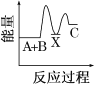
C. 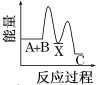 D.
D. 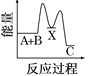
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按要求填空:
用化學用語回答下列問題:
(1)寫出二硫化碳分子的電子式:__________
(2)寫出氮氣分子的結構式:__________
(3)A+、B-、C、D 四種粒子(分子或離子),它們都分別含10個電子,已知它們有如下轉化關系:A++B-![]() C+D↑,則A+的電子式:_______;比較C和D的穩定性的強弱:_____(用化學式表示)
C+D↑,則A+的電子式:_______;比較C和D的穩定性的強弱:_____(用化學式表示)
(4)用電子式表示MgCl2的形成過程__________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向一定量的Fe、FeO、Fe2O3的混合物中加入100mL濃度為1.0mol·L-1的鹽酸,恰好使混合物完全溶解,有氣體放出,所得溶液中加入KSCN溶液后無紅色出現。若用足量的CO在高溫下還原相同質量此混合物,能得到鐵的質量是( )
A. 11.2g B. 5.6g
C. 2.8g D. 1.4g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有①熔融的BaCl2、②H2SO4溶于水、③NH4Cl溶于水、④Na2O2溶液、⑤干冰升華、⑥溴水被CCl4萃取六種物質,按下列要求回答:
(1)化學鍵沒有破壞的是__________,僅破壞共價鍵的是________,僅破壞離子鍵的是________,離子鍵和共價鍵都破壞的是_____________。
(2)NH4Cl的電子式是________,CO2的結構和CS2相似,請你寫出CS2的電子式_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Na2SO3是一種重要的還原劑,I2O5是一種重要的氧化劑,二者都是化學實驗室中的重要試劑。
(1)已知:2Na2SO3 (aq)+O2(aq)==2Na2SO4(aq) △H =m kJ·mol-1,O2(g)![]() O2(aq) △H =n kJ·mol-1 ,則Na2SO3溶液與O2(g)反應的熱化學方程式為______________________________。
O2(aq) △H =n kJ·mol-1 ,則Na2SO3溶液與O2(g)反應的熱化學方程式為______________________________。
(2)Na2SO3的氧化分富氧區和貧氧區兩個階段,貧氧區速率方程為v=k·ca(SO32-)·cb(O2),k為常數。
①當溶解氧濃度為4.0 mg/L(此時Na2SO3的氧化位于貧氧區)時,c(SO32-)與速率數值關系如下表所示,則a=____。
c(SO32-)×103 | 3.65 | 5.65 | 7.65 | 11.65 |
V×106 | 10.2 | 24.4 | 44.7 | 103.6 |
②兩個階段的速率方程和不同溫度的速率常數之比如下表所示。已知1n(k2/k1)=Ea/R(1/T2-1/T1),R 為常數,則Ea(富氧區)______(填“>”或“<”)Ea(貧氧區)。
反應階段 | 速率方程 | k(297.0K)/k(291.5K) |
富氧區 | v= k·c(SO32-)·c(O2) | 1.47 |
貧氧區 | v= k·ca(SO32-)·cb(O2) | 2.59 |
(3)等物質的量的Na2SO3和Na2SO4混合溶液中,c(SO32-) +c( HSO3-)______(填“>”“<”或“=”)c(SO42-)。
(4)利用I2O5可消除CO 污染,其反應為I2O5(s)+5CO(g) ![]() 5CO2(g)+I2(s),不同溫度下,向裝有足量I2O5固體的2 L 恒容密閉容器中通入2 mol CO,測得CO2氣體的體積分數φ(CO2) 隨時間t的變化曲線如圖所示。
5CO2(g)+I2(s),不同溫度下,向裝有足量I2O5固體的2 L 恒容密閉容器中通入2 mol CO,測得CO2氣體的體積分數φ(CO2) 隨時間t的變化曲線如圖所示。

①從反應開始至a點時的平均反應速率v(CO)=__________。
②b點時,CO 的轉化率為_____________。
③b點 和 d點 的 化學 平衡常數:Kb____(填“ >”“<”或“=” )Kd,判斷的理由是_____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將鋅片和銀片浸入稀硫酸中組成原電池,兩電極間連接一個電流計。
(1)鋅片上發生的電極反應:___________________;
(2)銀片上發生的電極反應:____________________;
(3)總反應的離子方程式:_________________;
(4)在______片上有氣泡產生,電子從______片上流向_______片上。
(5)若該電池中兩電極的總質量為60 g,工作一段時間后,取出鋅片和銀片洗凈干燥后稱重,總質量為47 g,試計算產生氫氣的體積(標準狀況)為___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】
鐵氮化合物(FexNy)在磁記錄材料領域有著廣泛的應用前景。某FexNy的制備需鐵、氮氣、丙酮和乙醇參與。
(1)Fe3+基態核外電子排布式為____________________。
(2)丙酮(![]() )分子中碳原子軌道的雜化類型是_______________,1 mol 丙酮分子中含有σ鍵的數目為______________。
)分子中碳原子軌道的雜化類型是_______________,1 mol 丙酮分子中含有σ鍵的數目為______________。
(3)C、H、O 三種元素的電負性由小到大的順序為________________。
(4)乙醇的沸點高于丙酮,這是因為____________________。
(5)某FexNy的晶胞如題21圖-1所示,Cu可以完全替代該晶體中a位置Fe或者b位置Fe,形成Cu替代型產物Fe(x-n) CunNy。FexNy轉化為兩種Cu替代型產物的能量變化如題21圖-2 所示,其中更穩定的Cu替代型產物的化學式為___________。

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com