(2011?金臺區模擬)I、圖1各物質是中學化學中常見的物質,甲、乙均是離子化合物,且陰、陽離子個數比為1:1.甲是發酵粉的主要成分,乙是一種常用的化肥.B、D常溫常壓下是氣體.請回答下列問題:
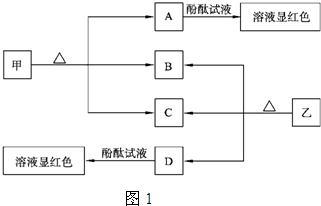
(1)甲的俗名是
小蘇打
小蘇打
.
(2)A、D物質的水溶液分別滴入酚酞試液后,溶液均顯紅色,說明溶液均顯
堿性
堿性
性,其原理是否相同?請用必要的文字加以解釋并寫出離子方程式:
不同,A溶液顯堿性是因為碳酸根離子發生水解,CO32-+H2O?HCO3-+OH-,D溶液顯堿性是因為:NH3?H2O?NH4++OH-
不同,A溶液顯堿性是因為碳酸根離子發生水解,CO32-+H2O?HCO3-+OH-,D溶液顯堿性是因為:NH3?H2O?NH4++OH-
.
(3)向飽和氯化鈉溶液中通入氣體D至飽和后,再通入足量的氣體B可制得物質甲,寫出該反應的化學方程式:
NaCl+NH3+CO2+H2O=NaCO3+NH4Cl
NaCl+NH3+CO2+H2O=NaCO3+NH4Cl
.
II、甲醇是一種可再生能源,具有開發和應用的廣闊前景,工業上一般可采用如下反應來合成甲醇:
CO(g)+2H
2(g)→CH
3OH(g).
(1)分析該反應并回答下列問題:
①平衡常數表達式為K=
.
②下列各項中,不能夠說明該反應已達到平衡的是
d
d
(填序號).
a.恒溫、恒容條件下,容器內的壓強不發生變化
b.一定條件下,CH
3OH分解的速率和CH
3OH生成的速率相等
c.一定條件下,CO、H
2和CH
3OH的濃度保持不變
d.一定條件下,單位時間內消耗2mol CO,同時生成1mol CH
3OH
(2)圖2是該反應在不同溫度下CO的轉化率隨時間變化的曲線.
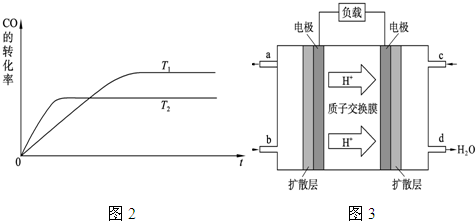
①該反應的焓變△H
<
<
0(填“>”、“<”或“=”).
②T
1和T
2溫度下的平衡常數大小關系是K
1>
>
K
2(填“>”、“<”或“=”).
③若容器容積不變,下列措施可增加甲醇產率的是
b
b
.
a.升高溫度
b.將CH
3OH(g)從體系中分離
c.使用合適的催化劑d.充入He,使體系總壓強增大
(3)已知在常溫常壓下:
①2CH
3OH(l)+3O
2(g)=2CO
2(g)+4H
2O(g)△H=-a kJ?mol
-1②2CO(g)+O
2(g)=2CO
2(g)△H=-b kJ?mol
-1③H
2O(g)=H
2O(l)△H=-c kJ?mol
-1
則CH
3OH(l)+O
2(g)=CO(g)+2H
2O(l)△H=
kJ?mol
-1.
(4)2009年10月,中國科學院長春應用化學研究所在甲醇燃料電池技術方面獲得新突破,組裝出了自呼吸電池及主動式電堆.甲醇燃料電池的工作原理如圖3所示.
①該電池工作時,b口通入的物質為
CH3OH
CH3OH
,c口通入的物質為
O2
O2
.
②該電池正極的電極反應式為:
O2+4e-+4H+=2H2O
O2+4e-+4H+=2H2O
.

 2NH3,下列選項不能作為反應達到平衡狀態標志的是( )
2NH3,下列選項不能作為反應達到平衡狀態標志的是( )

 名師伴你成長課時同步學練測系列答案
名師伴你成長課時同步學練測系列答案



 2NH3,下列選項不能作為反應達到平衡狀態標志的是( )
2NH3,下列選項不能作為反應達到平衡狀態標志的是( )