
【題目】煙氣中主要污染物SO2、NOx,為消除排放,保護環境,實現綠色可持續發展。
處理方法一:煙氣經O3預處理后用CaSO3水懸浮液吸收,可減少煙氣中SO2、NOx的含量。O3氧化煙氣中SO2、NO的主要反應的熱化學方程式為:
NO(g)+O3(g)=NO2(g)+O2(g) △H1
NO(g)+1/2O2(g)=NO2(g) △H2
SO2(g)+O3(g)![]() SO3(g)+O2(g) △H3
SO3(g)+O2(g) △H3
(1)反應3NO(g)+O3(g)=3NO2(g)的△H=_________。
(2) 室溫下,進入反應器的NO、SO2的物質的量恒定,改 變通入O3的物質的量,反應一段時間后體系中n(NO)、n(NO2)和n(SO2)隨反應前n(O3):nNO)的變化見圖。說明預處理過程中NO2的物質的量變化的原因_______,在反應中SO2的物質的量幾乎不發生變化的原因是_______________。

(3)在一定條件下,SO2(g)+O3(g)![]() SO3(g)+O2(g) △H3<0,在一定溫度下,向2L某恒容密閉容器中充入4molSO2(g)和1molO3(g),5min時,測得容器中SO3(g)的物質的量為0.5mol。
SO3(g)+O2(g) △H3<0,在一定溫度下,向2L某恒容密閉容器中充入4molSO2(g)和1molO3(g),5min時,測得容器中SO3(g)的物質的量為0.5mol。
①0-5min內,用SO2表示的平均反應速率v(SO2)________。
②下列說法中能判斷該反應達到平衡狀態的是________
a.單位時間內生成nmolSO2同時生成nmolSO3
b.SO3和O2的物質的量濃度之比1:1
C.容器內壓強保持不變
d.混合氣體的密度不變
e.混合氣體的平均相對分子質量不變
處理方法二: 也可采用NaClO2溶液作為吸收劑對煙氣進行處理。在不同溫度下,NaClO2溶液脫硫(S)、脫硝(N)的反應中,SO2和NO的平衡分壓Pe如圖所示。

(4) 由圖分析可知,反應溫度升高,脫硫、脫硝反應的平衡常數均_______(填“增大”、“不變”或“減小”)。
(5) 反應ClO2-+2SO32-![]() 2SO42-+Cl-的平衡常數K表達式為_______。
2SO42-+Cl-的平衡常數K表達式為_______。
【答案】△H1+2△H2 n(O3):n(NO)<1,臭氧氧化NO為NO2,NO減少,NO2增多;n(O3):n(NO)>1,臭氧過量把NO2轉化成更高價態 SO2與O3的反應速率慢 0.05mol(L·min)-1 a 減小 ![]()
【解析】
SO2(g)+O3(g)![]() SO3(g)+O2(g) △H3
SO3(g)+O2(g) △H3
(1)①NO(g)+O3(g)=NO2(g)+O2(g) △H1;②NO(g)+1/2O2(g)=NO2(g) △H2;由蓋斯定律,①+2×②可得:3NO(g)+O3(g)═3NO2(g),則△H=△H1+2△H2;
(2)①n(O3):n(NO)<1,臭氧氧化NO為NO2,NO減少,NO2增多;n(O3):n(NO)>1,臭氧過量把NO2轉化成更高價態;
②增加n(O3),O3氧化SO2的反應幾乎不受影響,說明濃度對反應速率影響較小,可能是SO2與O3的反應速率慢;
(3)在一定條件下,SO2(g)+O3(g)![]() SO3(g)+O2(g) △H3<0,在一定溫度下,向2L某恒容密閉容器中充入4molSO2(g)和1molO3(g),
SO3(g)+O2(g) △H3<0,在一定溫度下,向2L某恒容密閉容器中充入4molSO2(g)和1molO3(g),
①5min時,測得容器中SO3(g)的物質的量為0.5mol,則消耗SO2(g)的物質的量為0.5mol,0-5min內,用SO2表示的平均反應速率v(SO2)=![]() ;
;
②a. 單位時間內生成nmolSO2同時生成nmolSO3,表示的是正逆反應速率,且滿足二者的化學計量數關系,說明正逆反應速率相等,達到平衡狀態,故正確;b. 各物質分子數之比等于多少決定于開始加入的各物質的多少,與化學反應是否處于平衡狀態無關,不能說明反應達到平衡狀態,故錯誤;c.混合氣體物質的量不變,恒溫恒容下,容器內壓強為定值,不能說明反應達到平衡狀態,故錯誤;d. 容器容積不變,氣體的體積不變,反應兩邊都是氣體,氣體的總質量不變,根據ρ=![]() ,所以氣體的密度始終不變,因此密度不能作為判斷平衡狀態的依據,故錯誤;e.反應為氣體體積不變的反應,在反應的任何階段,總質量沒變,總的氣體分子數沒變,所以平均相對分子質量不會變,不能說明反應達到平衡狀態,故錯誤;答案選a;
,所以氣體的密度始終不變,因此密度不能作為判斷平衡狀態的依據,故錯誤;e.反應為氣體體積不變的反應,在反應的任何階段,總質量沒變,總的氣體分子數沒變,所以平均相對分子質量不會變,不能說明反應達到平衡狀態,故錯誤;答案選a;
(4)在不同溫度下,NaClO2溶液脫硫、脫硝的反應中,SO2和NO的平衡分壓pe如圖所示。 由圖分析可知,反應溫度升高,O2和NO的平衡分壓負對數減小,這說明反應向逆反應方向進行,因此脫硫、脫硝反應的平衡常數均減小;
(5)根據反應離子方程式ClO2-+2SO32-![]() 2SO42-+Cl-可知平衡常數K表達式為K=
2SO42-+Cl-可知平衡常數K表達式為K=![]() 。
。


科目:高中化學 來源: 題型:
【題目】有 A、B、C、D、E 五種短周期主族元素,原子序數由 A 到 E 逐漸增大.①A 元素最外層電子數是次外層電子數的 2 倍. ②B 的陰離子和 C 的陽離子與氖原子的電子層結構相同.③在通常狀況下,B 的單質是氣體,0.1molB 的氣體與足量的氫氣完全反應共有 0.4mol 電子轉移.④C 的單質在點燃時與 B 的單質充分反應,生成淡黃色的固體, 此淡黃色固體能與 AB2 反應可生成 B 的單質.⑤D 的氣態氫化物與其最高價含氧酸間能發生氧化還原反應.請寫出:
(1)A 元素的最高價氧化物的電子式_________________,A 元素簡單氣態氫化物可構成堿性燃料電池,該電池的的負極電極方程式為:_____________________
(2)B 元素在周期表中的位置 _____________________
(3)B 單質與 C 單質在點燃時反應的生成物中所含化學鍵類型有 _________________
(4)D 元素的低價氧化物與 E 的單質的水溶液反應的化學方程式為 :____________________
(5)C 與 D 能形成 2:1 的化合物,用電子式表示該化合物的形成過程:_________________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列溶液的物質的量濃度的計算正確的是![]()
![]()
A. VL![]() 溶液中含
溶液中含![]() g,溶液中
g,溶液中![]() 是
是![]()
![]()
B. 將100mL![]()
![]() 的NaCl溶液與200mL
的NaCl溶液與200mL![]()
![]() 的NaCl溶液混合
的NaCl溶液混合![]() 忽略溶液體積變化
忽略溶液體積變化![]() ,得到溶液的物質的量濃度為2
,得到溶液的物質的量濃度為2![]()
C. 實驗室配制480mL![]()
![]() 的硫酸銅溶液,應選取500mL容量瓶,稱取
的硫酸銅溶液,應選取500mL容量瓶,稱取![]() g膽礬配成500mL溶液
g膽礬配成500mL溶液
D. 標準狀況下,aL![]() 溶于1000g水中,得到的溶液密度為b
溶于1000g水中,得到的溶液密度為b![]() ,則該溶液的物質的量濃度為
,則該溶液的物質的量濃度為![]()
![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ、實驗室常用MnO2與濃鹽酸反應制備Cl2(MnO2+4HCl(濃)→MnCl2+Cl2↑+2H2O反應裝置如圖所示)。
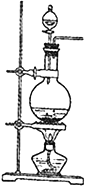
(1)裝置圖中的主要玻璃儀器有酒精燈、________、__________等。產生的氯氣通入水中制得氯水備用。氯水含有的離子除H+、Cl-外還有___________等離子,氯水中因含有__________而具有漂白性。
Ⅱ、某氯化鐵樣品含有少量FeCl2雜質。現要測定其中鐵元素的質量分數,實驗按以下步驟進行:
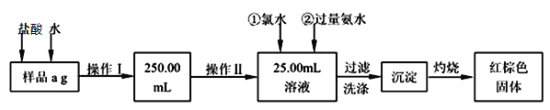
請根據上面流程,回答以下問題:
(2)樣品溶解時加鹽酸的作用是___________________________________。加入氯水所發生反應的離子方程式___________________________________。
(3)證明Fe3+離子已經沉淀完全的操作是___________________________________。將沉淀物加熱灼燒過程中,為使實驗結果準確,必須的操作為___________________。
(4)若原樣品質量a 為40.00g,加熱后紅棕色固體質量b為2.200g,則樣品中鐵元素的質量分數是_________;若稱量準確,最終測量的結果偏大,則造成誤差的原因可能是_____________(寫出一種原因即可)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將NO2、NH3和O2的混合氣體28L通過稀H2SO4后,溶液質量增加42g,氣體體積縮小為4.48L。將帶火星的木條插入其中,木條不復燃。則原混合氣體的平均相對分子質量為(氣體體積都是在標準狀況下測定)
A. 32.8B. 34.6C. 36.2D. 38.4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】松花皮蛋是夏季餐桌上的一道美食,其制作的原料有純堿、食鹽、生石灰、草木灰(內合碳酸鉀)、開水以及糠、稻殼等輔料,配料之間首先是生石灰與水反應生成熟石灰,試推斷另外最有可能發生的化學反應是( )
A.化合反應
B.分解反應
C.復分解反應
D.置換反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮的氧化物(NOx)是大氣污染物之一,工業上在一定溫度和催化劑條件下用NH3將NOx還原生成N2。某同學在實驗室中對NH3與NO2反應進行了探究。回答下列問題:
(1)氨氣的制備
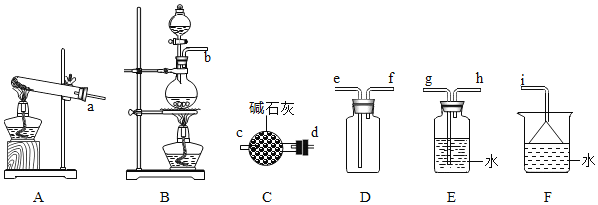
(2)氨氣的發生裝置可以選擇上圖中的________,反應的化學方程式為_______________。
(3)欲收集一瓶干燥的氨氣,選擇上圖中的裝置,其連接順序為:發生裝置→_________(按氣流方向,用各接口小寫字母表示)。
(4)氨氣與二氧化氮的反應
將上述收集到的NH3充入注射器X中,硬質玻璃管Y中加入少量催化劑,充入NO2(兩端用夾子K1、K2夾好)。
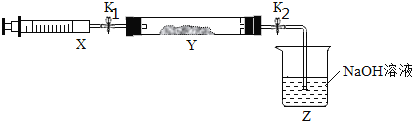
在一定溫度下按上圖所示裝置進行實驗。
操作步驟 | 實驗現象 | 解釋原因 |
打開K1,推動注射器活塞,使X中的氣體緩慢通入Y管中 | Y管中______ | 反應的化學方程式:___ |
將注射器活塞退回原處并固定,將裝置恢復到室溫 | Y管中有少量水珠 | 生成的氣態水冷凝 |
打開K2 | _________ | ________ |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下面有關過渡元素的說法正確的是
A.新型高效催化劑多與過渡元素有關B.高效低毒農藥多與過渡元素有關
C.過渡元素中只有鐵、錳等少數元素存在變價D.大多數過渡元素的單質不能與酸反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com