
| 9 |
| 18 |
| 22 |
| 44 |
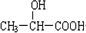 ,甲、丙、丁、己均能發生銀鏡反應.丙不易溶于水但丁易溶于水,丙為HCOOCH3,丁中含-OH,則丁為CH2OHCHO,然后結合有機物的結構和性質來解答.
,甲、丙、丁、己均能發生銀鏡反應.丙不易溶于水但丁易溶于水,丙為HCOOCH3,丁中含-OH,則丁為CH2OHCHO,然后結合有機物的結構和性質來解答.| 9 |
| 18 |
| 22 |
| 44 |
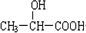 ,甲、丙、丁、己均能發生銀鏡反應.丙不易溶于水但丁易溶于水,丙為HCOOCH3,丁中含-OH,則丁為CH2OHCHO,
,甲、丙、丁、己均能發生銀鏡反應.丙不易溶于水但丁易溶于水,丙為HCOOCH3,丁中含-OH,則丁為CH2OHCHO,| △ |
| △ |


科目:高中化學 來源: 題型:
| A、稱取10.0gNaOH,加入500mL水 |
| B、稱取10.0gNaOH,選取500mL容量瓶進行配制 |
| C、稱取9.6gNaOH,選取480mL容量瓶進行配制 |
| D、稱取9.6gNaOH,選取500mL容量瓶進行配制 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、在原電池中,電子流出的一極是負極,發生氧化反應 |
| B、原電池是將化學能轉變為電能的裝置 |
| C、構成原電池的正極和負極必須是兩種不同的金屬 |
| D、原電池放電時,在外電路電子的流動方向是從負極到正極 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、酸 | B、氧化物 | C、有機物 | D、鈉鹽 |
查看答案和解析>>
科目:高中化學 來源: 題型:
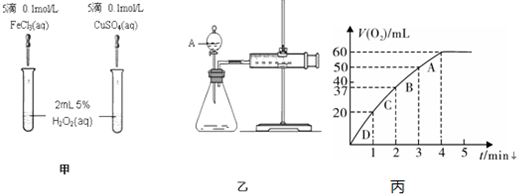
查看答案和解析>>
科目:高中化學 來源: 題型:
| 實驗序號 | 起始溫度t1/℃ | 終止溫度t2/℃ | |
| 鹽酸 | 氫氧化鈉 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
| T/K | 303 | 213 | 323 |
| 平衡時NH3的生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com