
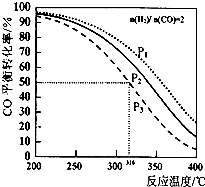
 以$\frac{n({H}_{2})}{n(CO)}$=2 通入IL的反應器中,一定條件T 發生反應:4H2(g)+2CO(g)?CH3OCH3(g)+H2O (g)△H,其中CO的平衡轉化率隨溫度、壓強變化關系如圖所示.下列說法正確的是( )
以$\frac{n({H}_{2})}{n(CO)}$=2 通入IL的反應器中,一定條件T 發生反應:4H2(g)+2CO(g)?CH3OCH3(g)+H2O (g)△H,其中CO的平衡轉化率隨溫度、壓強變化關系如圖所示.下列說法正確的是( )| A. | 該反應的△H>O | |
| B. | P1<P2<P3 | |
| C. | 若在P3和316℃時反應達到平衡,H2的轉化率等于50% | |
| D. | 若在P1和200℃時,反應達平衡后保持溫度和壓強不變,再充入2 mol H2和1molCO,則平衡時二甲醚的體積分數增大 |
分析 A.由圖可知,壓強一定時,溫度越高,平衡時CO的轉化率越低,說明升高溫度平衡向逆反應方向移動;
B.正反應為氣體體積減小的反應,溫度一定時,增大壓強平衡向正反應方向移動,CO的轉化率增大;
C.在P3和316℃時反應達到平衡,CO的轉化率為50%,結合開始時$\frac{n({H}_{2})}{n(CO)}$=2 計算;
D.若在P1和200℃時,反應達平衡后保持溫度和壓強不變,再充入2 mol H2和1molCO,與起始比值相同,為等效平衡.
解答 解:A.由圖可知,壓強一定時,溫度越高,平衡時CO的轉化率越低,說明升高溫度平衡向逆反應方向移動,故正反應為放熱反應,即△H<0,故A錯誤;
B.由圖可知轉化率P1>P2>P3,正反應為氣體體積減小的反應,溫度一定時,增大壓強平衡向正反應方向移動,CO的轉化率增大,故壓強P1>P2>P3,故B錯誤;
C.以n(H2):n(CO)=2通入1L的反應器中,令n(H2)=2mol、n(CO)=1mol,在P3和316℃時反應達到平衡,CO的平衡轉化率為50%,即轉化0.5mol,
4H2(g)+2CO(g)?CH3OCH3(g)+H2O
起始(mol) 2 1
轉化(mol) 1 0.5
則H2的轉化率$\frac{1}{2}$×100%=50%,
故C正確;
D.若在P1和200℃時,反應達平衡后保持溫度和壓強不變,再充入2 mol H2和1molCO,與起始比值相同,為等效平衡,則體積分數不變,故D錯誤.
故選C.
點評 本題考查化學平衡圖象、化學平衡影響因素及有關計算,為高頻考點,側重于學生的分析、計算能量的考查,難度中等,注意理解外界條件對平衡移動的影響,理解等效平衡的意義.


科目:高中化學 來源: 題型:選擇題
| A. | 氮氧化鋁中氮的化合價是-3 | |
| B. | 反應中氧化產物和還原產物的物質的量之比是1:2 | |
| C. | 反應中每生成5.7gAlON同時生成1.12LCO | |
| D. | AlON和CO的化學鍵類型不同 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
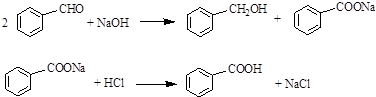
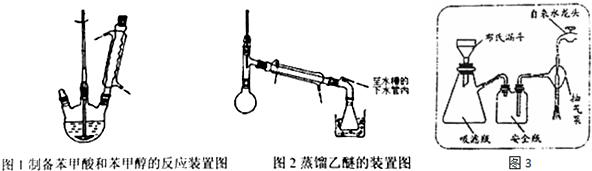
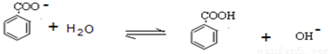 .
.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
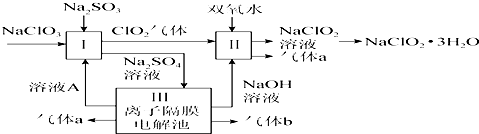
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
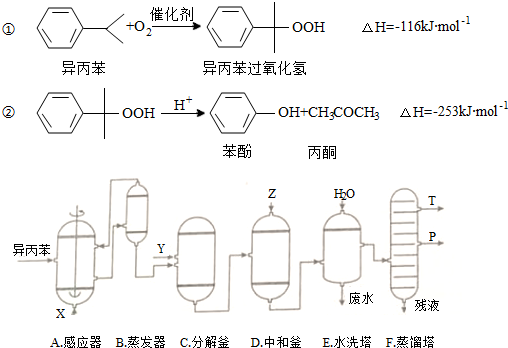
| 物質 | 相對分子質量 | 密度(g/cm-3) | 沸點/℃ |
| 異丙苯 | 120 | 0.8640 | 153 |
| 丙酮 | 58 | 0.7898 | 56.5 |
| 苯酚 | 94 | 1.0722 | 182 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
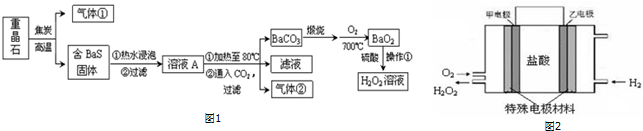
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 成 分 | NaCl | Mg(OH)2 | CaCO3 | BaSO4 | 其他不溶于酸的物質 |
| 質量分數/% | 15~20 | 15~20 | 5~10 | 30~40 | 10~15 |
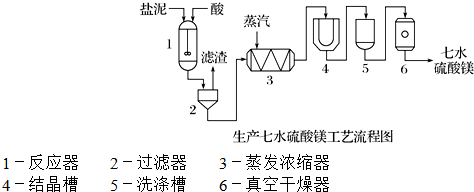
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 制備Fe(OH)3膠體:Fe3++3H2O═Fe(OH)3↓+3H+ | |
| B. | H2SO4溶液中投入鋅粒:2H++Zn═H2↑+Zn2+ | |
| C. | 用NaHCO3 治療胃酸過多:HCO3-+H+═CO2↑+H2O | |
| D. | 氯化鐵和氫氧化鉀溶液混合:Fe3++3OH-═Fe(OH)3↓ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com