
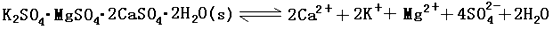
 已知298K時,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,求此溫度下該反應的平衡常數K(計算結果保留三位有效數字)。
已知298K時,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,求此溫度下該反應的平衡常數K(計算結果保留三位有效數字)。科目:高中化學 來源: 題型:
| SO | 2- 4 |
| CO | 2- 3 |
| SO | 2- 4 |
查看答案和解析>>
科目:高中化學 來源:2012-2013學年重慶市重慶一中高二上學期期中考試理科化學試卷(帶解析) 題型:填空題
(13分)難溶性雜鹵石(K2SO4·MgSO4·2CaSO4·2H2O)屬于“呆礦”,在水中存在如下平衡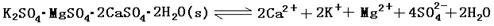
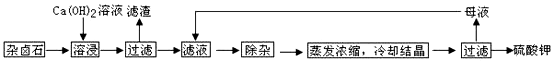
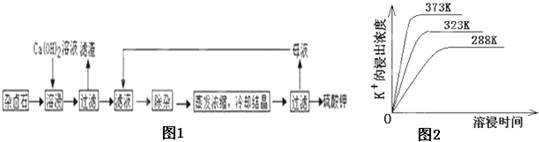
為能充分利用鉀資源,用飽和Ca(OH)2溶液溶浸雜鹵石制備硫酸鉀,工藝流程如下: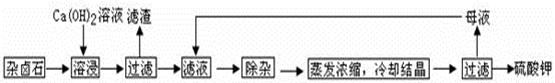
(1)濾渣主要成分有 和 以及未溶雜鹵石。
(2)用化學平衡移動原理解釋Ca(OH)2溶液能溶解雜鹵石浸出K+的原因: 。
(3)“除雜”環節中,先加入 溶液,經攪拌等操作后,過濾,再加入 溶液調濾液PH至中性。
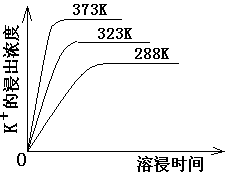
(4)不同溫度下,K+的浸出濃度與溶浸時間的關系是圖14,由圖可得,隨著溫度升高, 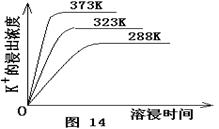
① 在相同時間K+的浸出濃度大。
② 在相同時間K+的浸出濃度減小
③ 反應的速率加快,平衡時溶浸時間短。
④ 反應速率減慢,平衡時溶浸時間增長。
(5)有人以可溶性碳酸鹽為溶浸劑,則溶浸過程中會發生:
已知298K時, Ksp(CaCO3)=2.80×10—9, Ksp(CaSO4)=4.90×10—5 ,求此溫度下該反應的平衡常數K 。
查看答案和解析>>
科目:高中化學 來源:2014屆重慶市高二上學期期中考試理科化學試卷(解析版) 題型:填空題
(13分)難溶性雜鹵石(K2SO4·MgSO4·2CaSO4·2H2O)屬于“呆礦”,在水中存在如下平衡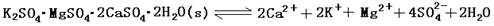
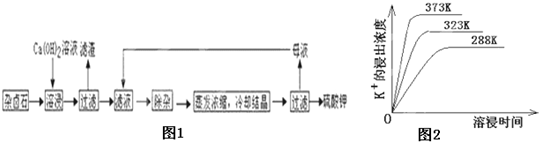
為能充分利用鉀資源,用飽和Ca(OH)2溶液溶浸雜鹵石制備硫酸鉀,工藝流程如下:
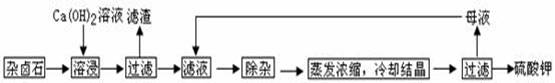
(1)濾渣主要成分有 和 以及未溶雜鹵石。
(2)用化學平衡移動原理解釋Ca(OH)2溶液能溶解雜鹵石浸出K+的原因: 。
(3)“除雜”環節中,先加入 溶液,經攪拌等操作后,過濾,再加入 溶液調濾液PH至中性。
(4)不同溫度下,K+的浸出濃度與溶浸時間的關系是圖14,由圖可得,隨著溫度升高,
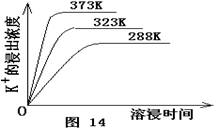
① 在相同時間K+的浸出濃度大。
② 在相同時間K+的浸出濃度減小
③ 反應的速率加快,平衡時溶浸時間短。
④ 反應速率減慢,平衡時溶浸時間增長。
(5)有人以可溶性碳酸鹽為溶浸劑,則溶浸過程中會發生:

已知298K時, Ksp(CaCO3)=2.80×10—9, Ksp(CaSO4)=4.90×10—5 ,求此溫度下該反應的平衡常數K 。
查看答案和解析>>
科目:高中化學 來源:廣東 題型:問答題
| SO | 2-4 |
| CO | 2-3 |
| SO | 2-4 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com