
 走進文言文系列答案
走進文言文系列答案科目:高中化學 來源: 題型:解答題
 鋁有多種化合物,在工業上用途廣泛.氮化鋁(AlN)中混有碳和氧化鋁,為確定某氮化鋁樣品的純度,進行如下實驗:(已知:AlN+H2O+NaOH→NaAlO2+NH3↑)
鋁有多種化合物,在工業上用途廣泛.氮化鋁(AlN)中混有碳和氧化鋁,為確定某氮化鋁樣品的純度,進行如下實驗:(已知:AlN+H2O+NaOH→NaAlO2+NH3↑)查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1.5 mol•L-1 | B. | 2.25 mol•L-1 | C. | 3 mol•L-1 | D. | 無法計算 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將Fe(NO3)2樣品溶于稀H2SO4后,滴加KSCN溶液,觀察溶液是否變紅,可以檢驗Fe(NO3)2晶體是否已氧化變質 | |
| B. | 濃氨水中滴加FeCl3飽和溶液可制得Fe(OH)3膠體 | |
| C. | 1 mol FeI2與足量氯氣反應時轉移的電子數為2NA | |
| D. | 水溶液中Fe2+、H+、SO${\;}_{3}^{2-}$、ClO-不能大量共存 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 序號 | 物質 | 雜質 | 除雜試劑或操作方法 |
| ① | NaCl | BaCl2 | 加入過量的K2CO3溶液,過濾,再加適量的鹽酸并加熱 |
| ② | FeSO4溶液 | CuSO4 | 加入過量Fe粉,過濾 |
| ③ | H2 | HCl | 通過盛NaHCO3溶液洗氣瓶,再通過盛H2SO4洗氣瓶 |
| ④ | 自來水 | 植物油 | 蒸餾 |
| A. | ①②③④ | B. | ②③④ | C. | ②④ | D. | ② |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 研究NO2、SO2、CO等大氣污染氣體的處理及利用的方法具有重要意義.
研究NO2、SO2、CO等大氣污染氣體的處理及利用的方法具有重要意義.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
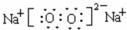 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com