
分析 鐵屑用稀鹽酸溶解得到氯化亞鐵溶液,調節溶液pH并加熱試劑X,將部分氧化為Fe2+氧化成Fe3+,可以是過氧化氫或氯水等,再加入NaOH溶液,加熱得到納米Fe3O4.
(1)鐵過量會和鐵離子發生氧化還原反應;
(2)①a.氫氣不溶于水、四氯化碳,但CCl4易揮發;
b.量氣管壓與水準管液面等高,即可測定氫氣體積;
c.讀數是保證裝置內壓強與外界大氣壓相等,氣體受熱溫度體積會增大,冷卻后體積會減小;
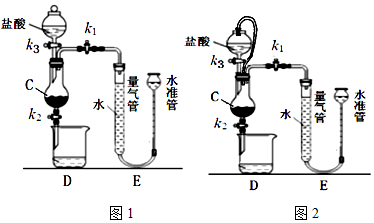
②圖2中分液漏斗連接橡膠管可以平衡壓強使液體順利流下;
(3)制備溶液A,試劑X是將部分氧化為Fe2+氧化成Fe3+,需要選擇具有強氧化性的物質;
(4)Fe2+、Fe3+在堿性、加熱條件下反應得到Fe3O4,還有水生成;制備中防止亞鐵離子被氧氣氧化;
(5)①鐵離子將碘離子氧化為碘單質,加入淀粉溶液呈藍色,滴定終點時藍色褪去;
②根據關系式:Fe3O4~2Fe3+~I2~2S2O32-計算.
解答 解:鐵屑用稀鹽酸溶解得到氯化亞鐵溶液,調節溶液pH并加熱試劑X,將部分氧化為Fe2+氧化成Fe3+,可以是過氧化氫或氯水等,再加入NaOH溶液,加熱得到納米Fe3O4.
(1)鐵過量會和鐵離子發生氧化還原反應,反應的離子方程式為:Fe+2Fe3+=3Fe2+,
故答案為:Fe+2Fe3+=3Fe2+;
(2)①a.氫氣不溶于水、四氯化碳,不影響沉淀氫氣體積,且CCl4易揮發,污染空氣,故a錯誤;
b.量氣管壓入水準管的水過多而溢出,但量氣管壓與水準管液面等高,即可測定氫氣體積,不會導致實驗失敗,故b錯誤;
c.讀數是保證裝置內壓強與外界大氣壓相等,氣體受熱溫度體積會增大,冷卻后體積會減小,應恢復室溫,故c正確,
故答案為:ab;
②將裝置D改為如圖2裝置,橡膠管的作用是:平衡氣壓使分液漏斗中的鹽酸能順利流下;且避免液體體積占位影響氣體體積測定
故答案為:平衡氣壓使分液漏斗中的鹽酸能順利流下;且避免液體體積占位影響氣體體積測定;
(3)制備溶液A,試劑X是將部分氧化為Fe2+氧化成Fe3+,需要選擇具有強氧化性的物質,可以是氯氣、過氧化氫,鐵離子可以氧化二氧化硫,
故答案為:ac;
(4)Fe2+、Fe3+在堿性、加熱條件下反應得到Fe3O4,還有水生成,反應離子方程式為:Fe2++2Fe3++8OH-$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2O,控制Fe2+、Fe3+、OH-的物質的量之比為:1:2:8,制備過程中須持續通入N2的原因是在 N2氣流下,防止Fe2+被氧化,
故答案為:1:2:8;在 N2氣流下,防止Fe2+被氧化;
(5)①鐵離子將碘離子氧化為碘單質,加入淀粉溶液呈藍色,用Na2S2O3溶液滴定滴定碘單質,滴定終點的現象是:溶液藍色褪去,且半分鐘不變色,
故答案為:溶液由藍色變無色,且半分鐘不變色;
②設樣品中鐵(Ⅲ)的物質的量為a,則:
Fe3O4~2Fe3+~I2~2S2O32-
2 2mol
a V×10-3L×cmol•L-1
a=cV×10-3mol,
樣品中Fe(Ⅲ)的質量分數=$\frac{cV×1{0}^{-3}mol×\frac{100}{10}×56g/mol}{mg}$×100%=$\frac{56cV}{m}%$
故答案為:$\frac{56cV}{m}%$.
點評 本題考查物質制備實驗與定量測定實驗,關鍵是對原理的理解,掌握氣體體積測量方法與滴定中關系式計算,熟練掌握元素化合物性質,題目培養了學生分析能力、知識遷移運用能力,題目難度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題
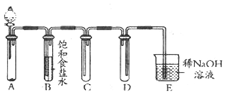 如圖是用KMnO4與濃鹽酸反應制取適量氯氣的簡易裝置.
如圖是用KMnO4與濃鹽酸反應制取適量氯氣的簡易裝置.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在使石蕊試液變紅的溶液中:Na+、K+、Br-、SO42- | |
| B. | 氯化亞鐵溶液中:K+、Al3+、SO42-、MnO4- | |
| C. | 硫酸鋁溶液中:K+、AlO2-、Na+、Cl- | |
| D. | 與鋁反應產生大量氫氣的溶液:NH4+、Na+、SO42-、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加熱 | B. | 通入氯化氫氣體 | ||
| C. | 加入適量的氫氧化鈉溶液 | D. | 加入固體AlCl3 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 4種 | B. | 8種 | C. | 10種 | D. | 12種 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
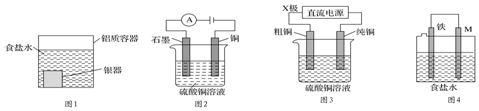
| A. | 用圖1裝置處理銀器表面的黑斑(Ag2S),銀器表面發生的反應為Ag2S+2e-═2Ag+S2-,該過程中總反應為2Al+3Ag2S═6Ag+Al2S3 | |
| B. | 用圖2裝置電解一段時間后,銅電極部分溶解,溶液中銅離子的濃度基本不變 | |
| C. | 圖3裝置中若直流電源的X極為正極,則該裝置可實現粗銅的電解精煉 | |
| D. | 圖4裝置中若M是銅,則該裝置能防止鐵被腐蝕 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com