
【題目】下列關于氮及其化合物說法,不正確的是
A.人體中極少量的NO會促進血管擴張,防止血管栓塞
B.光化學煙霧即為含有二氧化氮的有毒煙霧
C.氨水可作化肥
D.工業硝酸常因溶有少量NO2而略顯黃色
 世紀百通期末金卷系列答案
世紀百通期末金卷系列答案科目:高中化學 來源: 題型:
【題目】硫酸鐵銨[aFe2(SO4) 3·b(NH4) 2SO4·cH2O]廣泛用于城鎮生活飲用水、工業循環水的凈化處理等。某化工廠以硫酸亞鐵(含少量硝酸鈣)和硫酸銨為原料,設計了如下工藝流程制取硫酸鐵銨。

請回答下列問題:
(1)硫酸亞鐵溶液加H2SO4酸化的主要目的是_________,濾渣A的主要成分是________。
(2)下列物質中最適合的氧化劑B是______(填字母);反應的離子方程式___________。
a.NaClO b.H2O2 c.KMnO4 d.K2Cr2O7
(3)操作甲名稱分別是:甲______________,乙為常溫晾干。
(4)上述流程中,氧化之后和加熱蒸發之前,需取少量檢驗Fe2+是否已全部被氧化,所加試劑為__(寫化學式),能否用酸性的KMnO4溶液?_________填“能”或“否”)理由是:_______。(可用語言或方程式說明)
(5)稱取14.00 g樣品,將其溶于水配制成100 mL溶液,分成兩等份,向其中一份中加入足量NaOH溶液,過濾洗滌得到2.14 g沉淀;向另一份溶液中加入0.05 mol Ba(NO3)2溶液,恰好完全反應。則該硫酸鐵銨的化學式為______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】等質量的CH4和NH3相比較,下列結論錯誤的是
A. 它們的分子個數比為17:16 B. 它們的原子個數比為17:16
C. 它們的氫原子個數比為17:12 D. 它們所含氫元素的質量比為17:12
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】選用適當的試劑和除雜方法除去下列各物質中的雜質(括號中為雜質),將所選試劑和操作的名稱填寫在表格中.
序號 | 物質 | 試劑 | 除雜方法 |
① | 甲烷(C2H4) | ||
② | 硝基苯(混合酸) | ||
③ | KNO3(NaCl) |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關試劑的保存方法,錯誤的是
A. 濃硝酸保存在無色玻璃試劑瓶中
B. 少量的鈉保存在煤油中
C. 氫氧化鈉溶液保存在帶橡皮塞的玻璃試劑瓶中
D. 新制的氯水通常保存在棕色玻璃試劑瓶中
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據所學知識完成題目:
(1)將CO2氣體持續通入澄清石灰水中,發現澄清石灰水先渾濁,后又變澄清,寫出在該過程中所涉及的化學方程式:
(2)Cu與濃硫酸反應的化學反應方程式: 其中在此反應中,硫酸體現了什么性質:
(3)海水提鎂中,貝殼的作用是(用化學反應方程式表示):
(4)工業上制備粗硅的化學方程式是:
(5)SiO2是玻璃的成分之一,SiO2與氫氧化鈉溶液反應的化學方程式為 , 工藝師常用(填物質名稱)來雕刻玻璃.
(6)工業上常采用碳酸鹽與石英為原料制取玻璃,請寫出工業制取玻璃的化學反應方程式: .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關食物中營養素的說法正確的是( )
A.維生素C能防治壞血病B.攝入過多的淀粉不會發胖
C.油脂的成分是高級脂肪酸D.蛋白質水解的最終產物是葡萄糖
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】亞硝酸鈉常用作食品防腐劑。現用下圖所示儀器(夾持裝置已省略)及藥品。探究亞硝酸鈉與硫酸的反應及生成氣體產物的成分。巳知氣體液化的溫度:NO2:21℃;NO:-152 ℃
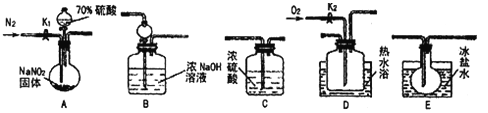
回答下列問題:
(1)為了檢驗裝置A中生成的氣體產物,儀器的連接順序為(按從左到右連接): A→C→___→____→______。
(2)組裝好儀器后,接下來進行的操作是____;實驗開始時通入N2的作用是______.
(3)關閉彈贊夾K1,打開分液漏斗活塞,滴入70%硫酸后,A中產生紅棕色氣體。確認A中產生的氣體中含有NO,依據的現象是__________;裝置E的作用是__________。
(4)根據上述實驗,寫出該反應的化學方程式:__________。
如果沒有裝置C,對驗證結論造成的影響是__________。
(5)實驗結束后還需通入N2的作用是_______;如果向D中通入過量O2,則裝置B中發生反應的離子方程式為_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】飲用水中的NO3﹣對人類健康會產生危害,為了降低飲用水中NO3﹣的濃度,某飲用水研究人員提出,在堿性條件下用鋁粉將NO3﹣還原為N2 , 其化學方程式為Al+NaNO3+NaOH﹣NaAlO2+N2↑+H2O (未配平).請回答下列問題:
(1)上述反應中,元素的化合價升高,則該元素的原子(填“得到”或“失去”)電子;而元素的化合價降低,則該元素的原子被(填“氧化”或“還原”).
(2)配平上述反應:Al+NaNO3+NaOH=NaAlO2+N2↑+H2O
(3)用“雙線橋法”表示反應中電子轉移的方向和數目:
(4)上述反應中若標準狀況下產生11.2L氣體物質,則轉移電子的數目為 .
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com