
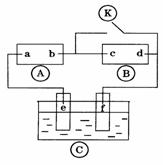
下圖![]() 為直流電源,
為直流電源,![]() 為浸透飽和氯化鈉溶液和酚酞試液的濾紙,
為浸透飽和氯化鈉溶液和酚酞試液的濾紙,![]() 為電鍍槽.斷開
為電鍍槽.斷開![]() ,接通電路后發現
,接通電路后發現![]() 上的c點顯紅色.為實現鐵上鍍銅,接通
上的c點顯紅色.為實現鐵上鍍銅,接通![]() 后,使c、d兩點短路.
后,使c、d兩點短路.
(1)a極為 e極連接的電極材料為
(2)若通電一段時間后,鐵上質量增加1.28g,則電源提供的電量為 庫侖?(每個電子所帶電量為1.6x10-19C,保留兩位小數點)
 (3)若
(3)若![]() 中兩極為石墨電極,電解液為400ml的AgNO3溶液,則e,f兩極的電極反應式分別為 ,
中兩極為石墨電極,電解液為400ml的AgNO3溶液,則e,f兩極的電極反應式分別為 ,
通過和(2)相同的電量后溶液的PH為 (假設電解后溶液體積不變,PH= -lgc(H+) )
 名師伴你成長課時同步學練測系列答案
名師伴你成長課時同步學練測系列答案科目:高中化學 來源: 題型:
(10分)高錳酸鉀是深紫色的針狀晶體,是最常用的氧化劑之一,工業上以軟錳礦(主要成分是MnO2)為原料制備高錳酸鉀。下面是實驗室制取高錳酸鉀的過程:
①稱取15g固體KOH和8g固體KClO3,導入坩堝內,混合均勻,小火加熱,并用鐵棒攪拌。待混合物熔融后,一面攪拌,一面將10gMnO2粉末分批加入。隨著反應的進行,熔融物的粘度逐漸增大,此時用力攪拌,待反應物干涸后,再強熱5~10min。
②待熔體冷卻后,從坩堝內取出,放入250mL燒杯中,用80mL蒸餾水分批浸取,并不斷攪拌,加熱以促進其溶解。趁熱減壓過濾浸取液,即可得到墨綠色的K2MnO4溶液。
③將K2MnO4溶液倒入燒杯中,加熱至60℃,按如圖所示進行電解。陽極是光滑的鎳片,卷成圓筒狀,陰極為粗鐵絲。接通直流電源,高錳酸鉀在陽極析出沉于燒杯底部,溶液由墨綠色逐漸轉為紫紅色,電解1h后,停止通電,取出電極。在冷水中冷卻電解液,使結晶完全,用玻璃砂布氏漏斗將晶體抽干,稱重,計算產率。
回答下列問題:
(1)步驟①發生的反應方程式為______________________________
(2)步驟①中共熔時要選擇__________坩堝(填“鐵”、“陶瓷”或“石英”)。
(3)寫出步驟③中發生的電極反應式:
陽極____________________________ 陰極________________________
(4)實驗中用到抽濾操作,抽濾裝置如下圖所示,儀器B的名稱是___________。抽濾完畢,吸濾瓶內的液體從_____________________倒出。步驟③抽濾時使用玻璃砂布氏漏斗的原因是_________________________________________________
查看答案和解析>>
科目:高中化學 來源:2012屆浙江省寧波四中高三第一學期期末考試化學試卷 題型:實驗題
(10分)高錳酸鉀是深紫色的針狀晶體,是最常用的氧化劑之一,工業上以軟錳礦(主要成分是MnO2)為原料制備高錳酸鉀。下面是實驗室制取高錳酸鉀的過程:
①稱取15g固體KOH和8g固體KClO3,導入坩堝內,混合均勻,小火加熱,并用鐵棒攪拌。待混合物熔融后,一面攪拌,一面將10gMnO2粉末分批加入。隨著反應的進行,熔融物的粘度逐漸增大,此時用力攪拌,待反應物干涸后,再強熱5~10min。
②待熔體冷卻后,從坩堝內取出,放入250mL燒杯中,用80mL蒸餾水分批浸取,并不斷攪拌,加熱以促進其溶解。趁熱減壓過濾浸取液,即可得到墨綠色的K2MnO4溶液。
③將K2MnO4溶液倒入燒杯中,加熱至60℃,按如圖所示進行電解。陽極是光滑的鎳片,卷成圓筒狀,陰極為粗鐵絲。接通直流電源,高錳酸鉀在陽極析出沉于燒杯底部,溶液由墨綠色逐漸轉為紫紅色,電解1h后,停止通電,取出電極。在冷水中冷卻電解液,使結晶完全,用玻璃砂布氏漏斗將晶體抽干,稱重,計算產率。
回答下列問題:
(1)步驟①發生的反應方程式為______________________________
(2)步驟①中共熔時要選擇__________坩堝(填“鐵”、“陶瓷”或“石英”)。
(3)寫出步驟③中發生的電極反應式:
陽極____________________________ 陰極________________________
(4)實驗中用到抽濾操作,抽濾裝置如下圖所示,儀器B的名稱是___________。抽濾完畢,吸濾瓶內的液體從_____________________倒出。步驟③抽濾時使用玻璃砂布氏漏斗的原因是_________________________________________________
查看答案和解析>>
科目:高中化學 來源:2015屆湖北省高二上學期期中考試化學試卷(解析版) 題型:填空題
(9分)某種碳酸錳礦的主要成分有MnCO3、MnO2、FeCO3、MgO、SiO2、Al2O3等。已知碳酸錳難溶于水。一種運用陰離子膜電解法的新技術可用于從碳酸錳礦中提取金屬錳,流程如下:

陰離子膜法電解裝置如下圖所示:

(1)寫出用稀硫酸溶解碳酸錳反應的離子方程式: 。
(2)已知Ksp
(Fe(OH)3) = 4 ´10–38,假設溶液中Fe3+離子濃度為0.1 mol·L–1,則開始生成Fe(OH)3
沉淀的pH是_________,沉淀完全的pH是_________。(可能用到的數據:lg =
-0.1 lg
=
-0.1 lg =0.2)
=0.2)
(3)已知不同金屬離子生成氫氧化物沉淀所需的pH如下表:
|
離子 |
Fe3+ |
A13+ |
Fe2+ |
Mn2+ |
Mg2+ |
|
開始沉淀的pH |
1.2 |
3.7 |
7.0 |
7.8 |
9.3 |
|
沉淀完全的pH |
3.7 |
4.7 |
9.6 |
9.8 |
10.8 |
加氨水調節溶液的pH等于6,則“濾渣(待處理)”的成分是 (寫化學式),濾液中含有的陽離子有H+和 (寫符號)。
(4)在浸出液里錳元素只以Mn2+的形式存在,且濾渣A中也無MnO2,請用離子方程式解釋原因: 。
(5)電解裝置中箭頭表示溶液中陰離子移動的方向,則A電極是直流電源的 極。實際生產中,陽極以稀硫酸為電解液,陽極的電極反應式為 。
(6)該工藝之所以采用陰離子交換膜,是為了防止Mn2+進入陽極區發生副反應生成MnO2造成資源浪費,寫出該副反應的電極反應式: 。
查看答案和解析>>
科目:高中化學 來源:2011-2012學年浙江省高三第一學期期末考試化學試卷 題型:實驗題
(10分)高錳酸鉀是深紫色的針狀晶體,是最常用的氧化劑之一,工業上以軟錳礦(主要成分是MnO2)為原料制備高錳酸鉀。下面是實驗室制取高錳酸鉀的過程:

①稱取15g固體KOH和8g固體KClO3,導入坩堝內,混合均勻,小火加熱,并用鐵棒攪拌。待混合物熔融后,一面攪拌,一面將10gMnO2粉末分批加入。隨著反應的進行,熔融物的粘度逐漸增大,此時用力攪拌,待反應物干涸后,再強熱5~10min。
②待熔體冷卻后,從坩堝內取出,放入250mL燒杯中,用80mL蒸餾水分批浸取,并不斷攪拌,加熱以促進其溶解。趁熱減壓過濾浸取液,即可得到墨綠色的K2MnO4溶液。
③將K2MnO4溶液倒入燒杯中,加熱至60℃,按如圖所示進行電解。陽極是光滑的鎳片,卷成圓筒狀,陰極為粗鐵絲。接通直流電源,高錳酸鉀在陽極析出沉于燒杯底部,溶液由墨綠色逐漸轉為紫紅色,電解1h后,停止通電,取出電極。在冷水中冷卻電解液,使結晶完全,用玻璃砂布氏漏斗將晶體抽干,稱重,計算產率。
回答下列問題:
(1)步驟①發生的反應方程式為______________________________
(2)步驟①中共熔時要選擇__________坩堝(填“鐵”、“陶瓷”或“石英”)。
(3)寫出步驟③中發生的電極反應式:
陽極____________________________ 陰極________________________
(4)實驗中用到抽濾操作,抽濾裝置如下圖所示,儀器B的名稱是___________。抽濾完畢,吸濾瓶內的液體從_____________________倒出。步驟③抽濾時使用玻璃砂布氏漏斗的原因是_________________________________________________

查看答案和解析>>
科目:高中化學 來源:湖南省模擬題 題型:單選題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com