
某含少量FeCl2雜質的FeCl3樣品,現要測定其中鐵元素的含量。實驗步驟如下:
①準確稱量m g樣品(2~3g);
②向樣品中加入10mL 5mol/L的鹽酸,再加入蒸餾水,配制成250mL溶液;
③量取25mL操作②中配得的溶液,加入3mL溴水,加熱使Fe2+完全被氧化;
④趁熱迅速加入濃度為10%的氨水至過量,充分攪拌,使之完全沉淀;
⑤過濾,將沉淀洗滌、灼燒、冷卻稱量,反復操作至恒重。
請根據上面的敘述回答:
(1)若稱量前,托盤天平的指針偏向標尺左方;稱量讀數時,指針剛好在標尺的中間,則所得樣品的質量 。
A.比m g多 B.比m g少 C.恰好為m g
(2)溶解樣品時要加入鹽酸,原因是 。
(3)配250mL溶液時,除需250mL容量瓶、燒杯外,還需用到的玻璃儀器是 、 。
(4)加入溴水時發生反應的離子方程式是 。
(5)若坩堝質量為W1 g,坩堝與灼燒后固體的總質量是W2 g,則樣品中鐵元素的質量分數是 。
(6)若在配制250mL溶液時,所用的容量瓶沒有洗干凈。當含有下列物質時,最終會使鐵元素的測定含量:①NaCl ;②Fe2(SO4)3 (填“偏高”、“偏低”或“不變”)。
科目:高中化學 來源: 題型:閱讀理解
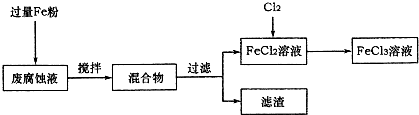
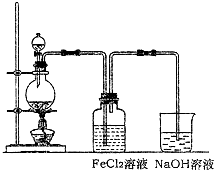
| ||
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:
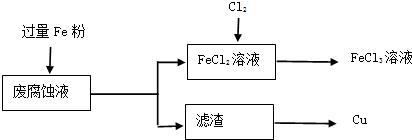
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com