
【題目】四氧化三鐵俗稱為磁性氧化鐵,通常用作顏料、拋光劑和電訊器材等。某化學興趣小組取磁性氧化鐵進行鋁熱反應實驗并對產物進行探究。
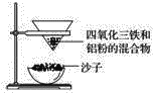
(1)取磁性氧化鐵按圖裝置進行鋁熱反應,引發鋁熱反應的實驗操作是__________。
(2)取少許反應生成的“鐵塊”溶于鹽酸,滴加硫氰化鉀溶液后溶液不變紅,則______(填“能”或“不能”)說明“鐵塊”一定不含四氧化三鐵,理由是_________。
(3)設計一個簡單的實驗方案,證明上述所得的“鐵塊”中含有金屬鋁,該實驗所用的試劑是__________,反應的離子方程式為___________。
(4)請寫出此鋁熱反應的化學方程式:_____________。
【答案】鋪上氯酸鉀,插鎂條并將其點燃 不能 產物中生成的鐵和可能未反應完的鋁能還原溶液中的鐵離子,所以溶液不變紅,因而不能說明“鐵塊”一定不含四氧化三鐵 氫氧化鈉溶液 2Al+2OH-+2H2O=2![]() +3H2↑ 8Al+3Fe3O4
+3H2↑ 8Al+3Fe3O4![]() 4Al2O3+9Fe
4Al2O3+9Fe
【解析】
(1)鋁熱反應的引發:鋁熱劑上鋪KClO3,插鎂條并將其點燃即可;
(2)鐵單質能把鐵離子還原為亞鐵離子;
(3)金屬鐵和氫氧化鈉不反應,但金屬鋁可以和氫氧化鈉反應放出氫氣;
(4)四氧化三鐵和鋁反應生成鐵和氧化鋁。
(1)取磁性氧化鐵按圖裝置進行鋁熱反應,引發鋁熱反應的實驗操作是:鋁熱劑上鋪上氯酸鉀,插鎂條并將其點燃。
(2)取少許反應生成的“鐵塊”溶于鹽酸,滴加硫氰化鉀溶液后溶液不變紅,不能說明“鐵塊”一定不含四氧化三鐵 ,理由是:產物中的鐵單質和可能未反應完的鋁能還原溶液中的鐵離子,所以溶液不變紅,因而不能說明“鐵塊”一定不含四氧化三鐵。
(3)證明上述所得的“鐵塊”中含有金屬鋁簡單的實驗方案是用氫氧化鈉溶液,取該鐵塊,向其中加入氫氧化鈉溶液,若固體溶解,同時產生無色無味的氣體,則證明含有鋁,反應的離子方程式是2Al+2OH-+2H2O=2![]() +3H2↑。
+3H2↑。
(4)在高溫下,鋁與四氧化三鐵發生鋁熱反應,生成氧化鋁和鐵,反應方程式是8Al+3Fe3O4![]() 4Al2O3+9Fe。
4Al2O3+9Fe。


科目:高中化學 來源: 題型:
【題目】(1)已知:Al2O3(s)+3C(s)=2Al(s)+3CO(g) ΔH1=+1 344.1 kJ·mol-1,2AlCl3(g)=2Al(s)+3Cl2(g) ΔH2=+1 169.2 kJ·mol-1,由Al2O3、C和Cl2反應生成AlCl3的熱化學方程式為______________。
(2)貯氫合金ThNi5可催化由CO、H2合成CH4 的反應。已知溫度為T時:CH4(g)+2H2O(g)=CO2(g)+4H2(g) ΔH=+165 kJ·mol-1,CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41 kJ·mol-1,溫度為T時,該反應的熱化學方程式為__________。
(3)FeSO4可轉化為FeCO3,FeCO3在空氣中加熱反應可制得鐵系氧化物材料。已知25 ℃,101 kPa時:4Fe(s)+3O2(g)=2Fe2O3(s) ΔH=-1 648 kJ·mol-1,C(s)+O2(g)=CO2(g) ΔH=-393 kJ·mol-1 2Fe(s)+2C(s)+3O2(g)=2FeCO3(s) ΔH=-1 480 kJ·mol-1,FeCO3在空氣中加熱反應生成Fe2O3的熱化學方程式是______。
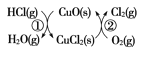
(4)用O2將HCl轉化為Cl2,可提高效益,減少污染。 傳統上該轉化通過如圖所示的催化循環實現,其中,反應①為:2HCl(g)+CuO(s)![]() H2O(g)+CuCl2(s) ΔH1,反應②生成1 mol Cl2(g)的反應熱為ΔH2,則總反應的熱化學方程式為________(反應熱用ΔH1和ΔH2表示)。
H2O(g)+CuCl2(s) ΔH1,反應②生成1 mol Cl2(g)的反應熱為ΔH2,則總反應的熱化學方程式為________(反應熱用ΔH1和ΔH2表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氨是一種重要的化工產品,也是重要的化工原料。某化學小組在實驗室制備氨并完成相關性質實驗。
(1)實驗一:用如圖所示裝置制備并收集 NH3。
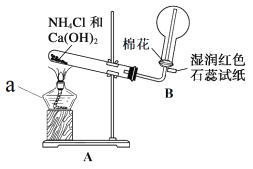
儀器 a 的名稱為____________,裝置 A 中產生 NH3 的化學方程式為____________, 裝置 B 中用圓底燒瓶收集 NH3 的方法為____________(填“向上排空氣法”或“向下 排空氣法”),當濕潤紅色石蕊試紙顏色變為____________色,表示已經收集滿 NH3。
(2)實驗二:用如圖所示裝置進行 NH3 的噴泉實驗。
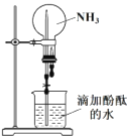
引發該噴泉實驗的操作是先____________,再打開止水夾,使燒杯內的水通過導管進入燒瓶形成噴泉,說明 NH3 具有的物理性質是____________,燒瓶內溶液呈紅色, 說明 NH3 的水溶液呈____________性。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】明礬石的主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O,含有少量氧化鐵,利用明礬石制備K2SO4的工藝流程如圖所示:
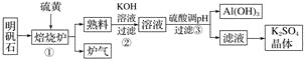
據此流程圖回答下列問題:
(1)①焙燒爐中Al2(SO4)3與S反應的產物是兩種氧化物,該反應的化學方程式為______;寫出爐氣的一種用途________。
(2)②中Al2O3參與反應的離子方程式為__________。
(3)③中調節pH不能用CO2的理由是____________________。
(4)工業冶煉金屬鋁需要定期更換補充陽極碳塊的原因是__________________。
(5)純凈氫氧化鋁經歷兩次__________________(填反應類型)可制得鋁。以Al和NiO(OH)為電極,NaOH溶液為電解液組成一種新型電池,放電時NiO(OH)轉化為Ni(OH)2,該電池負極的電極反應式是__________________。
(6)現有明礬石1 625 t,按上述流程制得780 t Al(OH)3,忽略鋁元素的損失,請計算明礬石中鉀元素的質量分數為____________%。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據提供的情境書寫指定反應的方程式。
(1)工業上以碳酸錳礦(主要成分為MnCO3,另含少量FeO、Fe2O3、CaO等雜質)為主要原料生產二氧化錳的工藝流程如下:
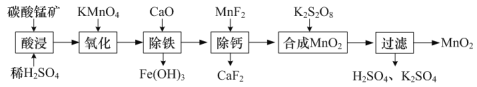
①“酸浸”時MnCO3發生反應的離子方程式為______。
②“氧化”時MnO![]() 轉化為Mn2+,該反應的離子方程式為_____。
轉化為Mn2+,該反應的離子方程式為_____。
③“合成MnO2”的化學方程式為______。
(2)氮氧化物是造成大氣污染的重要因素。
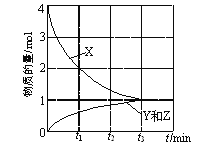
①在高壓下,NO在40 ℃下分解生成兩種化合物,體系中各組分的物質的量隨時間變化曲線如圖所示。NO分解的化學方程式為______。
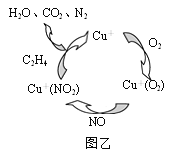
②一種以乙烯作為還原劑的脫硝(NO)機理示意圖如圖所示,該脫硝機理總反應的化學方程式為____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物G是一種重要的有機產品,其合成路線如下:
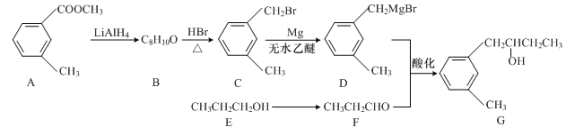
(1)E→F的反應還需的反應物和反應條件為_____。
(2)B的結構簡式是_____。
(3)寫出同時滿足下列條件的A的一種同分異構體的結構簡式:_______。
①分子中有4種不同化學環境的氫;
②能發生銀鏡反應和水解反應,且1mol該物質最多能與2mol NaOH反應。
(4)寫出以![]() 和CH3CHO為原料,制備
和CH3CHO為原料,制備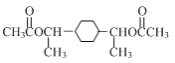 的合成路線流程圖(無機試劑和有機溶劑任用,合成路線流程圖示例見本題題干)。_____
的合成路線流程圖(無機試劑和有機溶劑任用,合成路線流程圖示例見本題題干)。_____
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)現有CuO和Fe2O3組成的混合物ag,向其中加入2 molL﹣1的硫酸溶液50 mL,恰好完全反應。若將ag該混合物在足量H2中加熱,使其充分反應,計算冷卻后剩余固體質量_________。
(2)取一定量的CuO粉末與0.5 L稀硫酸充分反應后,將一根50 g鐵棒插入上述溶液中,至鐵棒質量不再變化時,鐵棒增重0.24 g。并收集到224 mL氣體(標準狀況)。求此CuO粉末的質量_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上通常利用SiO2 和碳反應來制取硅,寫出反應的化學方程式___________________。
工業上還可以利用鎂制取硅,反應為2Mg+SiO2 = 2MgO+Si,同時會發生副反應:2Mg + Si = Mg2Si。如圖是進行Mg與SiO2反應的實驗裝置,試回答下列問題:

(1)由于O2和H2O(g)的存在對該實驗有較大影響,實驗中應通入氣體X作為保護氣,試管中的固體藥品可選用________(填序號)。
a.石灰石 b.鋅粒 c.純堿
(2)實驗開始時,必須先通一段時間X氣體,再加熱反應物,其理由是 ___________________________;當反應引發后,移走酒精燈,反應能繼續進行,其原因是______________________。
(3)反應結束后,待冷卻至常溫時,往反應后的混合物中加入稀鹽酸,可觀察到閃亮的火星,產生此現象的原因是副產物Mg2Si遇鹽酸迅速反應生成SiH4(硅烷)氣體,然后SiH4自燃.用化學方程式表示這兩個反應①________________________②___________________.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,通過下列反應可以制備特種陶瓷的原料MgO, MgSO3(s) + CO(g)![]() MgO(s) + CO2(g) +SO2(g) △H>0。該反應在恒容的密閉容器中達到平衡后,若僅改變圖中橫坐標x的值,重新達到平衡后,縱坐標y隨x變化趨勢合理的是
MgO(s) + CO2(g) +SO2(g) △H>0。該反應在恒容的密閉容器中達到平衡后,若僅改變圖中橫坐標x的值,重新達到平衡后,縱坐標y隨x變化趨勢合理的是

選項 | x | y |
A | 溫度 | 容器內混合氣體的密度 |
B | CO的物質的量 | CO2與CO的物質的量之比 |
C | SO2的濃度 | 平衡常數K |
D | MgSO4的質量(忽略體積) | CO的轉化率 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com