
| 實驗步驟(不要求寫出具體操作過程) | 預期實驗現象和結論 |
| 取少量黑色固體, |
| ||
| ||
| ||
| ||
| ||


 一課一練課時達標系列答案
一課一練課時達標系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
 乙醛在氧化銅催化劑存在的條件下,可以被空氣氧化成乙酸.依據此原理設計實驗制得并在試管C中收集到少量乙酸溶液(如圖所示:試管A中裝有40%的乙醛水溶液、氧化銅粉末;試管C中裝有適量蒸餾水;燒杯B中裝有某液體).已知在60℃~80℃時用雙連打氣球鼓入空氣即可發生乙醛的氧化反應,連續鼓入十幾次反應基本完全.有關物質的沸點見下表:
乙醛在氧化銅催化劑存在的條件下,可以被空氣氧化成乙酸.依據此原理設計實驗制得并在試管C中收集到少量乙酸溶液(如圖所示:試管A中裝有40%的乙醛水溶液、氧化銅粉末;試管C中裝有適量蒸餾水;燒杯B中裝有某液體).已知在60℃~80℃時用雙連打氣球鼓入空氣即可發生乙醛的氧化反應,連續鼓入十幾次反應基本完全.有關物質的沸點見下表:| 物質 | 乙醛 | 乙酸 | 甘油 | 乙二醇 | 水 |
| 沸點 | 20.8℃ | 117.9℃ | 290℃ | 197.2℃ | 100℃ |
查看答案和解析>>
科目:高中化學 來源: 題型:
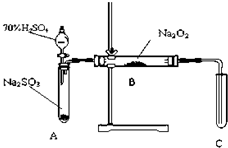 化學興趣小組同學運用類比學習的思想,探究過氧化鈉與二氧化硫的反應.小組同學改進了如圖所示的裝置進行實驗制取SO2的反應.充分反應,B中固體由淡黃色變為白色(Na2O2完全反應),將帶火星的木條插入試管C中,木條復燃.試回答下列問題:
化學興趣小組同學運用類比學習的思想,探究過氧化鈉與二氧化硫的反應.小組同學改進了如圖所示的裝置進行實驗制取SO2的反應.充分反應,B中固體由淡黃色變為白色(Na2O2完全反應),將帶火星的木條插入試管C中,木條復燃.試回答下列問題:| 實驗操作 | 預期現象與結論 |
| 步驟1:取少量白色固體于試管,加入 | 若 |
| 步驟2:在步驟1反應后的溶液加入 | 若 |
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
| A、0.1 mol?L-1 Na2S溶液中:c(OH-)=c(H+)+c(HS-)+2c(H2S) |
| B、0.1 mol?L-1 pH=8的NH4HCO3溶液中:c(HCO3-)>c(NH4+)>c(OH-)>c(H+) |
| C、濃度均為0.1 mol?L-1的NH3?H2O溶液和NH4Cl溶液等體積混合:c(NH4+)+c(H+)>c(NH3?H2O)+c(OH-) |
| D、0.1 mol?L-1 Na2S溶液與0.1 mol?L-1 NaHS溶液等體積混合:2c(Na+)-3c(S2-)=3c(HS-)+3c(H2S) |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、CuS |
| B、Cu(NO3)2 |
| C、Cu(OH)2 |
| D、CuCO3 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com