
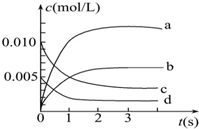
 在2L密閉容器內,800℃時發生反應:2NO(g)+O2(g)═2NO2(g),在體系中,n(NO)隨時間的變化如表:
在2L密閉容器內,800℃時發生反應:2NO(g)+O2(g)═2NO2(g),在體系中,n(NO)隨時間的變化如表:| 時間(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| NO的物質的量(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
分析 (1)根據表中數據可知,3s時NO為0.007mol,且不再隨著時間的推移而減小,所以反應不能完全進行,據此判斷反應是否是可逆反應,NO轉化率=$\frac{消耗量}{起始量}$×100%;
(2)從圖象分析,隨反應時間的延長,各物質的濃度不再不變,且反應物沒有完全反應,是可逆反應,根據一氧化氮物質的量的變化知,該反應向正反應方向移動,則二氧化氮的物質的量在不斷增大,且同一時間段內,一氧化氮減少的物質的量等于二氧化氮增加的物質的量;
根據△v=$\frac{\frac{△n}{V}}{△t}$計算一氧化氮的反應速率,再結合同一化學反應同一時間段內,各物質的反應速率之比等于其計量數之比計算氧氣的反應速率;
(3)化學平衡的標志是正逆反應速率相同,各組分含量保持不變.
解答 解:(1)根據表中數據可知,3s時NO為0.007mol,且不再隨著時間的推移而減小,所以反應不能完全進行,所以該反應是可逆反應,NO轉化率=$\frac{0.02mol-0007mol}{0.02mol}$×100%=65%,
故答案為:是;65%;
(2)從圖象分析,隨反應時間的延長,各物質的濃度不再不變,且反應物沒有完全反應,所以反應為可逆反應,根據一氧化氮物質的量的變化知,該反應向正反應方向移動,則二氧化氮的物質的量在不斷增大,且同一時間段內,一氧化氮減少的物質的量等于二氧化氮增加的物質的量,所以表示NO2的變化的曲線是b,
0~2s內v(NO)=$\frac{\frac{0.02mol-0.008mol}{2L}}{2s}$=0.0030mol/(L.s),同一化學反應同一時間段內,各物質的反應速率之比等于其計量數之比,所以氧氣的反應速率=$\frac{1}{2}$v(NO)=0.0015mol/(L•s),
故答案為:b,0.0015mol/(L•s);
②a.反應速率之比等于化學方程式計量數之比,v(NO2)=2v(O2)為正反應速率之比,不能說明正逆反應速率相同,無法判斷正逆反應速率是否相等,故a錯誤;
b.反應前后氣體體積不同,壓強不變說明正逆反應速率相等,各組分濃度不變,故b正確;
c.反應速率之比等于化學方程式計量數之比為正反應速率之比,v逆(NO)=2v正(O2)時,一氧化氮正逆反應速率相同,說明反應達到平衡狀態,故c正確;
d.恒容容器,反應物生成物都是氣體質量不變,體積不變,所以密度始終不變,不能說明反應達到平衡狀態,故d錯誤;
故選bc,
故答案為:bc
點評 本題考查了可逆反應的判斷、反應速率的計算、影響反應速率及化學平衡狀態的判斷,注意壓強、密度不變時平衡狀態的判斷為易錯點,題目難度中等.


科目:高中化學 來源: 題型:解答題
 .
. .
.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
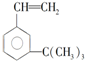 有如下性質:
有如下性質: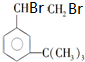 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 可根據硫酸密度的大小判斷鉛蓄電池是否需要充電 | |
| B. | 當物質中的化學鍵發生斷裂時,一定發生化學變化 | |
| C. | 淀粉和纖維素的化學式均為(C6H10O5)n,故互為同分異構體 | |
| D. | 只由一種元素的陽離子與另一種元素的陰離子組成的物質一定是純凈物 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
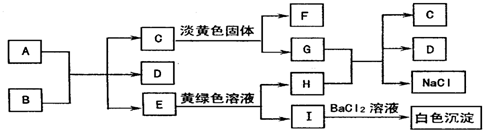
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
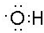 ;
;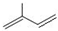 ;
;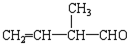 所含官能團的名稱是碳碳雙鍵、醛基;該有機物發生加聚反應后,所得產物的結構簡式為
所含官能團的名稱是碳碳雙鍵、醛基;該有機物發生加聚反應后,所得產物的結構簡式為 .
.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
 已知:1molC、1molCO分別按下式反應(燃燒):
已知:1molC、1molCO分別按下式反應(燃燒):查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 .
. .
.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com