
【題目】已知非金屬單質硫(S)是淡黃色固體粉末,難溶于水。為了驗證氯元素的非金屬性比硫元素的非金屬性強,某化學實驗小組設計了如下實驗,請回答下列問題:

(1)裝置A的分液漏斗中盛裝的試劑是 ,燒瓶中加入的試劑是 。
(2)虛線框內的實驗裝置的作用 。
(3)裝置B中盛放的試劑是 (選填下列所給試劑的代碼),實驗現象為 ,化學反應方程式是 ,該反應屬于四種基本反應類型中的 _______反應。
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(4)還有哪些事實能夠說明氯元素的非金屬性比硫元素的非金屬性強(試舉一例)。
【答案】(1)濃鹽酸 二氧化錳(2)除去Cl2中混有的氯化氫 (3)A 溶液變渾濁或有淺黃色沉淀產生 Cl2+Na2S=2NaCl+S↓ 置換(4)3Cl2+2Fe=2FeCl3 S+Fe="FeS" ;或答HCl比H2S穩定。
【解析】試題分析:(1)為了驗證氯元素的非金屬性比硫元素強,利用的是氯氣與硫化鈉的反應,因此裝置A是制取氯氣的裝置,故裝置A中分液漏斗中盛裝的試劑為濃鹽酸,而燒瓶中加入的試劑是二氧化錳;
(2)由于制得的氯氣中含有HCl雜質,因此虛線框內的實驗裝置的作用是除去除去Cl2中混有的氯化氫;
(3)裝置B的作用是驗證氯元素的非金屬性比硫元素強,因此裝置B中盛放的試劑是Na2S溶液,實驗現象是溶液變渾濁或有淺黃色沉淀產生,發生的反應的化學方程式為:Cl2+Na2S=2NaCl+S↓,該反應屬于置換反應;
(4)能夠證明氯元素的非金屬性比硫元素強的實驗事實有:Cl2比S更容易與H2發生反應;HCl比H2S穩定;Cl2能把Fe氧化到+3價態,而S只能把Fe氧化到+2價態等等。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】下圖是8種有機化合物的轉換關系:
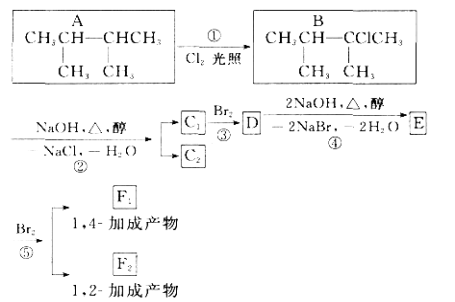
請回答下列問題:
(1)上述框圖中,①是________反應,③是________反應(填反應類型)。
(2)化合物E是重要的工業原料,寫出由D生成E的化學方程式:_______________________________________________________________。
(3) C 1的結構簡式是______________________;F 1的結構簡式是_____________________________。
(4) 上述8種化合物中,屬于二烯烴的是_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】右圖為濃硫酸與銅片反應的裝置。請回答:
(1)濃硫酸與銅片反應的化學方程式為 。

(2)反應一段時間后,試管乙中品紅溶液的現象是 。
(3)下列有關該實驗的說法中,不正確的是 。
A.該反應中濃硫酸只體現酸性
B.試管乙中含有堿液的棉花,其作用是吸收過量的SO2,防止環境污染
C.反應一段時間后,將試管甲中的溶液緩慢倒入盛有水的燒杯,溶液顯藍色
D.含0.04mol溶質的濃硫酸與足量的銅片反應,能收集到448mL的SO2(標準狀況)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】近來, 科學家研制了一種新型的乙醇電池(DEFC), 它用磺酸類質子作溶劑, 在200℃左右時供電, 乙醇電池比甲醇電池效率高出32倍且更加安全。電池總反應式為: C2H5OH+3O2 ![]() 2CO2+3H2O。下列說法不正確的是
2CO2+3H2O。下列說法不正確的是
A.C2H5OH在電池的負極上參加反應 B.1 mol乙醇被氧化轉移6 mol電子
C.在外電路中電子由負極沿導線流向正極 D.電池正極得電子的物質是O2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氫氣是清潔的能源,也是重要的化工原料,根據以下兩種制氫方法。完成下列問題:
(1)方法一:H2S熱分解法,反應式為:2H2S(g)![]() 2H2(g)+S2(g)△H
2H2(g)+S2(g)△H
在恒容密閉容器中,測定H2S分解的轉化率(H2S的起始濃度均為cmol/L),測定結果見右圖,圖中曲線a表示H2S的平衡轉化率與溫度關系,曲線表示不同溫度下反應經過相同時間未達到化學平衡時H2S的轉化率。

①△H______0,(“>”、“<”或“=”),
②若985℃時,反應經tmin達到平衡,此時H2S的轉化率為40%,則tmin內反應速率v(H2)=______(用含c、t的代數式表示)。
③請說明隨溫度的升高,曲線b向曲線a接近的原因:______。
(2)方法二:以CaO為吸收體,將生物材質(以C計)與水蒸氣反應制取H2.相關主要反應如下:
I:C(s)+H2O(g)═CO(g)+H2(g) △H=+131.0kJ/mol
Ⅱ:CO(g)+H2O(g)═CO2(g)+H2(g) △H=-43kJ/mol
Ⅲ:CaO(s)+CO2(g)═CaCO3(s) △H=-178.3kJ/mol
①計算反應C(s)+2H2O(g)+CaO(s)![]() CaCO3(s)+2H2(g)的△H=______;
CaCO3(s)+2H2(g)的△H=______;
若K1、K2、K3分別為反應I、Ⅱ、Ⅲ的平衡常數,該平衡常數K=_____________(用K1、K2、K3表示)。
②對于可逆反應C(s)+2H2O(g)+CaO(s)![]() CaCO3(s)+2H2(g),采取以下措施可以提高H2產率的是______。(填字母編號)
CaCO3(s)+2H2(g),采取以下措施可以提高H2產率的是______。(填字母編號)
A.降低體系的溫度
B.壓縮容器的體積
C.適當增加水蒸氣的通入量
D.增加CaO的量
③下圖為反應I在一定溫度下,平衡時各氣體體積百分含量隨壓強變化的關系圖。若反應達某一平衡狀態時,測得c(H2O)=2c(H2)=2c(CO)=2mol/L,試根據H2O的體積百分含量變化曲線,補充完整CO的變化曲線示意圖。
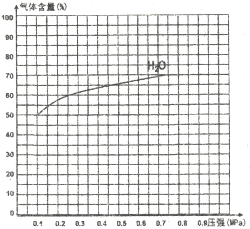
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】莫沙朵林是一種鎮痛藥,它的合成路線如下:
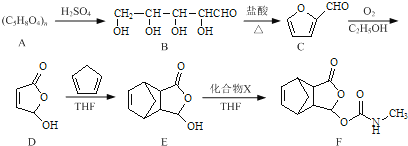
(1)B中手性碳原子數為____________;化合物D中含氧官能團的名稱為____________。
(2)C與新制氫氧化銅反應的化學方程式為____________。
(3)寫出同時滿足下列條件的E的一種同分異構體的結構簡式:____________
I.核磁共振氫譜有4個峰;
Ⅱ.能發生銀鏡反應和水解反應;
Ⅲ.能與FeCl3溶液發生顯色反應.
(4)已知E+X→F為加成反應,化合物X的結構簡式為____________。
(5)已知:![]() .化合物
.化合物 是合成抗病毒藥阿昔洛韋的中間體,請設計合理方案以
是合成抗病毒藥阿昔洛韋的中間體,請設計合理方案以![]() 和
和![]() 為原料合成該化合物(用合成路線流程圖表示,并注明反應條件).合成路線流程圖示例如下:
為原料合成該化合物(用合成路線流程圖表示,并注明反應條件).合成路線流程圖示例如下:![]() 。
。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】【化學—選修2 化學與技術】
Ⅰ.下列有關敘述正確的是( )
A.堿性鋅錳電池中,MnO2是催化劑
B.銀鋅紐扣電池工作時,Ag2O被還原為Ag
C.放電時,鉛酸蓄電池中硫酸濃度不斷增大
D.電鍍時,待鍍的金屬制品表面發生還原反應
Ⅱ.鋅是一種應用廣泛的金屬,目前工業上主要采用“濕法”工藝冶煉鋅,某含鋅礦的主要成分為ZnS(還含少量FeS等其他成分),以其為原料冶煉鋅的工藝流程如圖所示:

回答下列問題:
(1)硫化鋅精礦的焙燒在氧氣氣氛的沸騰爐中進行,所產生焙砂的主要成分的化學式為 。
(2)焙燒過程中產生的含塵煙氣可凈化制酸,該酸可用于后續的 操作。
(3)浸出液“凈化”過程中加入的主要物質為 ,其作用是 。
(4)電解沉積過程中的陰極采用鋁板,陽極采用Pb-Ag合金惰性電極,陽極逸出的氣是 。
(5)改進的鋅冶煉工藝,采用了“氧壓酸浸”的全濕法流程,既省略了易導致空氣污染的焙燒過程,又可獲得一種有工業價值的非金屬單質。“氧壓酸浸”中發生主要反應的離子方程式為 。
(6)我國古代曾采用“火法”工藝冶煉鋅,明代宋應星著的《天工開物》中有關于“升煉倭鉛”的記載:“爐甘石十斤,裝載入一泥罐內,……,然后逐層用煤炭餅墊盛,其底鋪薪,發火煅紅,……,冷淀,毀罐取出,……,即倭鉛也。”該煉鋅工藝過程主要反應的化學方程式為 。(注:爐甘石的主要成分為碳酸鋅,倭鉛是指金屬鋅)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】砷(As)是第四周期第VA族元素,它在自然界中的含量不高,但人類認識它、研究它的歷史卻很長。
(1)已知H3AsO3是兩性偏酸性的化合物,H3AsO3中As的化合價為_____,它與足量硫酸反應時生成鹽的化學式為_______________。Na2HAsO3溶液呈堿性,原因是_________________(用離子方程式表示),該溶液中c(H2AsO3-) _____c(AsO33-)(填”>”、“<”或“=”)。
(2)砷在自然界中主要以硫化物形式(如雄黃As4S4、雌黃As2S3等)存在。
①工業上以雄黃為原料制備砷、鑒定砒霜(As2O3)的原理如下圖:

反應a產生的廢氣直接排放可能帶來的環境問題是__________ _____,請寫出反應b的化學方程式:_________________________。
②雌黃可被濃硝酸氧化為H3AsO4與S,硝酸被還原為NO2,反應中還原劑與氧化劑物質的量之比為_________。
③向c(As3+)=0.01mol/L的工業廢水中加入FeS固體至砷完恰好完全除去(小于1×10-5mol/L),則此時c(Fe2+)=_____mol/L。(已知Ksp(As2S3)=1×10-22,Ksp(FeS)=6×10-18)
(3)某原電池裝置如右圖,電池總反應為AsO43-+2I-+H2O![]() AsO33-+I2+2OH-當P池中溶液由無色變成藍色時,正極上的電極反應式為_______________。當電流計指針歸中后向Q池中加入一定量的NaOH,則電子由_____(填“P”或“Q”)池流出。
AsO33-+I2+2OH-當P池中溶液由無色變成藍色時,正極上的電極反應式為_______________。當電流計指針歸中后向Q池中加入一定量的NaOH,則電子由_____(填“P”或“Q”)池流出。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用含銅、鐵的粗鋅制備硫酸鋅及相關物質。工藝流程圖及有關數據如下:

物質 | Cu(OH)2 | Zn(OH)2 | Fe(OH)3 | ZnS | CuS |
Ksp | 5.0×10-20 | 2.0×10-16 | 4.0×10-38 | 1.2×10-23 | 8.5×10-45 |
請回答下列問題:
(1)粗鋅中的銅與混酸的稀溶液反應的化學方程式為__________________________,圖中處理氣體X要能夠體現綠色化學思想,還需補充氣體______(填化學式)。
(2)若溶液I中c(Cu2+)為0.05mol·L-1,則溶液II中c(Fe3+)>____mol·L-1。
(3)若固體A是Zn,取9.61 g固體C溶解于足量的500mL 2 mol·L-1稀硝酸中,共收集到標準狀況下2.24L的氣體,向所得溶液中加入2 mol·L-1NaOH溶液,則當生成沉淀最多時,沉淀的質量為_____g;若固體A是另一種物質,取部分固體C于試管中,加入鹽酸產生有臭雞蛋味氣體,則該反應的離子方程式為________________________。
(4)溶液Ⅲ經過蒸發濃縮、____________、過濾、洗滌、干燥,即得到較純凈的硫酸鋅晶體;溶液還可以制備ZnS,實際選擇的是(NH4)2S溶液而不是Na2S溶液作為反應物,理由是后者制得的ZnS含有較多的雜質,則該雜質是____________(填化學式)。
(5)金屬鋅常用作酸性干電池的負極,干電池不使用時,由于負極與電解質溶液接觸而發生自放電反應:2NH4++Zn=2NH3+H2↑+Zn2+,造成電量自動減少。寫出鉛蓄電池不使用時,其正極上發生自放電的化學方程式__________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com