
 草酸晶體的組成可用H2C2O4•xH2O表示,為了測定x值,進行如下實驗:稱取Wg草酸晶體,配成100mL水溶液.量取25.00mL所配制的草酸溶液置于錐形瓶內,加入適量稀H2SO4后,用濃度為amol•L-1的KMnO4溶液滴定,所發生的反應:KMnO4+H2C2O4+H2SO4=K2SO4+CO2↑+MnSO4+H2O
草酸晶體的組成可用H2C2O4•xH2O表示,為了測定x值,進行如下實驗:稱取Wg草酸晶體,配成100mL水溶液.量取25.00mL所配制的草酸溶液置于錐形瓶內,加入適量稀H2SO4后,用濃度為amol•L-1的KMnO4溶液滴定,所發生的反應:KMnO4+H2C2O4+H2SO4=K2SO4+CO2↑+MnSO4+H2O分析 (1)KMnO4溶液具有強氧化性,能夠腐蝕橡皮管,不能裝在酸堿式滴定管中,只能用酸式滴定管;
(2)KMnO4溶液本身是紫色,草酸反應完畢,滴入最后一滴KMnO4溶液,紫色不褪去,說明滴定到終點;
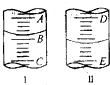
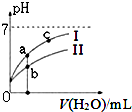
(3)圖I表示100mL量筒中液面的位置,A與B,B與C刻度間相差10mL,如果刻度A為30,則B的刻度為20,所以量筒中液體的體積讀數為22mL,在滴定管的下端有一段沒有刻度,且0刻度在上面,所以液面處的讀數是a時,滴定管中液體的體積大于(25-a)mL;
(4)根據化學方程式中各物質的關系進行計算出草酸的濃度,并根據Wg草酸晶體中草酸與結晶水的質量比可計算出x的值.
解答 解:(1)KMnO4溶液具有強氧化性,能夠腐蝕橡皮管,不能裝在酸堿式滴定管中,只能用酸式滴定管,
故答案為:酸;
(2)KMnO4溶液本身是紫色,所以在滴定草酸時不需要用指示劑,確定反應達到滴定終點時的現象是:滴入最后一滴KMnO4溶液,溶液由無色變紅色(紫紅色),且半分鐘不褪色,
故答案為:不需要;滴入最后一滴KMnO4溶液,溶液由無色變紅色(紫紅色),且半分鐘不褪色;
(3)圖I表示100mL量筒中液面的位置,A與B,B與C刻度間相差10mL,如果刻度A為30,則B的刻度為20.0mL,所以量筒中液體的體積讀數為22.0mL,在滴定管的下端有一段沒有刻度,且0刻度在上面,所以液面處的讀數是a時,滴定管中液體的體積大于(25-a)mL,故選D,
故答案為:22.0; D;
(4)2KMnO4~5H2C2O4
2 5
aV×10-3mol 0.025×cmol
c=$\frac{5aV×10{\;}^{-3}mol}{2×0.025mol}$=0.1aVmol•L-1,
樣品中含有草酸的質量為:90g/mol×0.1aVmol/L×0.025L×4=0.9aVg,Wg草酸晶體中含有結晶水的質量為:Wg-0.9aVg,
草酸晶體中含有結晶水數目為:x=$\frac{\frac{Wg-0.9aVg}{18g/mol}}{\frac{0.9aVg}{90g/mol}}$=$\frac{50W}{9aV}$-5,
故答案為:0.1aV;$\frac{50W}{9aV}$-5.
點評 本題考查一定物質的量濃度溶液配制、滴定操作中儀器的選用及計算等,題目難度中等,注意掌握配制一定物質的量濃度的溶液即中和滴定操作的方法,能夠根據實驗原理進行計算.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
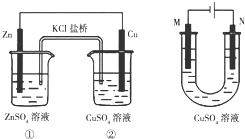
| A. | 裝置①將電能轉變為化學能 | |
| B. | 裝置①中鹽橋內的Cl-移向ZnSO4溶液 | |
| C. | 若裝置②用于鐵棒鍍銅,則N極為鐵棒 | |
| D. | 若裝置②用于電解精煉銅,則溶液中的Cu2+濃度保持不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
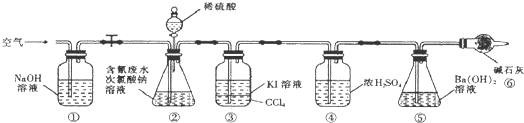
 “8.12”天津港爆炸中有一定量的氰化物泄露.氰化物多數易溶于水,有劇毒,易造成水污染.為了增加對氰化物的了解,同學們查找資料進行學習和探究.
“8.12”天津港爆炸中有一定量的氰化物泄露.氰化物多數易溶于水,有劇毒,易造成水污染.為了增加對氰化物的了解,同學們查找資料進行學習和探究.| 弱酸 | HCOOH | HCN | H2CO3 |
| 電離平衡常數( 25℃) | Ka=1.77×10-4 | Ka=5.0×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 他們的組成元素是相同的 | |
| B. | 耐腐蝕的性能不同 | |
| C. | 它們都屬于鋼,因此物理性質相同 | |
| D. | 構成普通鋼和不銹鋼的主要元素都是鐵,因此它們的化學性質相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
 .
.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com