
| A. | 鐵粉跟稀硫酸反應Fe+2H+=Fe2++H2↑ | |
| B. | 氧化鋁和稀硫酸反應 O2-+2H+=H2O | |
| C. | 氫氧化鋇溶液跟稀硫酸反應 Ba2++SO42-=BaSO4↓ | |
| D. | 銅與硝酸銀溶液反應:Cu+Ag+═Ag+Cu2+ |
分析 A.Fe和稀硫酸反應生成可溶性的硫酸亞鐵和氫氣;
B.氧化鋁是氧化物,要寫化學式;
C.漏寫氫離子和氫氧根離子生成水的離子反應方程式;
D.電荷不守恒、轉移電子不守恒.
解答 解:A.Fe和稀硫酸反應生成可溶性的硫酸亞鐵和氫氣,離子方程式為Fe+2H+=Fe2++H2↑,故A正確;
B.氧化鋁是氧化物,要寫化學式,離子方程式為Al2O3+6H+=3H2O+2Al 3+,故B錯誤;
C.漏寫氫離子和氫氧根離子生成水的離子反應方程式,離子方程式為2H++2OH-+SO42-+Ba2+=BaSO4↓+2H2O,故C錯誤;
D.電荷不守恒、轉移電子不守恒,離子方程式為Cu+2Ag+═2Ag+Cu2+,故D錯誤;
故選A.
點評 本題考查離子方程式書寫,為高頻考點,側重考查學生離子方程式書寫方法的掌握和靈活運用,要遵循客觀事實、原子守恒、電荷守恒、轉移電子守恒,知道哪些物質寫離子哪些寫化學式,易錯選項是C,題目難度不大.


科目:高中化學 來源: 題型:解答題
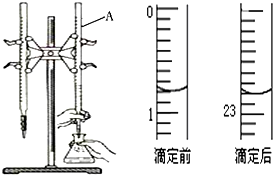 圖是用0.1000mol/L的鹽酸滴定某未知濃度的NaOH溶液的示意圖和某次滴定前、后的盛放鹽酸滴定管中液面的位置.請回答:
圖是用0.1000mol/L的鹽酸滴定某未知濃度的NaOH溶液的示意圖和某次滴定前、后的盛放鹽酸滴定管中液面的位置.請回答:| 實驗 編號 | 待測NaOH溶液的體積(mL) | 滴定前鹽酸的 體積讀數(mL) | 滴定后鹽酸的 體積讀數(mL) |
| 1 | 20.00 | 1.20 | 23.22 |
| 2 | 20.00 | 2.21 | 24.21 |
| 3 | 20.00 | 1.50 | 23.48 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 節日期間,在任意場所燃放煙花爆竹 | |
| B. | 實驗時,將水倒入濃硫酸配置稀硫酸 | |
| C. | 煤礦礦井,必須通風,嚴禁煙火 | |
| D. | 用點燃的火柴在液化氣鋼瓶口檢驗是否漏氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 28g乙烯與丙烯的混合氣體中含有雙鍵數目為NA | |
| B. | 標準狀況下,22.4L甘油中含有羥基的數目為3NA | |
| C. | 1L0.1mol•L-1NaHS溶液中,HS-與S2-數目之和為0.1 NA | |
| D. | 0.2molCl2與0.1molCH4充分反應,生成HCl分子數為0.2 NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 清晨,在茂密的樹林,常常可以看到從枝葉間透過的一道道光柱 | |
| B. | 一支鋼筆使用兩種不同牌號的藍黑墨水,易出現堵塞 | |
| C. | 在飽和FeCl3溶液中逐滴加入NaOH溶液,產生紅褐色沉淀 | |
| D. | 在河水與海水交界處有三角洲形成 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.8L0.1mol•L-1的KCl溶液 | B. | 0.2L0.2mol•L-1的HCl溶液 | ||
| C. | 0.3L0.2mol•L-1的MgCl2溶液 | D. | 0.5L 0.1mol•L-1的AlCl3溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com