
【題目】某同學在實驗室用如圖所示的裝置來制取乙酸乙酯。請回答下列問題:
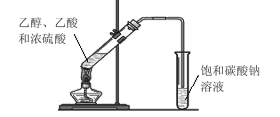
①試管中加入乙醇、乙酸和濃硫酸的順序是_______;
②濃硫酸的作用是_________;
③飽和碳酸鈉溶液的主要作用____;
④裝置中通蒸氣的導管只能插到飽和碳酸鈉溶液的液面處,不能插入溶液中,目的____,長導管的作用是________。
⑤若要把制得的乙酸乙酯分離出來,應采用的實驗操作是_________。
⑥進行該實驗時,最好向試管甲中加入幾塊碎瓷片,其目的是______。
⑦生成乙酸乙酯的反應是可逆反應,反應物不能完全轉化為生成物,反應一段時間后,就達到了該反應的限度,即達到化學平衡狀態。下列描述不能說明該反應已達到化學平衡狀態的是(填序號)______。
A 單位時間里,生成1mol乙酸乙酯,同時生成1mol水
B 單位時間里,生成1mol乙酸乙酯,同時生成1mol乙酸
C 單位時間里,消耗1mol乙醇,同時消耗1mol乙酸
D 正反應的速率與逆反應的速率相等
E 混合物中各物質的濃度不再變化
【答案】先加乙醇,再緩慢加入濃硫酸,最后加入乙酸 催化劑、吸水劑 吸收揮發出來的乙酸和乙醇,降低乙酸乙酯溶解度 防止倒吸; 導氣、將反應生成的乙酸乙酯蒸氣冷凝 分液 防止暴沸 BDE
【解析】
乙酸和乙醇在濃硫酸的催化作用下發生酯化反應,生成乙酸乙酯和水,方程式為:CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O,實驗室里用飽和碳酸鈉溶液冷卻乙酸乙酯的原因:一是利用碳酸鈉溶液中的水溶解乙醇(乙醇在水里的溶解度大于乙酸乙酯),二是碳酸鈉能跟乙酸反應吸收乙酸,便于聞到乙酸乙酯的香味,而乙酸乙酯難溶于飽和碳酸鈉溶液,這樣就可以獲得較為純凈的乙酸乙酯液體,混合乙醇和濃硫酸的方法是先加入一定量的乙醇,然后邊振蕩邊加入濃硫酸,濃硫酸的密度大于乙醇,防止酸液飛濺,乙酸和乙醇易溶于水,導管口在飽和碳酸鈉溶液液面上,而不插入液面下是為了防止倒吸。
CH3COOCH2CH3+H2O,實驗室里用飽和碳酸鈉溶液冷卻乙酸乙酯的原因:一是利用碳酸鈉溶液中的水溶解乙醇(乙醇在水里的溶解度大于乙酸乙酯),二是碳酸鈉能跟乙酸反應吸收乙酸,便于聞到乙酸乙酯的香味,而乙酸乙酯難溶于飽和碳酸鈉溶液,這樣就可以獲得較為純凈的乙酸乙酯液體,混合乙醇和濃硫酸的方法是先加入一定量的乙醇,然后邊振蕩邊加入濃硫酸,濃硫酸的密度大于乙醇,防止酸液飛濺,乙酸和乙醇易溶于水,導管口在飽和碳酸鈉溶液液面上,而不插入液面下是為了防止倒吸。
①濃硫酸稀釋時放熱,應將密度大的濃硫酸倒入乙醇中。試管中加入乙醇、乙酸和濃硫酸的順序是:先加乙醇,再緩慢加入濃硫酸,最后加入乙酸;
②濃硫酸在反應中起到催化劑的作用,為利于反應向正反應方向移動,濃硫酸起到吸水作用,故為:催化劑、吸水劑;
③實驗室里用飽和碳酸鈉溶液冷卻乙酸乙酯的原因:一是利用碳酸鈉溶液中的水溶解乙醇(乙醇在水里的溶解度大于乙酸乙酯),二是碳酸鈉能跟乙酸反應吸收乙酸,便于聞到乙酸乙酯的香味,而乙酸乙酯難溶于飽和碳酸鈉溶液,這樣就可以獲得較為純凈的乙酸乙酯液體,故答案為:吸收揮發出來的乙酸和乙醇,降低乙酸乙酯溶解度;
④乙酸和乙醇易溶于水,導管口在飽和碳酸鈉溶液液面上,而不插入液面下是為了防止倒吸,用長導管可與空氣發生充分的熱交換,利于蒸汽的冷卻,故答案為:防止倒吸;導氣、將反應生成的乙酸乙酯蒸氣冷凝;
⑤乙酸乙酯為難溶于飽和碳酸鈉的液體,可用分液的方法分離,故答案為:分液;
⑥碎瓷片起到防止暴沸的作用,故答案為:防止暴沸;
⑦A.化學反應速率之比等于化學計量數之比,無論是否達到平衡狀態,都存在單位時間里,生成1mol乙酸乙酯,同時生成1mol水,故A錯誤;
B.單位時間里,生成1mol乙酸乙酯,同時生成1mol乙酸,說明正逆反應速率相等,達到平衡狀態,故B正確;
C.化學反應速率之比等于化學計量數之比,無論是否達到平衡狀態,都存在單位時間里,消耗1mol乙醇,同時消耗1mol乙酸,故C錯誤;
D.正反應的速率與逆反應的速率相等,說明達到平衡狀態,故D正確;
E.混合物中各物質的濃度不再變化,說明達到平衡狀態,故E正確。
故選BDE。


 津橋教育計算小狀元系列答案
津橋教育計算小狀元系列答案科目:高中化學 來源: 題型:
【題目】ClO2是一種消毒殺菌效率高、二次污染小的水處理劑,實驗室可通過以下反應制得:2KClO3+H2C2O4+H2SO4===2ClO2↑+2CO2↑+K2SO4+2H2O。下列有關該反應的說法正確的是( )
A. KClO3在反應中失去電子B. ClO2是還原產物
C. H2C2O4在反應中被還原D. 1 mol H2C2O4參加反應有4 mol電子轉移
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知氨可以與灼熱的氧化銅反應得到氮氣和金屬銅,用示意圖中的裝置可以實現該反應。
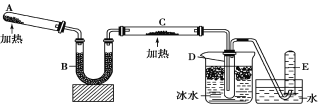
(1)A中裝有Ca(OH)2和NH4Cl混合粉末,該反應的化學方程式是______。
(2)B的作用是______。
(3)C中發生反應的化學方程式是:___,并在方程式中用單線橋標出電子轉移的方向和數目___。
(4)D中收集到的物質是___,檢驗該物質的方法和現象是___;E中收集到的氣體是_____(填化學式)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學生對Na2SO3與AgNO3在不同pH下的反應進行探究。
(1)測得Na2SO3溶液pH=11,AgNO3溶液pH=5,二者水解的離子分別是 。
(2)調節pH,實驗記錄如下:
實驗 | pH | 現象 |
A | 10 | 產生白色沉淀,稍后溶解,溶液澄清 |
B | 6 | 產生白色沉淀,一段時間后,沉淀未溶解 |
C | 2 | 產生大量白色沉淀,一段時間后,產生海綿狀棕黑色物質X |
查閱資料得知:
Ⅰ.Ag2SO3:白色,難溶于水,溶于過量Na2SO3的溶液
Ⅱ.Ag2O:棕黑色,不溶于水,能和酸反應
①推測a中白色沉淀為Ag2SO3,離子方程式是 。
②推測a中白色沉淀為Ag2SO4,推測的依據是 。
(3)取b、c中白色沉淀,置于Na2SO3溶液中,沉淀溶解。該同學設計實驗確認了白色沉淀不是Ag2SO4,實驗方法是:另取Ag2SO4固體置于 溶液中,未溶解。
(4)將c中X濾出、洗凈,為確認其組成,實驗如下:
Ⅰ.向X中滴加稀鹽酸,無明顯變化
Ⅱ.向X中加入過量濃HNO3,產生紅棕色氣體
Ⅲ.用Ba(NO3)2溶液、BaCl2溶液檢驗Ⅱ中反應后的溶液,前者無變化,后者產生白色沉淀
①實驗Ⅰ的目的是 。
②根據實驗現象,分析X的性質和元素組成是 。
③Ⅱ中反應的化學方程式是 。
(5)該同學綜合以上實驗,分析產生X的原因,認為隨著酸性的增強,還原性增強。通過進一步實驗確認了這種可能性,實驗如圖所示:
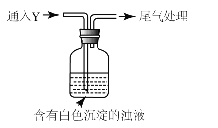
①氣體Y是 。
②白色沉淀轉化為X的化學方程式是 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物丙可由如下反應得到
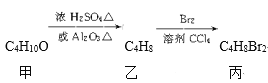
丙的結構簡式不可能是( )
A. CH3CH(CH2Br)2B. (CH3)2CBrCH2Br
C. C2H5CHBrCH2BrD. CH3(CHBr)2CH3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】具有解熱鎮痛及抗生素作用的藥物“芬必得”主要成分的結構簡式如圖,它屬于( )

①芳香族化合物 ②脂肪族化合物 ③有機羧酸 ④有機高分子化合物 ⑤芳香烴
A. ③⑤ B. ②③ C. ①③ D. ①④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將15mL 1.0mol/L的CH3COOH(Ka=1.8×10-5)加入到5mL 2.0mol/L的NaOH溶液中,并將混合溶液稀釋至100mL,則制得的溶液pH值約為
A. 4.4B. 4.8
C. 5.0D. 5.4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據合成氨反應的能量變化示意圖,下列有關說法正確的是( )
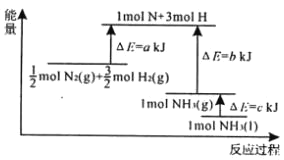
A.斷裂0.5molN2(g)和1.5mol H2(g)中所有的化學鍵釋放a kJ熱量
B.NH3(g)═NH3(l)△H=c kJmol﹣1
C.N2(g)+3H2(g)2NH3(g)△H=﹣2(a﹣b)kJmol﹣1
D.2NH3(l)N2(g)+3H2(g)△H=2(b+c﹣a) kJmol﹣1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】200℃時,11.6g CO2和水蒸氣的混合氣體與過量的Na2O2充分反應后,固體質量增加了3.6g,再將反應后剩余固體冷卻后加入含有Na+、HCO3-、SO32-、CO32-等離子的水溶液中,若溶液體積保持不變,則下列說法中正確的是
A.原混合氣體的平均摩爾質量為23.2g/mol
B.混合氣體與Na2O2反應過程中電子轉移的物質的量為0.25mol
C.溶液中SO32-的物質的量濃度基本保持不變
D.溶液中HCO3-的物質的量濃度減小,CO32-的物質的量濃度增大,但是HCO3-和CO32-的物質的量濃度之和基本保持不變
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com