
【題目】發展新能源汽車是國家戰略,經過近10年的發展,目前我國新能源汽車產銷量均達到80萬輛,LiFePO4電池是新能源汽車關鍵部件之一,其工作原理如圖所示。下列說法錯誤的是( )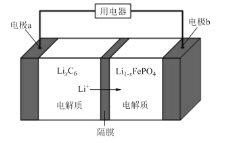
A. 充電時,電極a與電源的負極連接,電極b與電源正極連接
B. 電池驅動汽車前進時,正極的電極反應為:Li1-xFePO4+x Li++x e-= LiFePO4
C. 電池驅動汽車后退時,負極材料減重1.4g ,轉移0.4mol電子
D. 電池進水將會大大降低其使用壽命
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】在體積為2 L的恒容密閉容器中發生反應xA(g)+yB(g) ![]() zC(g),圖I表示200℃時容器中A、B、C物質的量隨時間的變化,圖Ⅱ表示不同溫度下平衡時C的體積分數隨起始n(A):n(B)的變化關系。則下列結論正確的是
zC(g),圖I表示200℃時容器中A、B、C物質的量隨時間的變化,圖Ⅱ表示不同溫度下平衡時C的體積分數隨起始n(A):n(B)的變化關系。則下列結論正確的是

A. 若在圖Ⅰ所示的平衡狀態下,再向體系中充入He,重新達到平衡前υ(正)>υ(逆)
B. 200℃時,反應從開始到剛好達平衡的平均速率υ(B)=0.02 mol·L﹣1·min﹣1
C. 圖Ⅱ所知反應xA(g)+yB(g) ![]() zC(g)的△H<0
zC(g)的△H<0
D. 200℃時,向容器中充入2 mol A和1 mol B,達到平衡時,A的體積分數大于0.5
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列不能用勒夏特列原理解釋的事實是( )
A.棕紅色的NO2加壓后顏色先變深后變淺
B.氫氣、碘蒸氣、碘化氫氣體組成的平衡體系加壓后顏色變深
C.黃綠色的氯水光照后顏色變淺
D.合成氨工業使用高壓以提高氨的產量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鐵在自然界中的含量豐富,而且在生活生產中應用廣泛。
(1)鐵在周期表中的位置為______。
(2)硝普試劑[Fe(NO)CN)5]2-可用于檢驗S2-,兩者反應得紫色溶液,其中兩個配體互為等電子體,已知硝普試劑[Fe(NO)(CN)5]2-中Fe為+2價,其基態離子的外圍電子排布式為_______。
(3)K4[Fe(CN)6]溶液可用于檢驗Fe3+,K、C、N的第一電離能由大到小的順序為______,K4[Fe(CN)6]內界中σ鍵與π鍵的個數比為______。
(4)二茂鐵是由兩個環戊二烯陰離子與Fe2+離子組成的三明治型化合物,即![]() 。環戊二烯分子(
。環戊二烯分子(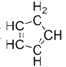 )中碳原子的雜化方式為_______。
)中碳原子的雜化方式為_______。
(5)工業電解熔融的FeO、Fe2O3冶煉高純鐵。FeO與Fe2O3相比,_____熔點高,其主要原因是_______。
(6)鐵單質晶體在不同溫度下有兩種主要的堆積方式——體心立方(A)與面心立方(B),假定Fe原子半徑不變,在兩種堆積中,配位數之比NA︰NB為_______晶體密度之比ρA︰ρB為_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖①、②、③、④、⑤五組儀器(可重復使用),選擇合適的裝置和藥品能完成的實驗是( )
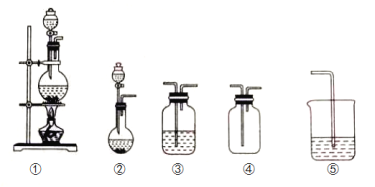
選項 | 實驗目的 | 實驗裝置 | 實驗藥品 |
A | 制備并收集HCl氣體 | ①③④ | 濃鹽酸、濃硫酸、水 |
B | 比較氯氣和溴的氧化性強弱 | ①③③⑤ | MnO2、濃鹽酸、飽和食鹽水、溴化鉀溶液、氫氧化鈉溶液 |
C | 探究乙烯的加成反應 | ①③ | 無水乙醇、濃硫酸、溴的四氯化碳溶液 |
D | 探究二氧化硫的還原性 | ②③③ | 亞硫酸鈉、30%的硝酸、溴水、氫氧化鈉溶液 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】近期發現,H2S是繼NO、CO之后第三個生命體系氣體信號分子,它具有參與調節神經信號傳遞、舒張血管減輕高血壓的功能。回答下列問題:
(1)下圖是通過熱化學循環在較低溫度下由水或硫化氫分解制備氫氣的反應系統原理。

通過計算,可知系統(Ⅰ)和系統(Ⅱ)制氫的熱化學方程式分別為________________、______________,制得等量H2所需能量較少的是_____________(填“系統(Ⅰ)”或“系統(Ⅱ)”)。
(2)羰基硫(COS)可作為一種糧食熏蒸劑,能防止某些昆蟲、線蟲和真菌的危害。H2S與CO2在高溫下發生反應:H2S(g)+CO2(g)![]() COS(g) +H2O(g)。在610 K時,將1 mol CO2與1 mol H2S充入2 L的空鋼瓶中,反應平衡后水的物質的量分數為0.02。
COS(g) +H2O(g)。在610 K時,將1 mol CO2與1 mol H2S充入2 L的空鋼瓶中,反應平衡后水的物質的量分數為0.02。
①H2S的平衡轉化率![]() =_______%,反應平衡常數K=________。
=_______%,反應平衡常數K=________。
②在620 K重復試驗,平衡后水的物質的量分數為0.03,H2S的轉化率![]() _____
_____![]() ,該反應的
,該反應的![]() H_____0。(填“>”、“<”或“=”)
H_____0。(填“>”、“<”或“=”)
③向反應器中再分別充入下列氣體,能使H2S轉化率增大的是________(填標號)
A.N2 B.H2S C.COS D.CO2
(3)25℃,在0.10 mol·L-1 H2S溶液中,通入HCl氣體或加入NaOH固體以調節溶液pH,溶液pH與c(S2-) 關系如下圖(忽略溶液體積的變化、H2S的揮發)。

①硫化氫的電離方程式為__________________________。
②向硫化氫溶液中加入CuSO4溶液時,硫化氫的電離平衡向______(“左”或“右”)移動,c(S2-)_____________(填“增大”、“不變”或“減小”)。
③當調節溶液pH=13時,溶液中的c( H2S ) + c( HS-)=_____mol·L-1。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學設計如下實驗方案,以分離KCl和BaCl2兩種固體混合物,試回答下列問題:

供選試劑:Na2SO4溶液、K2SO4溶液、K2CO3溶液、鹽酸
(1)操作①的名稱是___,操作②的名稱是___。
(2)試劑a是___,固體B是___。(填化學式)
(3)生成沉淀A的離子反應方程式為:__加入試劑b所發生的化學反應方程式為:___。
(4)該方案能否達到實驗目的:___。若不能,應如何改進(若能,此問不用回答)___。
(5)若要測定原混合物中KCl和BaCl2的質量分數,除了要準確稱量混合物的質量外,至少還要獲得的數據是____的質量。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】改變0.1molL—1二元弱酸H2A溶液的pH,溶液中的H2A、HA—、A2—的物質的量分數δ(x)隨pH的變化如圖所示[已知δ(x)=c(x)/(c(H2A)+c(HA—)+c(A2—)])。下列敘述正確的是

A. Ka2(H2A)的數量級為10-4
B. NaHA溶液中,HA-的水解能力小于HA-的電離能力
C. 在含H2A、HA-和A2-的溶液中,加入少量NaOH固體,δ(HA-)一定增大
D. 將等物質的量的NaHA和Na2A混合物溶于水,所得的溶液中δ(HA-)=δ(A2-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度T1時,Ag2SO4在水中的沉淀溶解曲線如圖實線所示。下列說法正確的是( )

A. T1時,Ag2SO4的溶度積常數(Ksp)為1×10-3
B. T1時,0.02 mol/L的AgNO3溶液與0.2 mol/L的Na2SO4溶液等體積混合不會生成沉淀
C. b點表示T1時Ag2SO4的飽和溶液,稀釋時可以使溶液由b點變到a點
D. 僅通過降溫的方法,可以使T2時的飽和溶液從c點變到T1時b點
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com