
| A. | 3:2 | B. | 2:5 | C. | 3:4 | D. | 4:3 |
分析 將鹽酸滴入碳酸鈉溶液中,發生反應:Na2CO3+HCl═NaHCO3+NaCl,NaHCO3+HCl═NaCl+CO2↑+H2O,將碳酸鈉溶液滴入鹽酸中,發生反應:Na2CO3+2HCl═2NaCl+CO2↑+H2O,生成的氣體體積不同,鹽酸不足,設碳酸鈉溶液物質的量濃度為c1,鹽酸的物質的量濃度為c2,依據方程式進行計算.
解答 解:將鹽酸滴入碳酸鈉溶液中,發生反應:Na2CO3+HCl═NaHCO3+NaCl,NaHCO3+HCl═NaCl+CO2↑+H2O,將碳酸鈉溶液滴入鹽酸中,發生反應:Na2CO3+2HCl═2NaCl+CO2↑+H2O,生成的氣體體積不同,鹽酸不足,設碳酸鈉溶液物質的量濃度為c1,鹽酸的物質的量濃度為c2,
鹽酸滴到碳酸鈉中發生兩步反應,鹽酸對第一步反應過量,對第二步反應不足:
Na2CO3+HCl═NaHCO3+NaCl,NaHCO3+HCl═NaCl+CO2↑+H2O,
c1 c2 c1 (c2-c1 ) (c2-c1 )
生成二氧化碳的物質的量(c2-c1);
碳酸鈉滴到鹽酸中,依據鹽酸的量計算生成二氧化碳的體積:
Na2CO3+2HCl═2NaCl+CO2↑+H2O
c2 0.5c2
生成二氧化碳物質的量0.5c2,依據題意:(c2-c1):0.5c2=1:2,則c1:c2=3:4;
故選:C.
點評 本題考查了有關物質的量計算,明確碳酸鈉與鹽酸性質及發生反應實質是解題關鍵,題目難度中等.


 每日10分鐘口算心算速算天天練系列答案
每日10分鐘口算心算速算天天練系列答案科目:高中化學 來源: 題型:解答題
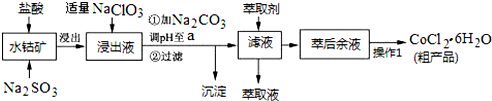
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 開始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
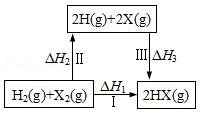
| A. | H2(g)+X2(g)═2H(g)+2X(g)△H2>0 | |
| B. | 生成HX的反應熱與途徑有關,所以△H1≠△H2+△H3 | |
| C. | 若X分別表示Cl,Br,I,則過程Ⅱ吸收的熱量依次增多 | |
| D. | △H1代表H2的燃燒熱 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
| 應量取的濃鹽酸的體積/mL | 應選用的容量瓶的規格/mL | 除容量瓶外需要的其他儀器 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
| 實際應稱Na2CO3質量/g | 應選用容量瓶的規格/mL |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Ba2+、Cl-、NO3-、K+ | B. | HCO3-、K+、SO42-、Cl- | ||
| C. | Fe2+、Cl-、Na+、NO3- | D. | Na+、Cl-、K+、SO42-、 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
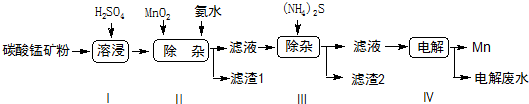
| 物質 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
| Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com