
已知A經如右圖所示的過程轉化為D, 
請回答下列問題:
(1)若A為非金屬單質,且常溫下為淡黃色固體,B為刺激性氣味的無色氣體,能使品紅溶液褪色,D為強酸。
①D的化學式是 。
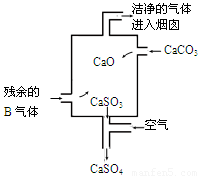
②在工業生產中B氣體的大量排放被雨水吸收后形成了 而污染了環境。某工廠凈化殘余的B氣體裝置如圖,則除去B氣體的總反應方程式是 。
(2)若A是能使酚酞試液變紅的氣體。D是一種強酸。寫出A→B的化學方程式 ;工業生產上,以34噸A為原料,最多可以生產63%的D酸 噸。
(1)①H2SO4 (2分) ②酸雨(1分);2SO2 +2CaCO3+O2 = 2CaSO4+2CO2(2分)
(2) 4NH3 +5O2
 4NO+6H2O
(2分);200(2分)
4NO+6H2O
(2分);200(2分)
【解析】
試題分析:(1)若A為非金屬單質,且常溫下為淡黃色固體,則A是單質S。硫在氧氣中燃燒生成SO2,SO2是刺激性氣味的無色氣體,則B是SO2,SO2能使品紅溶液褪色。SO2氧化得到三氧化硫,三氧化硫溶于水生成硫酸,即D為強酸硫酸。
①D的化學式是H2SO4。
②在工業生產中SO2氣體的大量排放被雨水吸收后形成了酸雨而污染了環境。根據示意圖可知,碳酸鈣高溫分解生成氧化鈣和CO2,氧化鈣吸收SO2生成亞硫酸鈣。亞硫酸鈣不穩定,被空氣中的氧氣氧化生成硫酸鈣,從而防止空氣污染,因此反應的總化學方程式為2SO2 +2CaCO3+O2=2CaSO4+2CO2。
(2)若A是能使酚酞試液變紅的氣體,則A是氨氣。氨氣在氧氣中發生催化氧化生成NO和水。NO被氧氣氧化生成NO2,NO2溶于水生成強酸硝酸,因此A→B的化學方程式為4NH3 +5O2
 4NO+6H2O。根據氮原子守恒可知:
4NO+6H2O。根據氮原子守恒可知:
NH3~~~~HNO3
17t 63t
34t m×63%
解得m=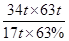 =200t
=200t
考點:考查無機框圖題的判斷、化學用語的書寫以及硝酸制備的有關計算等


 小學課時特訓系列答案
小學課時特訓系列答案科目:高中化學 來源:2013屆江西省南昌二中高三第一次考試化學試卷(帶解析) 題型:填空題
(8分)含氯消毒劑和過氧化物等強氧化性消毒劑可防甲型H1N1流感。
(1)過碳酸鈉是一種有多種用途的新型氧系固態漂白劑,化學式可表示為Na2CO3·3H2O2,它具有Na2CO3和H2O2的雙重性質。
①H2O2有時可作為礦業廢液消毒劑,如消除采礦業廢液中的氰化物(如NaCN),經以下反應實現:NaCN+H2O2+H2O===A+NH3↑,則生成物A的化學式為_______________,
②某強酸性反應體系中,反應物和生成物共六種物質:O2、MnO、H2O、Mn2+、H2O2、H+。已知該反應中H2O2只發生了如下過程:H2O2→ O2。寫出該反應的離子方程式:_________。
(2)某天然堿的化學式可表示為:aNa2CO3·bNaHCO3·2H2O,取m g天然堿溶于水配成溶液,再向溶液中逐滴加入1 mol/L的鹽酸,標準狀況下產生的CO2的體積與所加鹽酸體積之間的關系某同學作出了如右圖所示的A和B曲線,試回答下列問題:
①_______曲線正確,天然堿的化學式為___________,
③加鹽酸后產生CO2氣體體積(標準狀況)的最大值為_________________mL。
(3)漂白劑亞氯酸鈉(NaClO2)在常溫與黑暗處可保存一年。
亞氯酸不穩定可分解,反應的離子方程式為:HClO2―→ClO2↑+H++Cl-+H2O(未配平)。在該反應中,當有1 mol ClO2生成時轉移的電子個數是________。
查看答案和解析>>
科目:高中化學 來源:2013屆江西省江西師大附中、臨川一中高三12月聯考化學試卷(帶解析) 題型:填空題
(7分)化合物A是尿路結石的主要成分,屬于結晶水合物,可用X·nH2O表示。在一定條件下有如下圖所示的轉化關系: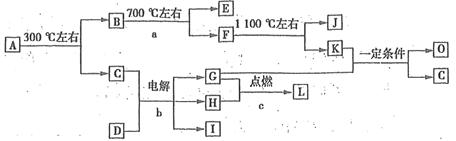
已知:①上圖中的各字母代表的物質均由常見元素(原子序數≤20)組成,其中X由三種元素組成;A、D晶體中陰、陽離子個數比都是l:1;D中的陽離子與C分子有相同的電子數,A中的陽離子與D中的陰離子的電子層結構相同。
②G、H是常見的氣體單質,E、K、L是常見的氣體化合物;E被人體吸入,會與血紅蛋白結合而使人中毒,K的大量排放是造成地球溫室效應的主要原因。
③反應b、c是重要的化工反應,I是一種重要的化工原料。
④轉化關系圖中的部分變化經定量測定,得到如右圖所示的固體產物的質量分數[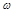 (%)]隨溫度[T(℃)]的變化曲線。
(%)]隨溫度[T(℃)]的變化曲線。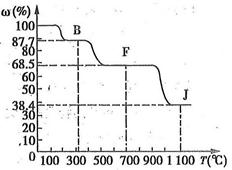
回答下列問題:
(1)寫出A的化學式: ,D陰離子的示意圖 。
(2)反應a的化學方程式為 。
(3)寫出電解反應b的化學方程式,并標出電子轉移的方向和數目: 。
(4)K與G在一定條件下可生成多種物質,既可獲得經濟效益,也可減少對環境的污染。若O是一種易揮發的液態燃料,有毒,誤飲5~10mL會導致雙目失明。則O的分子式為 。
查看答案和解析>>
科目:高中化學 來源:2012-2013學年江西省、臨川一中高三12月聯考化學試卷(解析版) 題型:填空題
(7分)化合物A是尿路結石的主要成分,屬于結晶水合物,可用X·nH2O表示。在一定條件下有如下圖所示的轉化關系:
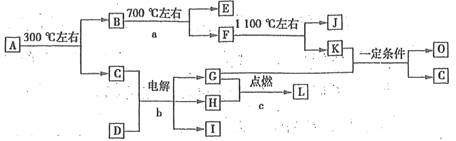
已知:①上圖中的各字母代表的物質均由常見元素(原子序數≤20)組成,其中X由三種元素組成;A、D晶體中陰、陽離子個數比都是l:1;D中的陽離子與C分子有相同的電子數,A中的陽離子與D中的陰離子的電子層結構相同。
②G、H是常見的氣體單質,E、K、L是常見的氣體化合物;E被人體吸入,會與血紅蛋白結合而使人中毒,K的大量排放是造成地球溫室效應的主要原因。
③反應b、c是重要的化工反應,I是一種重要的化工原料。
④轉化關系圖中的部分變化經定量測定,得到如右圖所示的固體產物的質量分數[ (%)]隨溫度[T(℃)]的變化曲線。
(%)]隨溫度[T(℃)]的變化曲線。

回答下列問題:
(1)寫出A的化學式: ,D陰離子的示意圖 。
(2)反應a的化學方程式為 。
(3)寫出電解反應b的化學方程式,并標出電子轉移的方向和數目: 。
(4)K與G在一定條件下可生成多種物質,既可獲得經濟效益,也可減少對環境的污染。若O是一種易揮發的液態燃料,有毒,誤飲5~10mL會導致雙目失明。則O的分子式為 。
查看答案和解析>>
科目:高中化學 來源:2012-2013學年江西省高三第一次考試化學試卷(解析版) 題型:填空題
(8分)含氯消毒劑和過氧化物等強氧化性消毒劑可防甲型H1N1流感。
(1)過碳酸鈉是一種有多種用途的新型氧系固態漂白劑,化學式可表示為Na2CO3·3H2O2,它具有Na2CO3和H2O2的雙重性質。
①H2O2有時可作為礦業廢液消毒劑,如消除采礦業廢液中的氰化物(如NaCN),經以下反應實現:NaCN+H2O2+H2O===A+NH3↑,則生成物A的化學式為_______________,
②某強酸性反應體系中,反應物和生成物共六種物質:O2、MnO、H2O、Mn2+、H2O2、H+。已知該反應中H2O2只發生了如下過程:H2O2→ O2。寫出該反應的離子方程式:_________。
(2)某天然堿的化學式可表示為:aNa2CO3·bNaHCO3·2H2O,取m g天然堿溶于水配成溶液,再向溶液中逐滴加入1 mol/L的鹽酸,標準狀況下產生的CO2的體積與所加鹽酸體積之間的關系某同學作出了如右圖所示的A和B曲線,試回答下列問題:

①_______曲線正確,天然堿的化學式為___________,
③加鹽酸后產生CO2氣體體積(標準狀況)的最大值為_________________mL。
(3)漂白劑亞氯酸鈉(NaClO2)在常溫與黑暗處可保存一年。
亞氯酸不穩定可分解,反應的離子方程式為:HClO2―→ClO2↑+H++Cl-+H2O(未配平)。在該反應中,當有1 mol ClO2生成時轉移的電子個數是________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com