
分析 (1)根據配制一定物質的量濃度溶液的步驟分析解答需要的儀器和用不到的儀器,依據配制溶液體積選擇容量瓶規格;
(2)依據m=CVM計算需要溶質的質量;
(3)配制一定物質的量濃度溶液的步驟:計算、稱量、溶解、冷卻、移液、洗滌、定容、搖勻,據此排序;
(4)分析操作對溶質的物質量和溶液體積的影響,依據C=$\frac{n}{V}$進行誤差分析.
解答 解:(1)用固體配制一定物質的量濃度基本步驟為:計算、稱量、溶解、冷卻、移液、洗滌、定容、搖勻,用到的儀器:托盤天平、藥匙、量筒、玻璃棒、燒杯、容量瓶、膠頭滴管,配制0.2mol/L的Na2CO3溶液480mL,應選擇500mL容量瓶,所以還缺少的儀器:500mL容量瓶;
故答案為:500mL容量瓶;
(2)用Na2CO3•10H2O晶體,配制0.2mol/L的Na2CO3溶液480mL,實際配制500mL溶液,需要溶質的質量為:0.2mol/L×0.5mL×286g/mol=28.6;
故答案為:28.6;
(3)配制一定物質的量濃度溶液的步驟:計算、稱量、溶解、冷卻、移液、洗滌、定容、搖勻,所以正確的順序為:⑤①④⑥③⑦②⑧;
故答案為:⑤①④⑥③⑦②⑧;
①碳酸鈉失去了部分結晶水,則稱取的溶質中含有碳酸鈉的物質的量偏大,溶液濃度偏高;
②用“左碼右物”的稱量方法稱量晶體并使用了游碼,導致稱取的溶質的質量偏小,溶質的物質的量偏小,溶液濃度偏低;
③碳酸鈉晶體不純,其中混有氯化鈉,導致稱取的溶質的物質的量偏小,溶液濃度偏低;
④稱量碳酸鈉晶體時所用砝碼生銹,導致稱取溶質的質量偏大,溶質的物質的量偏大,溶液濃度偏高;
⑤容量瓶未經干燥就使用,對溶質的物質的量和溶液體積都不產生影響,溶液濃度不變;
⑥轉移液體時不小心灑落了一滴在容量瓶的外面,導致溶質的物質的量偏小,溶液濃度偏低;
⑦定容時俯視刻度線,導致溶液體積偏小,溶液濃度偏高;
⑧搖勻后,凹液面低于刻度線未做任何處理,對溶質的物質的量和溶液體積都不會產生影響,溶液濃度不變;
所以:引起所配溶液濃度偏高的有①④⑥⑦,偏低的有②③,無影響的有⑤⑧;
故答案為:①④⑥⑦;②③;⑤⑧.
點評 本題考查了配制一定物質的量濃度的溶液的方法,注意掌握配制一定物質的量濃度的溶液的方法,該題是中等難度的試題,側重對學生能力的培養和解題方法的指導和訓練,該題的難點在于誤差分析,注意明確誤差分析的方法.


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化學 來源: 題型:選擇題
| A. | Al3+、Ba2+、Cl-、NO3- | B. | K+、Na+、HCO3-、NO3- | ||
| C. | K+、Fe2+、Cl-、NO3- | D. | Na+、K+、Cl-、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
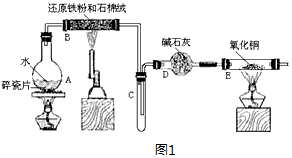

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NH4HCO3溶液與過量KOH濃溶液:NH4++OH-═NH3↑+H2O | |
| B. | 向Ba(OH)2溶液中滴加NaHSO4溶液至恰好為中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| C. | 稀硝酸和過量的鐵屑反應:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| D. | Fe(OH)3溶于氫碘酸中:Fe(OH)3+3H+═Fe3++3H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②③ | B. | ②④ | C. | ②③④ | D. | ①③ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①② | B. | ①②③ | C. | ①②③④ | D. | 全部 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 次氯酸有酸性,可用于漂白、殺菌消毒 | |
| B. | 純堿能與酸反應,可用作治療胃酸過多的藥物 | |
| C. | 液氨汽化時要吸收大量的熱,工業上可用作制冷劑 | |
| D. | 晶體硅的熔點高、硬度大,可用于制作半導體材料 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com