
【題目】運用元素周期律分析下面的推斷,其中錯誤的是![]()
A.鈹![]() 的氧化物對應的水化物可能具有兩性
的氧化物對應的水化物可能具有兩性
B.砹![]() 為有色固體,HAt不穩定,AgAt感光性很強,且不溶于水也不溶于酸
為有色固體,HAt不穩定,AgAt感光性很強,且不溶于水也不溶于酸
C.硒化氫![]() 是無色、有毒且穩定性比硫化氫還差的氣體
是無色、有毒且穩定性比硫化氫還差的氣體
D.同一主族的元素從上到下,金屬性呈周期性變化
 開心快樂假期作業暑假作業西安出版社系列答案
開心快樂假期作業暑假作業西安出版社系列答案科目:高中化學 來源: 題型:
【題目】如圖是以石墨作陽極,銅棒作陰極,電解 200mL,含有 Cu2+、Fe3+離子的酸性溶液,陰極生成固體與轉移電子的關系, 則以下說法正確的是( )
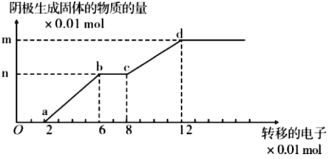
A.Oa 段、bc 段陰極均有氣體產生
B.bc 段的電極反應為:Fe3++e-=Fe2+
C.原溶液 PH 值約為 1
D.該溶液中 Cu2+,Fe3+離子的濃度之比為 1:2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述錯誤的是![]()
A.短周期中次外層電子數是最外層電子數2倍的原子一定是非金屬元素
B.鈹的最高價氧化物的水化物可能具有兩性
C.已知鍶![]() 是第 IIA元素,碳酸鍶難溶于水,但易溶于鹽酸
是第 IIA元素,碳酸鍶難溶于水,但易溶于鹽酸
D.科學家在周期表中金屬元素與非金屬元素分界線處找到了優良的半導體材料
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表中的實驗操作能達到實驗目的或能得出相應結論的是![]()
選項 | 實驗操作 | 實驗目的或結論 |
A | 向一定濃度的 |
|
B | 取少量 | 檢驗 |
C | 向某溶液中滴加 | 說明原溶液中一定含有 |
D | 將混有 | 除去 |
A.A
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在25mL0.1mol·L-1某一元堿中,逐滴加入0.1mol·L-1醋酸,滴定曲線如圖所示。則下列說法正確的是( )

A.無法判斷該堿溶液能否可以溶解Al(OH)3
B.a點對應的體積值等于25mL
C.C點時,c(CH3COO-)>c(Na+)>c(OH-) >c(H+)
D.D點時,c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】含硫各微粒![]() 、
、![]() 和
和![]() 存在于
存在于![]() 與NaOH溶液反應后的溶液中,它們的物質的量分數
與NaOH溶液反應后的溶液中,它們的物質的量分數![]() 與溶液pH的關系如下圖所示.下列說法正確的是
與溶液pH的關系如下圖所示.下列說法正確的是

A.![]() 時,溶液中
時,溶液中![]()
B.![]() 時,溶液中
時,溶液中![]()
C.為獲得盡可能純的![]() ,可將溶液的pH控制在
,可將溶液的pH控制在![]() 左右
左右
D.由圖中數據可估算出![]() 為
為![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A,B,C,D四種物質之間的轉化關系如圖所示![]() 部分產物已略去
部分產物已略去![]() ,下列說法正確的是
,下列說法正確的是![]()

A.若A為![]() 溶液,B可能為氨水,反應
溶液,B可能為氨水,反應![]() 的離子方程式為:
的離子方程式為:![]()
B.若A為Fe,B可能為稀硝酸,反應![]() 的離子方程式為:
的離子方程式為: ![]()
C.若A為NaOH溶液,B可能為![]() ,可用
,可用![]() 溶液鑒別C、D溶液
溶液鑒別C、D溶液
D.若A為![]() ,B可能為
,B可能為![]() ,實驗室可用加熱固體C的方法制取
,實驗室可用加熱固體C的方法制取![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】磷酸是三元弱酸,常溫下三級電離常數分別是:Ka1=7.1×10-3,Ka2=6.2×10-8,Ka3=4.5×10-13,解答下列問題:
(1)常溫下同濃度①Na3PO4、②Na2HPO4、③NaH2PO4的pH由小到大的順序___(填序號)。
(2)常溫下,NaH2PO4的水溶液pH___(填“>”“<”或“=”)7。
(3)常溫下,Na2HPO4的水溶液呈___(填“酸”“堿”或“中”)性,用Ka與Kh的相對大小,說明判斷理由:__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯和碘是ⅦA元素,回答下列問題:
(1)I3-中心原子的價層電子對數為_______ ,沸點ICl____Cl2(填大于,小于,等于)。
(2)已知CsICl2受熱分解,該分解的化學方程式是___________________。
(3)已知高碘酸的結構如圖1所示,1mol高碘酸中含有__________mol![]() 鍵。
鍵。
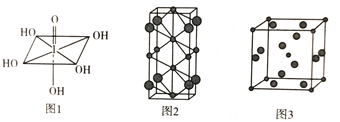
(4)Na和Cl兩種元素可以形成不同類型的晶體,如圖2和圖3(大球為氯原子,小球為鈉原子),圖2化學式為_____________;圖3中Na+的配位數為___________。
(5)若圖3晶胞的邊長為a cm,則晶體的密度![]() =____(NA表示阿伏加德羅常數的值)。
=____(NA表示阿伏加德羅常數的值)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com