
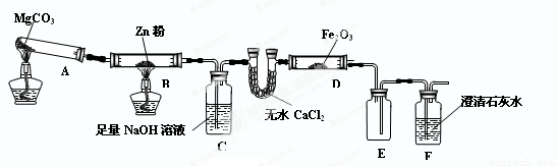
(12分)某研究小組利用下圖裝置探究溫度對CO還原Fe2O3的影響(固定裝置略)
(1) MgCO3的分解產物為 。
(2) 裝置C的作用是 ,處理尾氣的方法為 。
(3) 將研究小組分為兩組,按上圖裝置進行對比實驗,甲組用酒精燈、乙組用酒精噴燈給裝置D加熱,反應產物均為黑色粉末(純凈物),兩組分別用產物進行以下實驗。
步驟 | 操作 | 甲組現象 | 乙組現象 |
1 | 取黑色粉末加入稀鹽酸 | 溶解,無氣泡 | 溶解,有氣泡 |
2 | 取步驟1中溶液,滴加K3[Fe(CN)6]溶液 | 藍色沉淀 | 藍色沉淀 |
3 | 取步驟1中溶液,滴加KSCN溶液 | 變紅 | 無現象 |
4 | 向步驟3溶液中滴加新制氯水 | 紅色褪去 | 先變紅,后褪色 |
已知:3Fe2+ + 2[Fe(CN)6]3- = Fe3[Fe(CN)6]2↓(藍色)
① 乙組得到的黑色粉末是 ;
② 甲組步驟1中反應的離子方程式為 ;
③ 乙組步驟4中,溶液變紅的原因為 ;溶液褪色可能的原因及其驗證方法為
;
④ 從實驗安全考慮,上圖裝置還可采取的改進措施是 ;
(1) MgO、CO2(1分)
(2) 除CO2(1分)、 點燃(1分)
(3) ① Fe (1分)
② Fe3O4+8H+ = 2Fe3++Fe2++4H2O(2分)
③ Fe2+被氧化成Fe3+,Fe3+遇SCN-顯紅色;(2分)
假設SCN-被Cl2氧化,向溶液中繼續加入過量KSCN溶液,若出現紅色,則假設成立
(2分)(其它合理答案均可給分)
④ 在裝置BC之間添加裝置E防倒吸(其它合理答案均可給分) (2分)
【解析】
試題分析:
(1) 根據MgCO3的分解原理MgCO3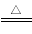 MgO+CO2↑;可得其是產物是MgO、CO2
MgO+CO2↑;可得其是產物是MgO、CO2
(2) 通過Zn粉,發生Zn+CO2 ZnO+CO;再通過NaOH溶液(裝置C),是為了除去二氧化碳;再通過無水氯化鈣是為了除去水蒸氣;然后CO還原氧化鐵,E裝置防倒吸,F裝置檢驗和吸收二氧化碳。尾氣是CO,點燃處理。
ZnO+CO;再通過NaOH溶液(裝置C),是為了除去二氧化碳;再通過無水氯化鈣是為了除去水蒸氣;然后CO還原氧化鐵,E裝置防倒吸,F裝置檢驗和吸收二氧化碳。尾氣是CO,點燃處理。
(3) CO還原氧化鐵生成黑色粉末可能是Fe、Fe3O4、FeO及其混合物。實驗1,證明甲組沒有Fe生成,乙組產生了Fe;實驗2,證明溶于酸時都生成了Fe2+;實驗3證明甲組生成了Fe3O4,乙組沒有生成;實驗4說明褪色的原因可能是SCN-可能被Cl2氧化。
考點:考查化學探究實驗與評價。


科目:高中化學 來源:2015屆江蘇省無錫江陰市高二下學期期中考試化學試卷(解析版) 題型:選擇題
下列熱化學方程式正確的是
A.S(s)+O2(g)= SO2(g);ΔH= -269.8kJ/mol
B.NaOH (aq)+HCl(aq)=NaCl(aq)+H2O(l);ΔH=+57.3kJ/mol
C.表示乙醇的燃燒熱:C2H5OH(l)+3O2(g)=2CO2(g)+ 3H2O(g);ΔH=-1367.0 kJ/mol
D.2NO2 = O2+2NO;ΔH= +116.2kJ/mol
查看答案和解析>>
科目:高中化學 來源:2015屆江蘇省高三上學期摸底考試化學試卷(解析版) 題型:選擇題
設NA為阿伏伽德羅常數的值。下列敘述正確的是
A.78gNa2O2固體中含有的陰離子數為NA
B.標準狀況下,2.24L氖氣所含原子數為0.2NA
C.1L 0.1 mol/L醋酸溶液中含有的氫離子數為0.1NA
D.標準狀況下,2.24L己烷含有分子的數目為0.1NA
查看答案和解析>>
科目:高中化學 來源:2015屆江蘇省南京市高三9月學情調研卷化學試卷(解析版) 題型:選擇題
短周期元素Q、W、X、Y、Z的原子序數依次增大,X元素的顏色反應呈黃色,Q原子的最外層電子數是其內層電子數的2倍,W、Z原子的最外層電子數相同,Z元素的核電荷數是W的2倍,Y是地殼中含量最多的金屬元素。下列說法不正確的是 ( )
A.工業上常用電解的方法制備X、Y的單質
B.元素Q和Z能形成QZ2型的共價化合物
C.原子半徑的大小順序:r(X)> r(Y)> r(W)> r(Q)
D.元素X、Y的最高價氧化物對應的水化物之間能發生反應
查看答案和解析>>
科目:高中化學 來源:2015屆江蘇省南京市高三9月學情調研卷化學試卷(解析版) 題型:選擇題
常溫下,下列各組離子在指定溶液中一定能大量共存的是()
A.1.0 mol·L-1KNO3溶液:H+、Fe2+、SCN-、SO42-
B.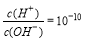 的溶液:K+、Ba2+、NO3-、Cl-
的溶液:K+、Ba2+、NO3-、Cl-
C.pH=0的溶液:Al3+、Cl-、SO42-、CO32-
D.c(ClO-) = 1.0 mol·L-1的溶液:Na+、I-、S2-、SO42-
查看答案和解析>>
科目:高中化學 來源:2015屆廣西桂林市高三上學期第一次月考化學試卷(解析版) 題型:選擇題
下列實驗誤差分析錯誤的是
A、用潤濕的pH試紙測稀堿溶液的pH,測定值偏小
B、用容量瓶配制溶液,定容時俯視刻度線,所配溶液濃度偏小
C、滴定前滴定管內無氣泡,終點讀數時有氣泡,所測體積偏小
D、測定中和反應的反應熱時,將堿緩慢倒入酸中,所測溫度值偏小
查看答案和解析>>
科目:高中化學 來源:2015屆廣西桂林市高三上學期第一次月考化學試卷(解析版) 題型:選擇題
已知單位體積的稀溶液中,非揮發性溶質的分子或離子數越多,該溶液的沸點就越高。則下列溶液沸點最高的是
A、0.01 mol·L-1的蔗糖溶液 B、0.01 mol·L-1的CaCl2溶液
C、0.02 mol·L-1的NaCl溶液 D、0.02 mol·L-1的CH3COOH溶液
查看答案和解析>>
科目:高中化學 來源:2015屆廣東肇慶中學高三8月考理綜化學試卷(解析版) 題型:選擇題
下列陳述中,Ⅰ、Ⅱ都正確且兩者間具有因果關系的一組是
選項 | 陳述Ⅰ | 陳述Ⅱ |
A | Na2O2使酚酞溶液變紅 | Na2O2能漂白織物、紙漿 |
B | SO2可使石蕊溶液先變紅后褪色 | SO2的水溶液具有酸性和漂白性 |
C | NH3、HCl可用作噴泉實驗 | NH3、HCl都極易溶于水 |
D | 晶體硅是良好的半導體材料 | 晶體硅可制作太陽能電池和光導纖維 |
查看答案和解析>>
科目:高中化學 來源:2015屆廣東省惠州市高三第一次調研考試化學試卷(解析版) 題型:選擇題
下述實驗設計能夠達到目的的是
選項 | 實驗目的 | 實驗設計 |
A | 證明Ksp(AgCl)﹥Ksp(AgI) | 往AgCl懸濁液中滴入KI濃溶液 |
B | 除去Cu粉中的CuO | 向混合物中滴加適量稀硝酸 |
C | 檢驗溶液中是否含有Fe2+ | 向溶液中滴入KSCN溶液,再滴加氯水 |
D | 證明H2CO3酸性比H2SiO3強 | Na2CO3和SiO2在高溫下熔融反應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com