
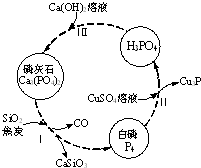
 磷及部分重要化合物的相互轉化如圖所示.
磷及部分重要化合物的相互轉化如圖所示.| 成分 | CaO | P2O5 | SO3 | CO2 |
| 質量分數(%) | 47.30 | 28.40 | 3.50 | 6.10 |
分析 (1)依據氧化還原反應中銅元素、磷元素化合價變化計算;
(2)磷酸為三元酸與氫氧化鈣反應,依據磷酸與氫氧化鈣量不同,得到的產物可能是:Ca3(PO4)2、CaHPO4、Ca(H2PO4)2;
(3)磷灰石中碳元素的質量分數=二氧化碳質量分數×二氧化碳中碳元素質量分數;
(4)根據鈣元素守恒計算;
(5)用m表示出磷灰石中Ca、S、P元素物質的量,計算出磷酸中P元素物質的量、硫酸中S元素物質的量,結合化學式可知n(Ca)=n(S)+$\frac{1}{2}$n(P),據此列方程解答.
解答 解:(1)Cu元素的化合價由+2價降低到+1價,CuSO4是氧化劑,P4部分磷元素由0價降低到-3價,部分磷元素由0價升高到+5價,磷元素的化合價既升高又降低,所以P4既是氧化劑又是還原劑,若有11molP4參加反應,其中5mol的P4做氧化劑,60mol硫酸銅做氧化劑,只有6mol的P4做還原劑,則由電子守恒可知,有1 mol的CuSO4參加反應,則被硫酸銅氧化的白磷分子的物質的量為n則:n×4(5-0)=1mol×(2-1),解得n=0.05mol;
故答案為:0.05mol
(2)磷酸為三元酸與氫氧化鈣反應,依據磷酸與氫氧化鈣量不同,得到的產物可能是:Ca3(PO4)2、CaHPO4、Ca(H2PO4)2;
故答案為:CaHPO4、Ca(H2PO4)2;
(1)磷灰石中碳元素的質量分數=6.10%×$\frac{12}{44}$=1.66%,故答案為:1.66%;
(2)100g磷灰石粉末中Ca元素質量=100g×47.3%×$\frac{40}{56}$,鈣元素全部以CaSO4的形式存在,根據Ca元素守恒可知,可以得到CaSO4的質量=$\frac{100g×47.3%×\frac{40}{56}}{\frac{40}{136}}$=114.87g,
故答案為:114.87;
(3)mg磷灰石中Ca元素物質的量=mg×47.3%÷56g/mol=0.00845m mol,S元素物質的量=mg×3.5%÷80g/mol=0.00044m mol,P元素物質的量=mg×28.4%×$\frac{62}{142}$÷31g/mol=0.004m mol,
磷酸中P元素物質的量=0.05L×0.5mol/L=0.025mol,硫酸中S元素質量=0.05L×0.1mol/L=0.005mol,
由化學式可知,n(Ca)=n(S)+$\frac{1}{2}$n(P),故0.00845m=(0.00044m+0.005)+(0.004m+0.025)×$\frac{1}{2}$,
解得m=2.91,
答:m的值為2.91.
點評 本題考查質量分數計算、混合物計算等,利用守恒進行計算,關鍵明確Ca元素沒有全部利用,P元素全部利用,題目計算量很大,題目難度較大.


科目:高中化學 來源: 題型:選擇題
| A. | 與水反應 | B. | 與氫氧化鈉溶液反應 | ||
| C. | 與硫酸反應 | D. | 與前三種物質均能反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 光伏發電主要利用高純度單質硅制成的硅太陽能電池 | |
| B. | 硅太陽能電池可將太陽能直接轉化為電能,減少化石燃料的使用,保護環境 | |
| C. | 硅的結構和金剛石類似,是具有金屬光澤的灰黑色固體 | |
| D. | 硅單質即能與氫氧化鈉反應又能與氫氟酸反應,所以硅是兩性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 上述實驗中不能用鹽酸代替硫酸 | |
| B. | 將試管充分振蕩后靜置,溶液顏色變為紫色 | |
| C. | 在酸性條件下,PbO2的氧化性比MnO4-的氧化性強 | |
| D. | 若硫酸錳充分反應,消耗PbO2的物質的量為0.01mol |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.| I1 | I2 | I3 | I4 | … | |
| 電離能(kJ/mol) | 738 | 1451 | 7733 | 10540 | … |

查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 6.02×1023 | B. | 12C原子質量的十二分之一 | ||
| C. | 0.012Kg12C所含的原子數 | D. | 1mol氧氣所含的微粒數 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 測定蒸氣的摩爾體積 | |
| B. | 與銀氨溶液反應,分析產生銀的量 | |
| C. | 與鈉反應,分析產生氫氣的量 | |
| D. | 用酸性高錳酸鉀溶液滴定,分析相關數據 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
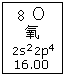
| A. | 氧元素的質量數是16 | |
| B. | 氧元素的相對原子質量是16.00 | |
| C. | 氧原子2p亞層有一個未成對電子 | |
| D. | 氧原子最外層有6個能量相同的電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NO3- | B. | SO42- | C. | Na+ | D. | H+ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com