
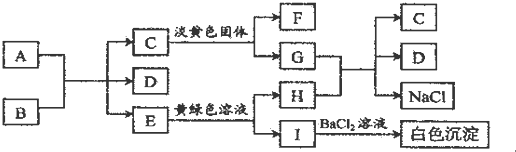
分析 根據圖中各物質轉化關系,A為固態單質,常溫下C、E、F都是無色氣體,則A與B的反應應為碳與濃酸硫或濃硝酸的反應,E能與黃綠色溶液(應為氯水)反應,生成I遇氯化鋇有白色沉淀,則I中應含有硫酸根,I為H2SO4,H為HCl,所以A與B的反應為碳與濃硫酸的反應,A為C,B為濃H2SO4,E為SO2,D為H2O,C是氣體能與淡黃色固體反應,則應為二氧化碳與過氧化鈉的反應,所以C為CO2,F為O2,G為Na2CO3,HCl與Na2CO3反應生成二氧化碳、氯化鈉和水,符合各物質轉化關系,據此答題.
解答 解:根據圖中各物質轉化關系,A為固態單質,常溫下C、E、F都是無色氣體,則A與B的反應應為碳與濃酸硫或濃硝酸的反應,E能與黃綠色溶液(應為氯水)反應,生成I遇氯化鋇有白色沉淀,則I中應含有硫酸根,I為H2SO4,H為HCl,所以A與B的反應為碳與濃硫酸的反應,A為C,B為濃H2SO4,E為SO2,D為H2O,C是氣體能與淡黃色固體反應,則應為二氧化碳與過氧化鈉的反應,所以C為CO2,F為O2,G為Na2CO3,HCl與Na2CO3反應生成二氧化碳、氯化鈉和水,符合各物質轉化關系,
(1)F為O2,題中淡黃色固體為過氧化鈉,過氧化鈉中陰陽離子個數比為1:2,
故答案為:O2;1:2;
(2)A與B反應的化學方程式是C+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑+CO2↑+2H2O,
故答案為:C+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑+CO2↑+2H2O;
(3)E轉變為H和I的離子方程式是SO2+Cl2+2H2O═4H++2Cl-+SO42-,
故答案為:SO2+Cl2+2H2O═4H++2Cl-+SO42-;
(4)I為H2SO4,少量I與BaCl2生成的白色沉淀為硫酸鋇,該沉淀中陰離子的檢驗操作為先加稀鹽酸,再加氯化鋇溶液,
故答案為:先加稀鹽酸,再加氯化鋇溶液.
點評 本題考查無機物的推斷,題目難度中等,物質的顏色為解答該題的突破口,注意把握反應的轉化關系的重要信息,側重于學生分析能力的考查,注意相關知識的學習.


 發散思維新課堂系列答案
發散思維新課堂系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
. .
.
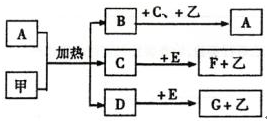
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
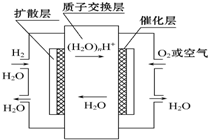
| A. | 正極通入H2,發生還原反應 | |
| B. | 負極通入H2,發生還原反應 | |
| C. | 導電離子為質子,且在電池內部由正極定向移向負極 | |
| D. | 總反應式為2H2+O2=2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 地球上絕大多數金屬元素是以游離態存在于自然界中的 | |
| B. | 在化學反應中,金屬容易失去電子,是還原劑 | |
| C. | 多數合金的熔點高于組成它的成分的金屬的熔點 | |
| D. | 硅單質是良好的半導體,所以它是金屬元素 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | SiO2是太陽能電池的主要原料 | |
| B. | 油脂和蛋白質都是高分子化合物 | |
| C. | 金屬的鍍層被破壞后,鍍鋅鐵比鍍銅鐵更容易被腐蝕 | |
| D. | 明礬凈水是因為能生成有吸附性的物質 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
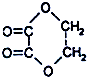 ④CH3OCOCH3 ⑤(COOC2H5)2 ⑥C2H5OCOOC2H5 ⑦CH3-COCH2O-CH3 ⑧CH3OCOOH ⑨HCOOCH3.
④CH3OCOCH3 ⑤(COOC2H5)2 ⑥C2H5OCOOC2H5 ⑦CH3-COCH2O-CH3 ⑧CH3OCOOH ⑨HCOOCH3.| A. | ①②⑤ | B. | ①②⑦ | C. | ②③⑧ | D. | ④⑥⑨ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 元素代號 | X | Y | Z | W | T |
| 原子半徑/nm | 0.186 | 0.143 | 0.102 | 0.074 | 0.071 |
| 主要化合價 | +1 | +3 | +6、-2 | -2 | -1、無正價 |
| A. | X與W形成的化合物中都只含離子鍵 | |
| B. | Z的氫化物與T的單質具有相同的核外電子數 | |
| C. | Y、X的最高價氧化物的水化物之間能反應 | |
| D. | Z的氧化物不止一種 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com