
I.X、W、Y、Z均為短周期主族元素,原子序數依次增大,X原子的最外層電子數是W的4倍,X、Y在周期表中相對位置如下圖。
| X | | |
| | | Y |
 8W2Yn(l)。放電時,W+離子向___極移動;正極的電極反應式為________。
8W2Yn(l)。放電時,W+離子向___極移動;正極的電極反應式為________。 zC,恒溫下,通過壓縮容器體積改變壓強,分別測得A的平衡濃度如下表:
zC,恒溫下,通過壓縮容器體積改變壓強,分別測得A的平衡濃度如下表:
I.(1)第二周期第ⅣA族;(2)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
(3)H2S+2Fe3+=2Fe2++2H++S↓;(4)nS8+16e-=8Sn2-;
II.(5)=;(6)K=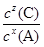 。
。
解析試題分析:I.X、W、Y、Z均為短周期主族元素,原子序數依次增大,X原子的最外層電子數是W的4倍,則根據X、Y在周期表中相對位置可知,X一定是第二周期元素,W、Y、Z均是第三周期元素,其中X是第ⅣA族的碳元素,W是鈉元素,Y是硫元素,Z是氯元素。
(1)X在周期表中的位置是第二周期第ⅣA族;
(2)氯氣與石灰乳反應的化學方程式為2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
(3)H2S具有還原性,能把鐵離子氧化生成單質硫,所以Y的氣態氫化物通入FeCl3溶液中,有Y單質析出的離子方程式為H2S+2Fe3+=2Fe2++2H++S↓;
(4)原電池中較活潑的金屬是負極,失去電子,發生氧化反應。電子經導線傳遞到正極,所以溶液中的陽離子向正極移動,正極得到電子,發生還原反應。因此放電時,Na+離子向正極移動;正極硫得到電子,電極反應式為nS8+16e-=8Sn2-;
II.(5)根據①②數據分析得出,壓強變為原來的2倍時,A的濃度變為原來的2倍,這說明增大壓強平衡不移動,因此正方應是體積不變的可逆反應,即x+y=z;
(6)由②③數據可知,壓強變為原來的5倍時A的濃度大于原來的5倍,這說明增大壓強平衡向逆反應方向移動,即正方應是體積增大的可逆反應。所以此時B不再是氣態,因此該溫度下反應的平衡常數表達式為K=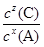 。
。
考點:考查元素推斷、氧化還原反應、離子反應、電極反應式的書寫以及外界條件對平衡狀態的影響和平衡常數表達式的書寫等


科目:高中化學 來源: 題型:填空題
為保持街道整潔、濕潤,在路面或廣場上噴灑含化學式為XY2的溶液作保濕劑。X原子的結構示意圖為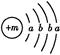 ,X的陽離子與Y的陰離子的電子層結構相同。元素Z、W均為短周期元素,它們原子的最外層電子數均是其電子層數的2倍,Z與Y相鄰且Z、W能形成一種WZ2型分子。
,X的陽離子與Y的陰離子的電子層結構相同。元素Z、W均為短周期元素,它們原子的最外層電子數均是其電子層數的2倍,Z與Y相鄰且Z、W能形成一種WZ2型分子。
(1)m= ,該保濕劑的化學式為
(2)Z、W元素的名稱為 、
(3)下列說法中正確的是
A.XY2和WZ2都為離子化合物
B.XY2中僅含離子鍵,WZ2中僅含極性共價鍵
C.H2Z比HY的穩定性強
D.X的陽離子比Y的陰離子半徑大
(4)下列化學用語表達正確的是
A.XY2的電子式:X2+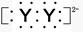
B.WZ2的結構式:Z=W=Z
C.Y元素的單質與H2Z水溶液反應的離子方程式為:Y2+Z2- 2Y-+Z↓
2Y-+Z↓
D.用電子式表示XY2的形成過程為: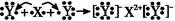
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、D、E是周期表中前四周期的元素,其有關性質或結構信息如下表:
| 元素 | 有關性質或結構信息 |
| A | 負二價的A元素的氫化物在通常狀況下是一種液體,其中A的質量分數為88.9% |
| B | B原子得到一個電子后3p軌道全充滿 |
| C | C原子的p軌道半充滿,它的氣態氫化物能與其最高價氧化物的水化物反應生成一種常見的鹽X |
| D | D元素的最高化合價與最低化合價的代數和為零,其最高價氧化物為分子晶體 |
| E | E元素的核電荷數等于A元素和B元素氫化物的核電荷數之和 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、D、E、F六種短周期主族元素,它們的原子序數依次增大。已知:A元素的原子半徑最小,B元素原子的最外層電子數是內層電子數的2倍,C元素的最高價氧化物對應的水化物與其氫化物反應能生成鹽,D與E同主族,E元素原子的最外層電子數比次外層電子數少2。請回答:
(1)元素C在周期表中的位置是________。
(2)元素D的單質與金屬鈉反應生成的化合物可作潛水面具中的供氧劑,這種化合物與水反應的離子方程式________________________________。
(3)D和E兩種元素相比較,其原子得電子能力較強的是________(寫名稱)。
以下說法中,可以證明上述結論的是__________(填寫編號)。
a.比較這兩種元素的常見單質的沸點
b.二者形成的化合物中,D元素的原子顯負價
c.比較這兩種元素的氣態氫化物的穩定性
d.比較這兩種元素氫化物的水溶液的酸性
(4)元素A、D、E與鈉元素可形成兩種酸式鹽(均含有該四種元素),這兩種酸式鹽在水溶液中反應的離子方程式是_________________________________。
(5)由元素A、B、D組成的一元酸X為日常生活中的調味劑,元素A、F組成的化合物為Y。在等體積、等pH的X、Y的溶液中分別加入等質量的鋅粉,反應后若最后僅有一份溶液中存在鋅粉,則反應過程中兩溶液中反應速率的大小關系是:X________Y(填“>”、“=”或“<”)。
(6)元素F的單質常溫下是一種氣體,工業上主要是通過電解其鈉鹽的飽和溶液的方法獲得該氣體,假定裝入的飽和溶液為100 mL(電解前后溶液體積變化可忽略),當測得陰極上產生11.2 mL(標準狀況)氣體時停止通電,將溶液搖勻,此時溶液的pH為________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、D、E五種短周期元素的原子序數依次增大。元素A的負一價離子具有和稀有氣體He一樣的結構,元素B的最外層電子數是內層電子總數的2倍,元素C是短周期元素中原子半徑最大的主族元素,元素D在地殼中的含量位于第二位,元素E與元素B可形成具有正四面體結構的物質。請回答下列問題:
(1)在周期表中,元素B位于第 周期第 族;A與C形成的離子化合物的化學式為 _________________ ; A與C形成的離子化合物與水反應的化學方程式為 。
(2)C形成的簡單離子的離子結構示意圖為 。
(3)D、E元素形成的化合物可與水反應生成一種沉淀和一種氣體,試寫出該反應的化學方程式: ___________ 。
(4)單質B與水反應是將B充分利用的措施之一,試寫出該反應的化學方程式: ______________________________________ 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
如圖是從元素周期表中截取的一個片斷,其中X、Y、Z、W均屬于短周期元素。請回答下列問題。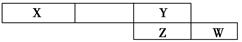
(1)若X單質為空氣中的主要成分之一,則W的原子結構示意圖為________。
(2)若Y、W、Z的最高價氧化物對應的水化物依次為一元酸、二元酸、三元酸,這三種酸的正鹽的含氧酸根離子中,有兩種的電子數相等,這兩種離子的離子符號是________、________。
(3)若Na與Y和Z的單質分別反應可以生成摩爾質量相同的兩種化合物,其中Na與Y形成的化合物的電子式為________,所含化學鍵的類型為________。
(4)Y元素在元素周期表中處于第________縱行(寫出所有可能縱行數)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
短周期元素A、X、D、E、R、T原子序數依次增大,原子結構及性質如表所示:
| 元素 | 結構及性質 |
| A | A的原子半徑最小 |
| X | X原子最外層電子數是次外層的兩倍 |
| D | D是短周期中金屬性最強的元素 |
| E | E的最高價氧化物對應水化物是一種常見的兩性氫氧化物 |
| R | R與X同主族 |
| T | T的負一價陰離子的核外電子排布與Ar原子相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
W、X、Y、Z是四種常見的短周期元素,其原子半徑隨原子序數變化如下圖所示。已知W的一種核素的質量數為18,中子數為10;X和Ne原子的核外電子數相差1;Y的單質是一種常見的半導體材料;Z的電負性在同周期主族元素中最大。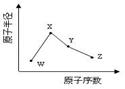
(1)X位于元素周期表中的位置 ;18W與X形成原子個數1:1的物質,該物質與H2O反應的化學方程式 。(在化學式中標出質量數18)
(2)X的單質和Y的單質相比,熔點較高的是_____(寫化學式);Z的氣態氫化物和溴化氫相比,較穩定的是_______(寫化學式)。
(3)Y與Z形成的化合物和足量水反應,生成一種弱酸和一種強酸,該反應的化學方程式是________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
下列關于元素周期律和元素周期表的論述中正確的是( )。
| A.同一主族的元素從上到下金屬性逐漸減弱 |
| B.元素周期表是元素周期律的具體表現形式 |
| C.同一周期從左到右,元素原子半徑逐漸增大 |
| D.非金屬元素的最高正化合價等于它的負化合價的絕對值 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com