
分析 (1)根據n=cv計算溶質Na2CO3的物質的量,利用Na2CO3•10H2O的物質的量等于Na2CO3的物質的量,根據m=nM計算Na2CO3•10H2O的質量;
(2)根據天平的稱量原理;
(3)根據容量瓶的使用方法分析;
(4)根據c=$\frac{n}{V}$分析操作對溶質的物質的量或對溶液的體積的影響判斷.
解答 解:(1)因配制溶液的體積為480ml,而容量瓶的規格沒有480ml,只能選用500ml,Na2CO3的物質的量n=cV=0.5L×0.08mol•L-1=0.04mol,Na2CO3•10H2O的物質的量等于Na2CO3的物質的量,所以Na2CO3•10H2O的質量0.04mol×286g/mol=11.4g,
故答案為:11.4;
(2)因天平的稱量原理:左盤物體的質量=右盤物體的質量+游碼的讀數,11.4g=m+0.4×2g,則實際稱量的碳酸鈉晶體m=10.6g,
故答案為:10.6;
(3)容量瓶使用前,必須檢驗是否漏水,故答案為:B;
(4)A、仰視刻度線,溶液的體積偏大,濃度偏低;
B、忘記將洗滌液轉入容量瓶,溶質的質量偏小,濃度偏低;
C、容量瓶內壁附有水珠而未干燥處理,溶液的體積不變,濃度不變;
D、溶解后沒有冷卻便進行定容,溶液的體積偏小,濃度偏高,
故答案為:偏低、偏低、無影響、偏高.
點評 本題考查了一定物質的量濃度溶液的配制過程以及誤差分析,難度不大,注意實驗的基本操作方法和注意事項.


科目:高中化學 來源: 題型:選擇題
| A. | 1s22s22p1 | B. | 1s22s22p33s1 | ||
| C. | 1s22s22p63s23p63d104s2 | D. | 1s22s22p63s23p63d34s2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | J | |||||||
| 2 | E | K | F | |||||
| 3 | A | C | D | I | G | R | ||
| 4 | B | H |
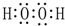 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向Fe2(SO4)3溶液中加入過量的Na2S:2Fe3++S2-=2Fe2++S↓ | |
| B. | 將鐵粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 用銅作電極電解飽和食鹽水:2Cl-+2H2O $\frac{\underline{\;電解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| D. | 將銅屑加入Fe3+ 溶液中:2Fe3++Cu=2Fe2++Cu2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
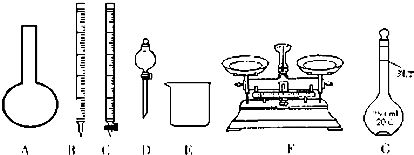
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .⑦的電子式為
.⑦的電子式為 .
.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
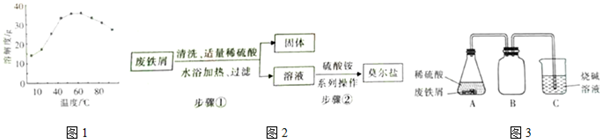
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com