
|


科目:高中化學 來源: 題型:
| A、Mg(OH)2的溶解度最小 |
| B、Ca(OH)2的溶解度最小 |
| C、AgCl的溶解度最小 |
| D、物質Ksp越大溶解度也越大 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、化學計量數:m+n>p |
| B、平衡向正反應方向移動了 |
| C、物質B的轉化率減小了 |
| D、物質C的質量分數增加了 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、加入水時,平衡向逆反應方向移動 |
| B、加入少量CH3COONa固體,平衡向正反應方向移動 |
| C、加入少量0.1mol?L-1 HCl溶液,平衡向逆反應方向移動,溶液中c(H+)增大 |
| D、加入少量NaOH固體,平衡向正反應方向移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 .請寫出有機化合物A與稀、冷的KMnO4溶液在堿性條件下反應的化學方程式:
.請寫出有機化合物A與稀、冷的KMnO4溶液在堿性條件下反應的化學方程式:查看答案和解析>>
科目:高中化學 來源: 題型:
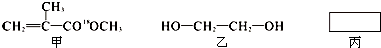

查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
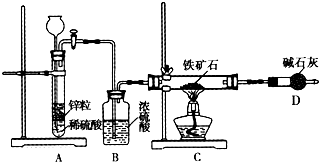

查看答案和解析>>
科目:高中化學 來源: 題型:
| A、通入足量CO2后的溶液中:Na+、SiO32-、CH3COO-、CO32- | ||
| B、無色溶液中:Mg2+、MnO4-、SO42-、K+ | ||
C、
| ||
| D、c(ClO-)=1.0mol?L-1的溶液:Na+、SO32-、S2-、SO42- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com