
| 實驗編號 | 實驗步驟 | 實驗現象 |
| i | 向甲溶液滴加KSCN溶液 | 溶液變紅色 |
| ii | 向乙溶液滴加酸性高錳酸鉀溶液 | 溶液不褪色 |
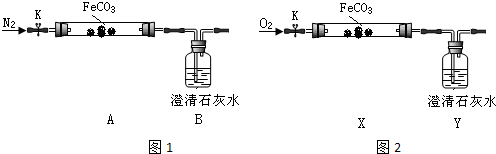
分析 (1)硫酸亞鐵和碳酸氫銨發生復分解反應生成碳酸亞鐵沉淀、二氧化碳和水;
(2)亞鐵鹽不穩定,易被空氣中氧氣氧化生成鐵鹽,從而干擾實驗;
根據元素守恒知,能使澄清石灰水變渾濁的氣體是二氧化碳;
(3)通入氮氣,玻璃管內氣壓不會減小,所以不會產生倒吸現象;
(4)①固體可能是氧化鐵和四氧化三鐵的混合物;
②鐵離子能和KSCN溶液反應生成血紅色溶液;
亞鐵離子具有還原性,能被酸性高錳酸鉀溶液氧化而使酸性高錳酸鉀溶液褪色;
(5)根據最初固體質量和減少質量之間的關系式確定固體成分.
解答 解:(1)硫酸亞鐵和碳酸氫銨溶液反應生成硫酸氫銨、碳酸亞鐵,硫酸氫銨電離氫離子,和碳酸氫銨反應生成二氧化碳和水,化學方程式為FeSO4+2NH4HCO3=FeCO3↓+(NH4)2SO4+CO2↑+H2O,離子方程式為Fe2++2HCO3-=FeCO3↓+CO2↑+H2O,
故答案為:Fe2++2HCO3-=FeCO3↓+CO2↑+H2O;
(2)探究碳酸亞鐵穩定性,排除裝置內空氣,避免空氣氧化+2價鐵元素;B中澄清石灰水變渾濁,說明碳酸亞鐵分解產物有二氧化碳,
故答案為:排盡裝置內空氣,避免氧氣干擾;分解產物有二氧化碳;
(3)繼續通入氮氣,不會減小玻璃管內氣壓,所以不能產生倒吸,則不必拆開A、B之間橡膠管,
故答案為:否;通入氮氣,玻璃管內氣壓不會減小;
(4)①固體可能是氧化鐵和四氧化三鐵,故答案為:氧化鐵和四氧化三鐵;
③實驗(i)只能證明樣品含有+3價鐵元素,不能證明是否有+2價.實驗(ii)證明殘留固體不含+2價,則一定含+3價鐵,故殘留固體成分是氧化鐵,
故答案為:i;溶液變紅色,只證明有+3價鐵,固體可能是氧化鐵、四氧化三鐵、氧化鐵和四氧化三鐵混合物;
(5)假設碳酸亞鐵在氧氣中分解產物為四氧化三鐵,則固體凈減質量為m.
6FeCO3+O2$\frac{\underline{\;高溫\;}}{\;}$2Fe3O4+6CO2 固體凈減質量
6×116 232
232.2g m
$\frac{6×116}{232}$=$\frac{23.2g}{m}$,
m=7.7g>7.2g.
假設碳酸亞鐵在氧氣中高溫反應固體產物為氧化鐵,則固體凈減質量為x.
4FeCO3+O2$\frac{\underline{\;高溫\;}}{\;}$2Fe2O3+4CO2 固體凈減質量
4×116 144
23.2g x
$\frac{4×116}{144}$=$\frac{23.2g}{x}$,x=7.2g,
與題意相符,故碳酸亞鐵在氧氣中高溫灼燒生成氧化鐵;
故答案為:氧化鐵.
點評 本題考查性質實驗方案設計,為高頻考點,涉及離子方程式的書寫、物質成分判斷、離子檢驗等知識點,同時考查學生分析判斷、實驗操作及計算能力,難點是(5)題成分判斷,要利用假設法解答,題目難度中等.


 應用題天天練四川大學出版社系列答案
應用題天天練四川大學出版社系列答案科目:高中化學 來源: 題型:選擇題
| A. | 硫化氫在氧氣中燃燒 | B. | 鐵在硫蒸氣中燃燒 | ||
| C. | 二氧化硫通入石灰水中 | D. | 硫酸中加入鐵粉 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
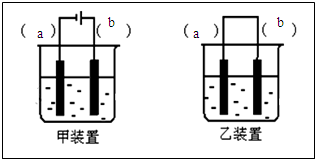
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 醛基的結構簡式-COH | B. | 丙烯分子的結構簡式為:CH3CHCH2 | ||
| C. | 四氯化碳分子的電子式為: | D. | 2-乙基-1,3-丁二烯的鍵線式: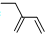 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
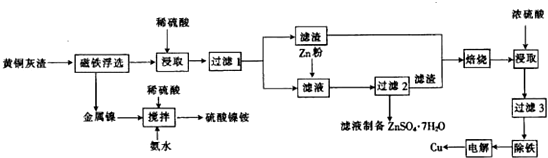
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
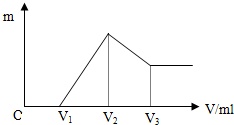 將0.1mol的鎂、鋁混合物溶于100ml 4mol/L的鹽酸中,然后滴加NaOH溶液,在滴加NaOH溶液過程中,沉淀的質量m隨加入NaOH溶液的體積V變化的關系如圖所示.
將0.1mol的鎂、鋁混合物溶于100ml 4mol/L的鹽酸中,然后滴加NaOH溶液,在滴加NaOH溶液過程中,沉淀的質量m隨加入NaOH溶液的體積V變化的關系如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 元素代號 | A | B | C | D | E |
| 原子半徑/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合價 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | A2+與D2-的核外電子數相等 | |
| B. | B與E形成的化合物既能與強酸反應又能與強堿反應 | |
| C. | 原子的失電子能力:C>A | |
| D. | 單質與濃度相等的稀鹽酸反應的速率為B>A |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 正丁烷分子儲存的能量大于異丁烷分子 | |
| B. | 正丁烷的穩定性大于異丁烷 | |
| C. | 異丁烷轉化為正丁烷的過程是一個放熱過程 | |
| D. | 異丁烷分子中的碳氫鍵比正丁烷的多 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com