
已知:Fe2O3(s) + ![]() C(s) =
C(s) = ![]() CO2(g) + 2 Fe(s) ΔΗ=234.1 kJ?mol-1
CO2(g) + 2 Fe(s) ΔΗ=234.1 kJ?mol-1
C(s) + O2(g) = CO2(g) ΔΗ=-393.5 kJ?mol-1
則2 Fe(s)+ ![]() O2(g) = Fe2O3(s) 的ΔΗ 是
O2(g) = Fe2O3(s) 的ΔΗ 是
A.-824.4 kJ?mol-1 B.-627.6 kJ?mol-1
C.-744.7 kJ?mol-1 D.-169.4 kJ?mol-1
 學練快車道快樂假期寒假作業系列答案
學練快車道快樂假期寒假作業系列答案 新思維寒假作業系列答案
新思維寒假作業系列答案科目:高中化學 來源: 題型:
下列說法不正確的是
A.已知冰的熔化熱為6.0 kJ/mol,冰中氫鍵鍵能為20 kJ/mol,假設1 mol冰中有2 mol 氫鍵,且熔化熱完全用于破壞冰的氫鍵,則最多只能破壞冰中15%的氫鍵
B.已知一定溫度下,醋酸溶液的物質的量濃度為c,電離度為α,![]() 。
。
若加入少量醋酸鈉固體,則CH3COOH![]() CH3COO-+H+向左移動,α減小,Ka變小
CH3COO-+H+向左移動,α減小,Ka變小
C.實驗測得環己烷(l)、環己烯(l)和苯(l)的標準燃燒熱分別為-3916 kJ/mol、-3747 kJ/mol和-3265 kJ/mol,可以證明在苯分子中不存在獨立的碳碳雙鍵
D.已知:Fe2O3(s)+3C(石墨)![]() 2Fe(s)+3CO(g),△H=+489.0 kJ/mol。
2Fe(s)+3CO(g),△H=+489.0 kJ/mol。
CO(g)+![]() O2(g)
O2(g)![]() CO2(g),△H=-283.0 kJ/mol。
CO2(g),△H=-283.0 kJ/mol。
C(石墨)+O2(g)![]() CO2(g),△H=-393.5 kJ/mol。
CO2(g),△H=-393.5 kJ/mol。
則4Fe(s)+3O2(g)![]() 2Fe2O3(s),△H=-1641.0 kJ/mol
2Fe2O3(s),△H=-1641.0 kJ/mol
查看答案和解析>>
科目:高中化學 來源:2012-2013學年云南省玉溪一中高二上學期期末考試化學試卷(帶解析) 題型:填空題
(每空2分,共6分)熱化學方程式中的ΔH實際上是熱力學中的一個物理量,叫做焓變,其數值和符號與反應物和生成物的總能量有關,也與反應物和生成物的鍵能有關。
(1)如下圖Ⅰ所示表示的是NO2和CO反應生成CO2和NO過程中能量變化示意圖,請寫出NO2和CO反應的熱化學方程式:________________________。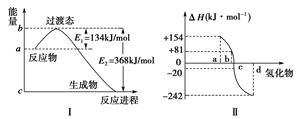
(2)圖Ⅱ表示氧族元素中的氧、硫、硒、碲在生成氫化物時的焓變數據,根據焓變數據可確定a、b、c、d分別代表哪種元素,試寫出硒化氫在熱力學標準態下,發生分解反應的熱化學方程式:_________________________________________________。
(3)已知:
①Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g);
ΔH=-25 kJ·mol-1,
②3Fe2O3(s)+CO(g)===2Fe3O4(s)+CO2(g);
ΔH=-47 kJ·mol-1,
③Fe3O4(s)+CO(g)===3FeO(s)+CO2(g);
ΔH=19 kJ·mol-1
請寫出CO還原FeO的熱化學方程式:
________________________________________________________________________。
查看答案和解析>>
科目:高中化學 來源:2014屆江蘇省宿遷市高三上學期第一次摸底考試化學試卷(解析版) 題型:填空題
研究CO2的利用對促進低碳社會的構建具有重要意義。
(1)將CO2與焦炭作用生成CO,CO可用于煉鐵等。
已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H 1=+489.0 kJ·mol-1
C(石墨)+CO2(g)=2CO(g) △H 2=+172.5 kJ·mol-1
則CO還原Fe2O3(s)的熱化學方程式為 。
(2)二氧化碳合成甲醇是碳減排的新方向,將CO2轉化為甲醇的熱化學方程式為:
CO2(g)+3H2(g) CH3OH(g)+H2O(g)
△H
CH3OH(g)+H2O(g)
△H
①該反應的平衡常數表達式為K= 。
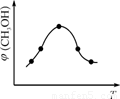
②取一定體積CO2和H2的混合氣體(物質的量之比為1∶3),加入恒容密閉容器中,發生上述反應。反應過程中測得甲醇的體積分數φ(CH3OH)與反應溫度T的關系如圖所示,則該反應的ΔH 0(填“>”、“<”或“=”)。
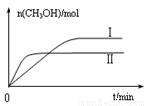
③在兩種不同條件下發生反應,測得CH3OH的物質的量隨時間變化如圖所示,曲線I、Ⅱ對應的平衡常數大小關系為KⅠ KⅡ(填“>”、“<”或“=”)。
(3)以CO2為原料還可以合成多種物質。
①工業上尿素[CO(NH2)2]由CO2和NH3在一定條件下合成,其反應方程式為 。當氨碳比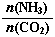 =3,達平衡時CO2的轉化率為60%,則NH3的平衡轉化率為
=3,達平衡時CO2的轉化率為60%,則NH3的平衡轉化率為
。
②用硫酸溶液作電解質進行電解,CO2在電極上可轉化為甲烷,該電極反應的方程式為 。
查看答案和解析>>
科目:高中化學 來源:2013屆浙江寧波金蘭合作組織高二下學期期中聯考化學試卷(解析版) 題型:選擇題
下列說法不正確的是
A.已知冰的熔化熱為6.0 kJ/mol,冰中氫鍵鍵能為20 kJ/mol,假設1 mol冰中有2 mol 氫鍵,且熔化熱完全用于破壞冰的氫鍵,則最多只能破壞冰中15%的氫鍵
B.已知一定溫度下,醋酸溶液的物質的量濃度為c,電離度為α,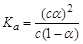 。若加入少量醋酸鈉固體,則CH3COOH
。若加入少量醋酸鈉固體,則CH3COOH CH3COO-+H+向左移動,α減小,Ka變小
CH3COO-+H+向左移動,α減小,Ka變小
C.實驗測得環己烷(l)、環己烯(l)和苯(l)的標準燃燒熱分別為-3916 kJ/mol、-3747 kJ/mol和-3265 kJ/mol,可以證明在苯分子中不存在獨立的碳碳雙鍵
D.已知:Fe2O3(s)+3C(石墨) 2Fe(s)+3CO(g),△H=+489.0 kJ/mol。
2Fe(s)+3CO(g),△H=+489.0 kJ/mol。
CO(g)+1/2O2(g) CO2(g),△H=-283.0 kJ/mol。
CO2(g),△H=-283.0 kJ/mol。
C(石墨)+O2(g) CO2(g),△H=-393.5 kJ/mol。
CO2(g),△H=-393.5 kJ/mol。
則4Fe(s)+3O2(g) 2Fe2O3(s),△H=-1641.0 kJ/mol
2Fe2O3(s),△H=-1641.0 kJ/mol
查看答案和解析>>
科目:高中化學 來源:2010-2011學年廣東省中山市實驗高中高三12月月考(理綜)化學部分 題型:選擇題
已知:Fe2O3 (s)+C(s)= CO2(g)+2Fe(s) △H=234.1kJ·mol-1
C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1 則2Fe(s)+O2(g ) = Fe2O3(s) 的△H是
A.-824.4kJ·mol-1 B.-627.6kJ·mol-1
C.-744.7kJ·mol-1 D.-169.4kJ·mol-1
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com