
【題目】如圖是元素周期表的一部分,下列敘述不正確的是
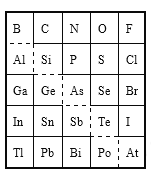
A. Sn的最高正價為+4
B. Br的最高價氧化物對應水化物的化學式為HBrO3
C. 酸性強弱:H3AsO4<H2SeO4
D. 原子半徑比較:N<Si
科目:高中化學 來源: 題型:
【題目】過二硫酸鉀(K2S2O8) 在科研與工業上有重要用途。
(1)H2S2O8的結構式如圖,其中S元素的化合價為__________。在Ag+催化下,S2O82-能使含Mn2+的溶液變成紫紅色,氧化產物是___________(填離子符號)。

(2)某廠采用濕法K2S2O8氧化脫硝和氨法脫硫工藝綜合處理鍋爐煙氣,提高了煙氣處理效率,處理液還可以用作城市植被綠化的肥料。
①脫硫過程中,當氨吸收液的pH=6時,n(SO32-)∶n(HSO3-)=________。
[巳知:25℃時,Ka1(H2SO3)=1.5×10-2,K a2(H2SO3)=1.0×10-7]
②脫硝過程中依次發生兩步反應:第1步,K2S2O8將NO氧化成HNO2,第2步,K2S2O8繼續氧化HNO2,第2步反應的化學方程式為______________________________________;
(3)過二硫酸鉀可通過“電解→轉化→提純”方法制得,電解裝置示意圖如圖所示。
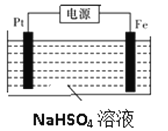
①電解時,鐵電極連接電源的_________________極。
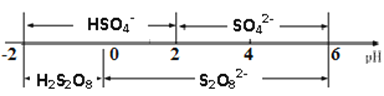
②常溫下,電解液中含硫微粒的主要存在形式與pH的關系如下圖所示。在陽極放電的離子主要是HSO4-,陽極區電解質溶液的pH范圍為_________,陽極的電極反應式為________________________。
③往電解產品中加入硫酸鉀,使其轉化為過二硫酸鉀粗產品,提純粗產品的方法____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,反應3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g),在一密閉容器中進行達平衡后,試回答:
Fe3O4(s)+4H2(g),在一密閉容器中進行達平衡后,試回答:
(1)增加Fe的物質的量,其正反應速率___________。(A.變快 B.不變 C變慢,前4問填字母代號)。
(2)將容器的體積縮小一半,其正反應速率___________ ,逆反應速率___________。
(3)若保持體積不變,充入Ar,其逆反應速率___________
(4)保持壓強不變,充入Ar,其正反應速率 ___________。
(5)保持壓強不變,充入Ar,該反應向___________ 方向移動。(填正移、逆移或不移)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有5種短周期元素的原子序數按E、D、B、A、C 的順序依次增大; A、C 同周期,B、C同主族;A與B 可形成離子化合物A2B,A2B 中陰陽離子的電子層結構完全相同,且電子總數為30;D 和E可形成4 核10 電子的分子。試回答下列問題:
(1)寫出下列物質的電子式:
①D元素形成的單質___________。
②B與E 形成的四原子化合物___________。
③A、B、E 形成的化合物___________。
④D、E 形成的簡單化合物___________。
(2)B、D、E形成的原子個數3︰2︰4的鹽的化學式為_______,類別屬于______化合物(填離子或共價),含有的化學鍵類型__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】環境中常見的重金屬污染物有汞、鉛、錳、鉻、鎘。處理工業廢水中含有的![]() 和
和![]() 常用的方法是還原沉淀法,該法的工藝流程為
常用的方法是還原沉淀法,該法的工藝流程為![]()
![]()
![]()
![]() Cr3+
Cr3+![]() Cr(OH)3。
Cr(OH)3。
其中第①步存在平衡:2![]() (黃色)+2H+
(黃色)+2H+![]()
![]() (橙色)+H2O。
(橙色)+H2O。
(1)寫出第①步反應的平衡常數表達式:_________________________________。
(2)關于第①步反應,下列說法正確的是________(填序號)。
A.通過測定溶液的pH可以判斷反應是否已達到平衡狀態
B.該反應為氧化還原反應
C.在強酸性環境下,溶液的顏色為橙色
(3)第②步反應中,還原0.1 mol![]() ,需要________mol FeSO4·7H2O。
,需要________mol FeSO4·7H2O。
(4)第③步反應除生成Cr(OH)3沉淀外,還可能生成的沉淀為________。
(5)在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)![]() Cr3+(aq)+3OH-(aq)。常溫下,Cr(OH)3的溶度積常數Ksp=10-32,當溶液中Cr3+的濃度降至10-5mol·L-1,認為Cr3+已經完全沉淀。現將第③步反應后溶液的pH調至4,請通過計算說明Cr3+是否沉淀完全(請寫出計算過程)。____________
Cr3+(aq)+3OH-(aq)。常溫下,Cr(OH)3的溶度積常數Ksp=10-32,當溶液中Cr3+的濃度降至10-5mol·L-1,認為Cr3+已經完全沉淀。現將第③步反應后溶液的pH調至4,請通過計算說明Cr3+是否沉淀完全(請寫出計算過程)。____________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氨氣是一種重要化合物,在工農業生產、生活中有著重要作用。
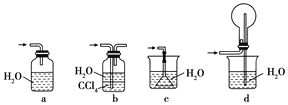
(1)“氨的催化氧化”是工業生產硝酸的重要步驟。某化學課外活動小組設計了如下裝置模擬該實驗過程,并用水吸收制取硝酸(固定裝置略去):
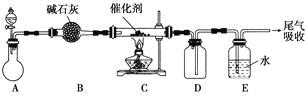
①A裝置的分液漏斗中盛放濃氨水,則燒瓶中盛放的藥品應該是________。
②C裝置中發生反應的化學方程式為________________。
③反應后,裝置E中除存在較多的H+外,還可能存在的一種離子是________,試設計實驗證明這種離子的存在_____________________。
④下列哪些裝置可以同時起到裝置D和E的作用________(填代號)。
(2)若將氯氣和氨氣在集氣瓶中混合,會出現濃厚的白煙并在容器內壁凝結,另一生成物是空氣的主要成分之一,請寫出反應的化學方程式:________________(不必配平),該反應生成的還原產物的化學鍵類型是________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表為元素周期表的一部分,請參照元素①-⑩在表中的位置,回答下列問題:
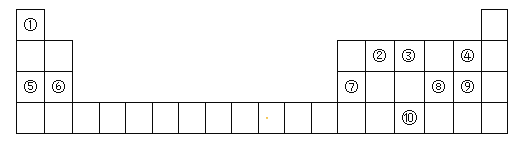
(1)元素⑩在周期表中的位置是_____,⑦的原子結構示意圖為_____。
(2)④、⑤、⑥的簡單離子半徑由大到小的順序為______(用離子符號和“>”表示)。
(3)④⑧⑨的氣態氫化物中,最穩定的是______(用化學式表示),最高價氧化物對應水化物中,酸性最強的是_____(用化學式表示)。
(4)⑤的最高價氧化物對應的水化物與⑦的最高價氧化物對應的水化物發生反應的離子方程式___。
(5)由①③⑨組成的離子化合物的化學式為____,其中含有的化學鍵類型是______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】過氧化氫(H2O2)溶液俗稱雙氧水,醫療上常用3%的雙氧水進行傷口消毒。H2O2能與SO2反應生成H2SO4, H2O2的分子結構如圖所示。下列說法錯誤的是( )

A. H2O2的結構式為H—O—O—H
B. H2O2為含有極性鍵和非極性鍵的共價化合物
C. 與SO2在水溶液中反應的離子方程式為SO2+ H2O2=2H++SO42-
D. H2O2與SO2反應過程中有共價鍵斷裂,同時有共價鍵和離子鍵形成
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組離子一定能大量存在的是
A. 加入鋁粉可以產生H2的溶液中:Al3+、K+、SO42-、Cl﹣
B. 滴入酚酞顯紅色的溶液:Na+、Mg2+、NO3﹣、HSO3﹣
C. 在酸性溶液中:Cu2+、I-、![]() 、Na+
、Na+
D. 在中性溶液中:Mg2+、NO3-、Cl-、SO42-
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com