
【題目】某有機物的結構簡式如圖所示,下列關于該有機物的性質說法錯誤的是( )
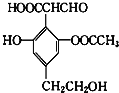
A. 1mol該物質可與4mol氫氧化鈉溶液反應
B. 與NaHCO3溶液反應可以產生CO2氣體
C. 該物質與H2反應,1mol該物質最多消耗3mol H2
D. 該物質可以使酸性KMnO4溶液褪色,也可發生消去反應
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】硫元素在自然界中通常以硫化物、硫酸鹽或單質的形式存在,其單質和化合物在工農業生產中有著重要的作用。
(1)硫元素在周期表中的位置為___________,其最簡單氣態氫化物的電子式為_________。
(2)在工業上SO2可以用于制備H2SO4。
已知SO2(g)+![]() O2(g)+H2O(g)=H2SO4(l) △H1=-272.5kJ·mol-1
O2(g)+H2O(g)=H2SO4(l) △H1=-272.5kJ·mol-1
H2O(g)=H2O(l) △H2=-44kJ·mol-1
SO3(g)+H2O(l)=H2SO4(l) △H3=-130kJ·mol-1
則2SO2(g)+O2(g)=2SO3(g) △H=_____________kJ·mol-1
(3)某興趣小組同學探究SO2的還原性,使用的藥品和裝置如圖所示:

A瓶中發生反應的離子方程式為_______________________。B瓶中出現的現象為________。若要證明A、B的反應中SO2均顯現還原性被氧化為SO42—,可以采取的操作和現象是_______________________________________。
(4)硫的氧化物排放到大氣中會造成空氣污染,常溫常壓下用如圖所示傳感器可以檢測空氣中SO2的含量。下列關于該傳感器的敘述正確的是__________(填序號)。

A. a為電源的正極
B. Pt電極網上發生氧化反應
C.當電路中電子轉移0.5mol時,進入傳感器的SO2為11.2L
D.陰極的電極反應是2HSO3—+2H+-2e—=S2O42—+2H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.高鐵酸鉀(K2FeO4)是一種新型、高效、多功能綠色水處理劑,工業上是先制得高鐵酸鈉,然后在低溫下,向高鐵酸鈉溶液中加入KOH至飽和,使高鐵酸鉀析出。
(1)干法制備高鐵酸鈉的主要反應為:2FeSO4 + 6 Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,該反應中Na2O2 是___________(填氧化劑、還原劑)
(2)濕法制備高鐵酸鉀的反應體系中有六種微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①堿性條件下,氧化劑和還原劑的物質的量的比為3:2發生反應,寫出并配平濕法制高鐵酸鉀的離子反應方程式:__________________。
②若反應過程中轉移了0.3mol電子,則還原產物的物質的量為__________mol。
Ⅱ.已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(1)含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此時被氧化的離子是______。
(2)若向含a mol FeI2和b mol FeBr2的溶液中通入c mol Cl2,當I-、Fe2+、Br-完全被氧化時,c=__________(用含a、b的代數式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】寫出化學方程式
(1)硫在氧氣中燃燒的化學方程式____
(2)碳粉和氧氣的化學反應方程式____
(3)水蒸氣與灼熱的炭發生氧化還原反應的化學方程式____
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】東晉《華陽國志南中志》卷四中已有關于白銅的記載,云南鎳白銅(銅鎳合金)聞名中外,曾主要用于造幣,亦可用于制作仿銀飾品。回答下列問題:
(1)鎳元素的基態價電子排布式為_____________,3d能級上的未成對的電子數為______。
(2)硫酸鎳溶于氨水形成[Ni(NH3)6]SO4藍色溶液。
①[Ni(NH3)6]SO4中陰離子的立體構型是___________。
②在[Ni(NH3)6]2+中Ni2+與NH3之間形成的化學鍵稱為______________,提供孤電子對的成鍵原子是_____________。
③氨的沸點_________(填“高于”或“低于”)膦(PH3),原因是__________________;氨是_________分子(填“極性”或“非極性”),中心原子的軌道雜化類型為_______。
(3)單質銅及鎳都是由______________鍵形成的晶體。
(4)某鎳白銅合金的立方晶胞結構如圖所示。
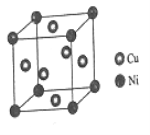
①晶胞中銅原子與鎳原子的數量比為___________。
②若合金的密度為dg/cm3,晶胞邊長a=______________nm。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應既屬于化合反應,又屬于氧化還原反應的是( )
A.Fe+2HCl=H2↑+FeCl2B.2FeCl2+Cl2=2FeCl3
C.CaO+H2O=Ca(OH)2D.2Fe(OH)3![]() Fe2O3+3H2O
Fe2O3+3H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某實驗小組利用下圖所示裝置在實驗室欲制備乙酸乙酯。
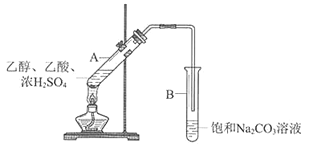
(1)B裝置中,導管口略高于液面的目的是________________________
(2)為了改善反應過程中混合溶液變黑的現象,甲同學采用NaHSO4代替濃硫酸做催化劑(其他試劑及用量不變)來制備乙酸乙酯,NaHSO4可代替濃硫酸做催化劑的原因是__________________________________________________________
(3)下圖是甲同學采用NaHSO4做催化劑,其他條件不變(其中乙酸用量為2 mL)不同質量的NaHSO4來制備乙酸乙酯的催化效果圖,其中NaHSO4的質量為_______g時催化效果最好。

(4)乙同學實驗時,在飽和NaCO3中滴加兩滴酚酞,實驗結束,取下試管B振蕩,紅色褪去。為探究褪色的原因,進行如下實驗。
編號 | ① | ② | ③ |
實驗 |
|
|
|
操作 | 充分振蕩、靜置 | 充分振蕩、靜置 | 充分振蕩、靜置、分液。取下層溶液,加入飽和Na2CO3溶液 |
現象 | 上層液體變薄,冒氣泡,下層溶液紅色褪去 | 上層液體不變薄,無氣泡,下層溶液紅色褪去 |
a試管①中產生氣泡的原因是(用化學方程式解釋)____________________________。
b對比實驗①和②可得出的結論是___________________________________。
c針對實驗②中現象,乙同學提出猜想:酚酞更易溶于乙酸乙酯。實驗③中觀察到__________________________________,證實乙的猜想正確。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯化亞砜(SOCl2)是一種液態化合物,在農藥、制藥行業中用途廣泛。實驗室合成原理為:SO2+Cl2+SCl2=2SOCl2,部分裝置如圖所示,回答以下問題:

已知:①SOCl2沸點為78.8℃,SCl2 的沸點為50℃,且兩種液體可互溶。
②SOCl2遇水劇烈反應,液面上產生白霧,并帶有刺激性氣味的有氣體產生。
(1)實驗室制取SOCl2在三頸燒瓶中進行,整個裝置所選儀器的連接順序是:⑥→__________→①,②←______________(某些儀器可以多次使用)。
(2)儀器a的名稱是________,儀器b的作用是____________。
(3)本實驗中制Cl2的離子方程式為___________________,本實驗中制SO2的化學方程式為______________________,SOCl2與水反應的化學方程式為___________。
(4)實驗結束后,從三頸燒瓶分離出SOCl2的實驗操作名稱是_________________。若反應中消耗Cl2的體積為896 mL(標準狀況,SO2足量),最后得到純凈的SOCl2 7.14 g,則SOCl2的產率為_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】請按指定要求完成下列問題。
(1)在3BrF3+5H2O=HBrO3+Br2+9HF+O2↑的反應中,3mol的BrF3參加反應時,被水還原的BrF3的物質的量是___。
(2)已知砒霜As2O3與Zn可發生如下反應:As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O
①請用雙線橋法標出電子轉移的方向和數目___。
②若生成0.2molAsH3,則轉移的電子數為___。
(3)二氧化氯(ClO2)是一種在水處理等方面有廣泛應用的高效安全消毒劑,制備ClO2有以下兩種方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
①方法一中氧化劑與還原劑的物質的量之比為___。
②若兩種方法制備得到相同條件下相同體積的ClO2氣體,則兩種方法中消耗的還原劑質量之比是___。
③Cl2與ClO2均用作水處理劑,若它們中的氯元素均被還原為Cl-,則相同質量的ClO2是Cl2消毒效率的___倍(消毒效率:等質量兩種物質所轉移電子的物質的量之比)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com