
【題目】在![]() 時,
時,![]() 橘紅色
橘紅色![]() 在水溶液中沉淀溶解平衡曲線如圖所示。又知AgCl的
在水溶液中沉淀溶解平衡曲線如圖所示。又知AgCl的![]() 下列說法正確的是
下列說法正確的是

A.將![]() 溶液滴加到KCl溶液中,反應的活化能幾乎為零
溶液滴加到KCl溶液中,反應的活化能幾乎為零
B.![]() 時,
時,![]() 的
的![]()
C.飽和![]() 溶液中,加入水能使溶液由X點變為Y點
溶液中,加入水能使溶液由X點變為Y點
D.![]() 時,AgCl比
時,AgCl比![]() 的溶解度大
的溶解度大
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】25℃時,將某一元酸HA和NaOH溶液等體積混合(體積變化忽略不計),測得反應后溶液的pH如下表,下列判斷不正確的是( )
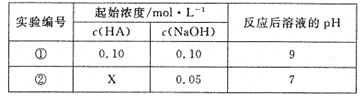
A.X>0.05
B.將實驗①所得溶液加水稀釋后,c(OHˉ )/c(A-)變大
C.實驗①所得溶液c(A-)+c(HA)=0.10mol·L-1
D.實驗②所得溶液: c(Na+)+c(OH-)= c(A-)+c(H+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,體積為10 L的密閉容器中,1 mol X和1 mol Y進行反應:2X(g)+Y(g) ![]() Z(g),經60 s達到平衡,生成0.3 mol Z。下列說法正確的是
Z(g),經60 s達到平衡,生成0.3 mol Z。下列說法正確的是
A. 若增大壓強,則物質Y的轉化率減小
B. 將容器體積變為20 L,Z的平衡濃度變為原來的![]()
C. 以X的濃度變化表示的反應速率為0.001 mol/(L·s)
D. 若升高溫度,X的體積分數增大,則該反應的ΔH >0
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】請回答下列問題:
(1)25℃時,pH=5的CH3COOH溶液中.加入少量NaOH固體,則溶液中![]() _______(填“增大”、“減小”或“不變”)。
_______(填“增大”、“減小”或“不變”)。
(2)25℃下,向某Na2CO3溶液中加入稀鹽酸,其中含碳元素的各種微粒物質的量分數(φ)隨溶液pH變化的部分情況如圖所示。
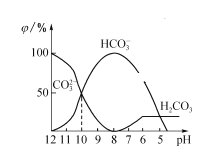
①在同一溶液中,H2CO3、HCO3-、CO32-______(填“能”或“不能”)大量共存。
②當pH =7時,溶液中含碳元素的微粒主要為________。溶液中各種離子的物質的量濃度大小關系為___________________________。
③反應的CO32-+H2O![]() HCO3-+OH-的平衡常數Kh值為_________。
HCO3-+OH-的平衡常數Kh值為_________。
(3)生物脫H2S的原理為:H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4、4FeSO4+O2+2H2SO4 2Fe2(SO4)3+2H2O。
2Fe2(SO4)3+2H2O。
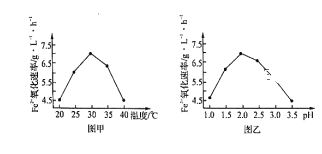
①硫桿菌存在時,FeSO4被氧化的速率是無菌時的5×105倍,該菌的作用是___________。
②由圖甲和圖乙判斷使用硫桿菌的最佳條件為____________。在最佳條件下,該反應的加熱
方式為_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】T℃時,在一個體積為2L的容器中,A氣體與B氣體反應生成C氣體,反應過程中A、B、C濃度變化如圖所示.

1)寫出該反應的方程式:__________________
2)計算該溫度下該反應的平衡常數:____________
3)已知:K(300℃)<K(350℃),該反應是__________熱反應.
4)0~4分鐘時,B的平均反應速率為:____________
5)到達平衡時A的轉化率為:____________
6)恒容條件下,下列措施中能使n(A)/n(C)降低的有____________.
A.充入氦氣 B.使用催化劑
C.再充入2.4molA和1.6molB D.降低溫度.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用NA表示阿伏加德羅常數的數值,下列說法中正確的是( )
①標準狀況下,4.48L NO 和2.24L O2 充分混合后所得混合物分子數為0.2NA
②含13g甲醛(HCHO)和17g乙酸(CH3COOH)的液體混合物中,氧原子數目為NA
③0.1 mol H2和 0.1 mol I2于密閉容器中充分反應后,其分子總數為 0.2NA
④1mol Na2O 和Na2O2混合物中含有的陰、陽離子總數是3NA
⑤常溫常壓下,30g的C2H6含有的共價鍵數為6NA
⑥標準狀況下,22.4L HF中所含F原子數目為NA
⑦在反應KIO3+6HI=KI+3I2+3H2O中,每生成3molI2轉移的電子數為5NA
A.②③④⑦B.①④⑤⑥C.①②③⑤⑥D.①②④⑥⑦
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關實驗及其分析敘述正確的是( )
A.向2.0mL濃度均為0.lmolL-l的KC1、KI混合溶液中滴加1~2滴0.0lmol/LAgNO3溶液,振蕩,沉淀呈黃色,說明AgCl的Ksp比AgI的Ksp大
B.在稀硫酸中加入銅粉,銅粉不溶解;再加入適量的H2O2,銅粉仍不溶解
C.向AlC13溶液中滴加氨水,產生白色沉淀;再加入NaHSO4溶液,沉淀不消失
D.將CO2通入Ba(NO3)2溶液中至飽和,無沉淀產生;再通入SO2,也無沉淀產生
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】醋酸亞鉻水合物[Cr(CH3COO)2]2·2H2O是一種氧氣吸收劑,為紅棕色晶體,易被氧化,不溶于水和乙醚(易揮發的有機溶劑),微溶于乙醇,易溶于鹽酸,其制備裝置如下(已知Cr3+水溶液顏色為綠色,Cr2+水溶液顏色為藍色):

(1)裝置甲中連通管a的作用是________________________。
(2)向三頸燒瓶中依次加入過量鋅粒、適量CrCl3溶液:關閉k2打開k1,旋開分液漏斗的旋塞并控制好滴速;當觀察到三頸燒瓶中溶液顏色__________________時,打開k2關閉k1,當觀察到裝置乙中出現大量紅棕色晶體時,關閉分液漏斗的旋塞。
(3)裝置乙中反應的離子方程式為__________________________________。
(4)將裝置乙中混合物快速過濾、洗滌和干燥,稱量得到a g [Cr(CH3COO)2]2·2H2O。洗滌時依次用去氧的冷蒸餾水、無水乙醇、乙醚洗滌。其中乙醇洗滌的目的是___________。
(5)若實驗所取用的CrCl3溶液中含溶質b g,則[Cr(CH3COO)2]2·2H2O (相對分子質量為376) 的產率是________________。
(6)該實驗裝置有一個明顯的缺陷,解決此缺陷的措施為________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫單質和化合物在工農業生產中有著重要的應用,而SO2直接排放會對環境造成危害。
Ⅰ.已知:重晶石(BaSO4)高溫煅燒可發生一系列反應,其中部分反應如下:
BaSO4(s)+4C(s)=BaS(s)+4CO(g) ΔH=+571.2 kJ·mol-1
BaS(s)=Ba(s)+S(s) ΔH=+460 kJ·mol-1
已知:2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
則:Ba(s)+S(s)+2O2(g)=BaSO4(s) ΔH=____________。
Ⅱ.SO2的尾氣處理通常有以下幾種方法:
(1)活性炭還原法:反應原理:恒溫恒容時2C(s)+2SO2(g)![]() S2(g)+2CO2(g)。反應進行到不同時間測得各物質的濃度如圖:
S2(g)+2CO2(g)。反應進行到不同時間測得各物質的濃度如圖:
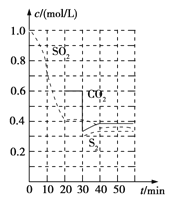
①0~20 min反應速率表示為v(SO2)=____________;
②30 min時,改變某一條件平衡發生移動,則改變的條件最有可能是____________;
③平衡常數的表達式K=____________。
(2)亞硫酸鈉吸收法
①Na2SO3溶液吸收SO2的離子方程式為__________________;
②常溫下,當吸收至NaHSO3時,吸收液中相關離子濃度關系一定正確的是____________(填序號)。
a.c(Na+)+c(H+)>c(SO32-)+c(HSO3-)+c(OH-)
b.c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3)
c.c(Na+)>c(HSO3-)>c(H+)>c(SO32-)
d.水電離出c(H+)=1×10-8mol/L
(3)電化學處理法

①如圖所示,Pt(Ⅰ)電極的反應式為__________________;
②當電路中轉移0.02 mol e-時(較濃H2SO4尚未排出),交換膜左側溶液中約增加________mol離子。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com