


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
| A、由Al、Cu、稀H2SO4組成原電池,其負極反應式為:Al→Al3++3e- |
| B、由Mg、Al、NaOH溶液組成原電池,其負極反應式為:Al+4OH→-Al(OH)4-+3e- |
| C、由Fe、Cu、FeCl3溶液組成原電池,其負極反應式為:Cu→Cu2++2e- |
| D、由Al、Cu、濃硝酸組成原電池,其負極反應式為:Cu→Cu2++2e- |
查看答案和解析>>
科目:高中化學 來源: 題型:
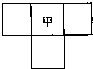 甲、乙、丙、丁四種短周期元素的位置如圖(其中乙、丙、丁的位置未標出),已知四種元素的原子序數之和為36,乙的原子序數與甲、丁原子序數之和相等.
甲、乙、丙、丁四種短周期元素的位置如圖(其中乙、丙、丁的位置未標出),已知四種元素的原子序數之和為36,乙的原子序數與甲、丁原子序數之和相等.查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:

| 物質類別 | 酸 | 堿 | 鹽 | 氧化物 | 氫化物 |
| 化學式 | ①HNO3 ② |
③NaOH ④ |
⑤Na2SO4 ⑥ |
⑦SO2 ⑧SO3 |
⑨NH3 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、NaClO4和KClO3 |
| B、KClO和KCl |
| C、NaClO和NaCl |
| D、NaCl和KCl |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 放電 |
| 充電 |
| A、充電時陽極反應:Ni(OH)2-e-+OH-=NiOOH+H2O |
| B、充電時陰極附近溶液的堿性增強 |
| C、放電過程是電能轉化為化學能的過程 |
| D、放電時負極反應:Cd+2OH--2e-=Cd(OH)2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com