
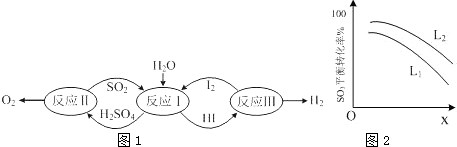
分析 (1)由圖可知,反應I為二氧化硫與碘發生氧化還原反應生成硫酸和HI;
(2)①分成兩層,與溶解性、密度有關;
②兩層的顏色不同;
③H2SO4中c(H+):c(SO42-)=2:1,且HI電離出氫離子;
(3)①由圖可知,X越大,轉化率越低;
②分解反應為吸熱反應,溫度高,轉化率大.
解答 解:(1)由圖可知,反應I為二氧化硫與碘發生氧化還原反應生成硫酸和HI,該反應為SO2+2H2O+I2=H2SO4+2HI,
故答案為:SO2+2H2O+I2=H2SO4+2HI;
(2)①a.兩層溶液的密度存在差,才出現上下層,故a正確;
b.加I2前,H2SO4溶液和HI溶液互溶,與分層無關,故b錯誤;
c.I2在HI溶液中比在H2SO4溶液中易溶,則碘在不同溶劑中溶解性不同,類似萃取,與分層有關,故c正確;
故答案為:ac;
②辨別兩層溶液的方法是:觀察顏色,顏色深的為HI層,顏色淺的為硫酸層,
故答案為:觀察顏色,顏色深的為HI層,顏色淺的為硫酸層;
③H2SO4層中c(H+):c(SO42-)=2.06:1.其比值大于2的原因是硫酸層中含少量的HI,且HI電離出氫離子,
故答案為:硫酸層中含少量的HI,且HI電離出氫離子;
(3)①由圖可知,X越大,轉化率越低,升高溫度轉化率增大,則X表示壓強,
故答案為:壓強;
②由2SO3(g)=2SO2(g)+O2(g)△H>0,溫度高,轉化率大,圖中等壓強時L2對應的轉化率大,則L1<L2,
故答案為:L1<L2,分解反應為吸熱反應,溫度高,轉化率大.
點評 本題考查混合物分離提純及化學平衡等,為高頻考點,題目難度中等,把握發生的反應、平衡影響因素為解答的關鍵,側重分析與應用能力的綜合考查.


 千里馬走向假期期末仿真試卷寒假系列答案
千里馬走向假期期末仿真試卷寒假系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向NaHCO3溶液中加入過量的石灰水產生白色沉淀:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| B. | 向AgCl懸濁液中滴加Na2S溶液產生黑色沉淀:2AgCl(s)+S2-═Ag2S(s)+2Cl- | |
| C. | 石灰乳中Ca(OH)2的電離:Ca(OH)2(s)═Ca2++2OH- | |
| D. | Fe(OH)3膠體的制備:FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(膠體)+3HCl |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氧化性MnO4->Cl2>I2>Fe3+ | B. | 還原性:Fe2+>I->Cl- | ||
| C. | Fe3+能將I-氧化為I2 | D. | Fe2+只有還原性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NaOH和H2 | B. | Cu(OH)2、NaCl和H2 | C. | Cu和NaCl | D. | NaCl、Cu(OH)2和HCl |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 硫酸鐵的化學式為FeSO4 | |
| B. | 氧離子結構示意圖: | |
| C. | 碳酸氫鈉的電離方程式 NaHCO3═Na++HCO3- | |
| D. | 質量數為37的氯核素符號:${\;}_{37}^{17}$Cl |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①④⑥ | B. | ②③④ | C. | ②③⑤ | D. | ③④⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
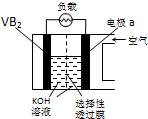 硼化釩(VB2)-空氣電池是目前儲電能力最高的電池,電池示意圖如圖所示,該電池工作時反應為:4VB2+11O2═4B2O3+2V2O5.下列說法正確的是( )
硼化釩(VB2)-空氣電池是目前儲電能力最高的電池,電池示意圖如圖所示,該電池工作時反應為:4VB2+11O2═4B2O3+2V2O5.下列說法正確的是( )| A. | 電極a為電池正極 | |
| B. | 圖中選擇性透過膜只能讓陽離子選擇性透過 | |
| C. | 電子由VB2極經KOH溶液流向a電極 | |
| D. | VB2極發生的電極反應為:2VB2+22OH--22e-═V2O5+2B2O3+11H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
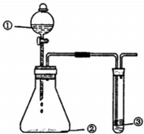 用如圖所示裝置進行下列實驗,有關分析一定不正確的是
用如圖所示裝置進行下列實驗,有關分析一定不正確的是| 選項 | ① | ② | ③ | 預期現象或結論 |
| A | 稀H2SO4 | Na2SO3 | 澄清石灰水 | 滴入少量稀H2SO4時③中立即出現渾濁 |
| B | H2O2溶液 | FeCl3 | FeCl2溶液 | FeCl3作催化劑 |
| C | 鹽酸 | KMnO4 | 淀粉KI溶液 | 氧化性:KMnO4>Cl2>I2 |
| D | 濃 HNO3 | Cu粉 | 石蕊溶液 | ③中可能先變后褪色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com