
【題目】高血脂是一種常見的心血管疾病,治療高血脂的新藥I的合成路線如下(A~I)均為有機物):

已知:a. 
b.  RCHO
RCHO
回答下列問題:
(1)反應①的化學方程式為_______;F的官能團名稱為______。
(2)反應②的類型是_______。D→E所需試劑、條件分別是_______、______。
(3)G的結構簡式為____________。
(4)芳香族化合物W的化學式為C8H8O2, 且滿足下列條件的W的結構共有_______種(不考慮立體異構)。
i.遇FeCl3溶液顯紫色; ii.能發(fā)生銀鏡反應。
其中核磁共振氫譜顯示有5種不司化學環(huán)境的氫,峰面積比為2:2:2:1:1的是____________(寫出結構簡式)。
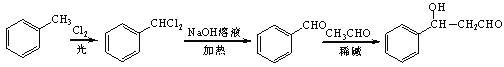
(5)設計以甲苯和乙醛為原料制備 的合成路線。無機試劑任選,合成路線的表示方式為:
的合成路線。無機試劑任選,合成路線的表示方式為:![]() _____________.
_____________.
【答案】![]() +Cl2
+Cl2![]()
![]() +HCl 醛基 取代反應(或酯化反應) NaOH溶液 加熱
+HCl 醛基 取代反應(或酯化反應) NaOH溶液 加熱 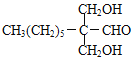 13
13 ![]()
【解析】
甲烷和氯氣在光照條件下發(fā)生取代反應生成D(CH2Cl2),D在氫氧化鈉的水溶液、加熱條件下發(fā)生取代反應,但同一個碳原子上含有兩個羥基不穩(wěn)定會失水生成醛,則E為HCHO,F是CH3(CH2)6CHO和甲醛反應生成G,根據(jù)題給信息知G為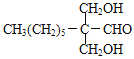 ,G和氫氣發(fā)生加成反應生成H為
,G和氫氣發(fā)生加成反應生成H為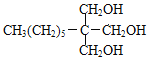 ;甲苯在光照條件下與氯氣發(fā)生取代反應生成
;甲苯在光照條件下與氯氣發(fā)生取代反應生成![]() ,水解得到A為
,水解得到A為![]() ,A氧化生成B為
,A氧化生成B為![]() ,B進一步氧化生成C為
,B進一步氧化生成C為![]() ,C與H發(fā)生酯化反應生成I為
,C與H發(fā)生酯化反應生成I為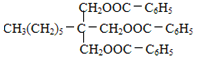 ;
;
(5)苯與氯氣在光照條件下生成![]() ,然后發(fā)生水解反應生成
,然后發(fā)生水解反應生成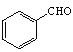 ,最后與乙醛在堿性條件下反應生成目標物。
,最后與乙醛在堿性條件下反應生成目標物。
根據(jù)上述分析可知:A為![]() ,B為
,B為![]() ,C為
,C為![]() ,D為CH2Cl2,E為HCHO,F為CH3(CH2)6CHO,G為
,D為CH2Cl2,E為HCHO,F為CH3(CH2)6CHO,G為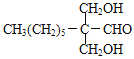 ,H為
,H為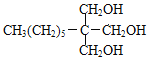 ,I為
,I為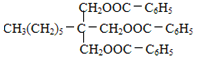 。
。
(1)反應①為甲苯和氯氣的取代反應,方程式為:![]() +Cl2
+Cl2![]()
![]() +HCl; F為CH3(CH2)6CHO ,官能團名稱為醛基;
+HCl; F為CH3(CH2)6CHO ,官能團名稱為醛基;
(2)反應②是C(![]() )與H(
)與H(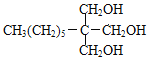 )發(fā)生酯化反應或取代反應產生I(
)發(fā)生酯化反應或取代反應產生I(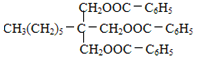 ),反應類型為酯化反應或取代反應;
),反應類型為酯化反應或取代反應;
D為CH2Cl2,E為HCHO,D與NaOH水溶液混合加熱發(fā)生取代反應產生E,所以D→E所需試劑、條件分別是NaOH溶液、加熱;
(3)G的結構簡式為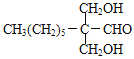 ;
;
(4)化合物W化學式為C8H8O2,W比C多一個-CH2原子團,且滿足下列條件,
①遇 FeCl3 溶液顯紫色,說明含有酚羥基、苯環(huán);
②能發(fā)生銀鏡反應,說明含有醛基,根據(jù)不飽和度知,除了苯環(huán)外不含雙鍵或環(huán)狀結構;
如果存在-OH、-CH2CHO,有鄰、間、對3種不同結構;
如果取代基為-OH、-CH3、-CHO,有10種不同結構;
所以符合條件的同分異構體有13種,其中核磁共振氫譜顯示有5種不同化學環(huán)境的氫,峰面積比為 2:2:2:1:1 的結構簡式為![]() ;
;
(5)苯與氯氣在光照條件下生成![]() ,
,![]() 發(fā)生水解反應生成
發(fā)生水解反應生成 ,
, 與CH3CHO發(fā)生醛的加成反應產生
與CH3CHO發(fā)生醛的加成反應產生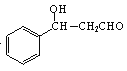 ,故合成路線流程圖為:
,故合成路線流程圖為: 。
。


 活力課時同步練習冊系列答案
活力課時同步練習冊系列答案科目:高中化學 來源: 題型:
【題目】某興趣小組以廢鐵屑制得硫酸亞鐵銨后,按下列流程制備二水合草酸亞鐵(FeC2O4·2H2O),進一步制備高純度還原鐵粉。
已知:FeC2O4·2H2O難溶于水,150℃開始失結晶水;常溫下H2C2O4為晶體,易溶于水,溶解度隨溫度升高而增大。

請回答:
(1)步驟②,發(fā)生反應的離子方程式____________________________;該步驟H2C2O4稍過量主要是為了_________________。
(2)下列操作或描述正確的是_______________。
A.步驟①,酸化主要是為了抑制Fe2+水解
B.步驟③,如果采用冷水洗滌可提高除雜效果
C.步驟③,如果在常壓下快速干燥,溫度可選擇略高于100℃
(3)稱取一定量的FeC2O4·2H2O試樣,用硫酸溶解,采用KMnO4滴定法測定,折算結果如下:
n(Fe2+)/mol | n(C2O42-)·mol-1 | 試樣中FeC2O4·2H2O的質量分數(shù) |
9.80×10-4 | 9.80×10-4 | 0.98 |
由表中數(shù)據(jù)推測試樣中最主要的雜質是_________________。
(4)實現(xiàn)步驟④必須用到的兩種儀器是_________(供選儀器如下)
a.坩堝;b.燒杯;c.蒸餾燒瓶;d.錐形瓶;e.表面皿:f.高溫爐
該步驟的化學方程式是______________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知AG=lg![]() ,電離度α=
,電離度α=![]() ×100%。常溫下,向10mL0.1mol/LHX溶液中滴加0.1mol/LNaOH溶液,混合溶液中AG與滴加NaOH溶液體積的關系如圖所示。
×100%。常溫下,向10mL0.1mol/LHX溶液中滴加0.1mol/LNaOH溶液,混合溶液中AG與滴加NaOH溶液體積的關系如圖所示。
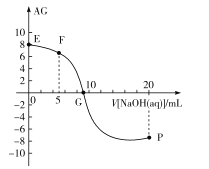
下列說法錯誤的是( )
A.F點溶液pH<7
B.G點溶液中c(Na+)=c(X-)>c(H+)=c(OH-)
C.V=10時,溶液中c(OH-)<c(HX)
D.常溫下,HX的電離度約為1%
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖表示物質A~F之間的轉化關系,其中A為淡黃色固體物質,B、C為無色溶液,D為氣體,E、F為白色沉淀。請?zhí)顚懴铝懈骺眨?/span>
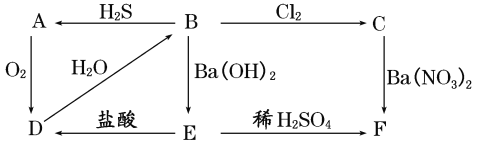
(1)寫出各物質的化學式:
A為______,B為_____,C為_____,D為_____,E為_____,F為______。
(2)寫出下列反應的化學方程式:
B→A:________________________。
B→C:___________________________。
(3)寫出C→F的離子方程式:___________________。
(4)在A~F六種物質中,既有氧化性又有還原性的是(填字母代號)______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CO、CO2是化石燃料燃燒后的主要產物。
(1)將體積比為2:1的CO2和CO混合氣體通入有足量Na2O2固體的密閉容器中,同時不斷地用電火花點燃。將殘留固體溶于水,所得溶液中2c(CO32-)+c(HCO3-)____________c(Na+)(填“>”“<”或“=”) 。
(2)已知:2CO(g)+O2(g)=2CO2(g) △H=-566.0 kJ/mol;鍵能E(o=o)=499.0 kJ/mol
①CO(g)+O2(g)![]() CO2(g)+O(g) 的△H=____________kJ/mol
CO2(g)+O(g) 的△H=____________kJ/mol
②已知2500K時,①中反應的平衡常數(shù)為0.40。某時刻該反應體系中各物質濃度滿足: c(CO)·c(O2)=c(CO2)·c(O),則此時反應____________(填向左”或“向右”)進行。
(3)已知:反應CO2(g)![]() CO(g)+O(g)在密閉容器中CO2分解實驗的結果如下圖1;反應2CO2(g)
CO(g)+O(g)在密閉容器中CO2分解實驗的結果如下圖1;反應2CO2(g)![]() 2CO(g)+O2(g)中1molCO2在不同溫度下的平衡分解量如下圖2,
2CO(g)+O2(g)中1molCO2在不同溫度下的平衡分解量如下圖2, 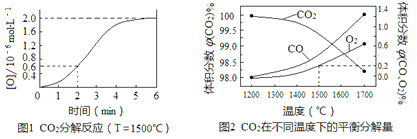
①分析圖1,求2min內v(CO2)=_______。
②分析圖2,1500℃時反應達平衡,此時容器體積為1 L,則反應的平衡常數(shù)K=______(計算結果保留1位小數(shù))。
(4)為探究不同催化劑對CO和H2合成CH3OH的選擇性效果,某實驗室控制CO和H2的初始投料比為1:3進行實驗,得到如下數(shù)據(jù):
選項 | T/K | 時間/min | 催化劑種類 | 甲醇的含量(%) |
A | 450 | 10 | CuO-ZnO | 78 |
B | 450 | 10 | CuO-ZnO-ZrO2 | 88 |
C | 450 | 10 | ZnO-ZrO2 | 46 |
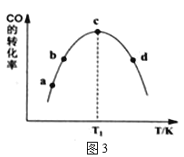
①由表1可知,該反應的最佳催化劑為____________(填編號);圖3中a、b、c、d四點是該溫度下CO的平衡轉化率的是____________。
②有利于提高CO轉化為CH3OH的平衡轉化率的措施有____________。
A. 使用催化劑CuO-ZnO-ZrO2 B. 適當降低反應溫度
C. 增大CO和H2的初始投料比 D. 恒容下,再充入a mol CO和3a mol H2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是室溫下,幾種弱酸的電離平衡常數(shù)(Ka)和弱堿的電離平衡常數(shù)(Kb):
酸或堿 | 電離常數(shù)(Ka或Kb) |
CH3COOH | Ka=1.75×10-5 |
檸檬酸(H3C6H5O7) | Ka1=7.4×10-4 Ka2=1.73×10-5 Ka3=4.0×10-7 |
NH3·H2O | Kb=1.75×10-5 |
請回答下列問題:
(1)用蒸餾水稀釋0.1 mol/L的醋酸溶液,下列選項中一定變小的是__________(填字母)。
A.![]()
B.c(H+)
C.c(OH-)·c(H+)
D.![]()
E.![]()
(2)濃度為0.10 mol/L檸檬酸氫二鈉(Na2HC6H5O7)溶液顯_____(填“酸”“堿”或“中”)性,通過計算說明其原因____
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)25°C時,若向a mol·L-1的HA溶液中,滴加等體積的b mol·L-1的NaOH溶液,使溶液呈中性,用含a的代數(shù)式表示HA的電離平衡常數(shù)Ka=____________。
(2)25°C時,將a mol·L-1的氨水與0.01 mol·L-1的鹽酸等體積混合,反應完后溶液中c(NH4+)=c(Cl-),則溶液顯_____性(填“酸”、“堿”或“中”),用含a的代數(shù)式表示NH3·H2O的電離平衡常數(shù)Kb=____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】回答下列關于N及其化合物的問題:
(1)配制Fe(NO3)2溶液時可否加入少量HNO3抑制Fe2+水解?_______,原因是__________________________________________。
(2)汽車尾氣中含有大量NO2,會導致環(huán)境污染,在汽車尾氣管裝上電化學轉化裝置在堿性水溶液環(huán)境中形成原電池,可部分解除NO2的污染,則該裝置的正極反應方程式為_________________________________;該裝置的負極原料為NH3,當電路中轉移8mole-時,負極消耗NH3的質量理論值約為________,(保留小數(shù)點后一位小數(shù))實際上消耗NH3的量遠大于該理論值的原因可能為_________________________________________。
(3)NaOH溶液也可解除NO2的污染,該反應的化學方程式為_____________________________。
(4)第(3)問反應可產生致癌物質NaNO2,該物質中N元素的化合價為_____價,酸性環(huán)境中的NaNO2可用H2O2氧化處理,處理過程的離子方程式為___________________,若改用O2來氧化,則68g的H2O2相當于O2的質量為____;(保留小數(shù)點后一位小數(shù))使用H2O2作為氧化劑的優(yōu)點是________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】若定義pc是溶液中微粒物質的量濃度的負對數(shù),則常溫下,一定濃度的某酸(H2A)水溶液中pc(H2A)、pc(HA-)、pc(A2-)隨著溶液pH的變化曲線如圖所示。下列說法一定正確的是( )
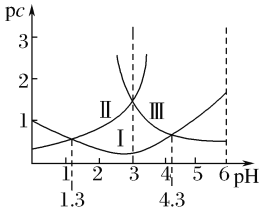
A.pH=4時,c(HA-)<c(A2-)
B.c(H2A)+c(HA-)+c(A2-)是定值
C.常溫下,該酸的電離常數(shù)Ka1=10-1.3
D.常溫下,NaHA的水溶液呈堿性
查看答案和解析>>
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com