
化學與社會、生產、生活密切相關。下列說法正確的是
A.光纖通信使用的光纜主要成分是Si,太陽能電池使用的材料主要是SiO2
B.視頻《穹頂之下》再次引起公眾對“PM2.5”的關注。“PM2.5”是指大氣中直徑小于或等于2.5×10—6m的細小顆粒物,這些顆粒擴散在空氣中形成膠體
C.醫用酒精是用淀粉類植物發酵經蒸餾制成,濃度通常是75%
D.油脂是人類維持生命活動所需能量的主要來源
科目:高中化學 來源:2017屆湖北省老河口市高三10月月考化學卷(解析版) 題型:選擇題
下列有關物質的分類或歸類中正確的是( )
①混合物:福爾馬林、水玻璃、水銀
②化合物:CaCl2、燒堿、聚苯乙烯、HD
③電解質:明礬、膽礬、冰醋酸、硫酸鋇
④同位素: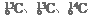
A.①③ B.②③ C.③④ D.②④
查看答案和解析>>
科目:高中化學 來源:2017屆福建省高三上聯考一化學卷(解析版) 題型:選擇題
X、Y、Z、W均為短周期元素,在周期表中位置如圖所示。Y原子的最外層電子數是電子層數的3倍。下列說法中不正確的是( )
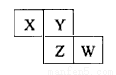
A. Y、Z的氣態氫化物,前者更穩定
B. Y、W的單質,均可通過電解的方法獲得
C. Z、W的最高價氧化物對應水化物的酸性,前者強
D. X、W的氣態氫化物相互反應,生成物中既含離子鍵又含共價鍵
查看答案和解析>>
科目:高中化學 來源:2017屆安徽省六校教育研究會高三上第一次聯考化學卷(解析版) 題型:選擇題
下列離子或分子組中,在相應的環境中一定能大量共存的是
選項 | 環境要求 | 離子或分子 |
A | A12(SO4)3溶液中 | K+、A1O2—、Cl—、NO3— |
B | 溶液pH>7 | Na+、SO32—、K+、S2— |
C | 水電離產生的c(OH—)=10—l2mol/L的溶液 | ClO—、CO32—、NH4+、K+ |
D | 氯氣中 | O2、NH3、CO2、HC1 |
查看答案和解析>>
科目:高中化學 來源:2017屆安徽省六校教育研究會高三上第一次聯考化學卷(解析版) 題型:選擇題
電解質在溶液中的行為是化學研究的重要內容。下列有關溶液的敘述不正確的是
A.加熱蒸干NaCl、MgCl2溶液時可以得到晶體NaCl、MgCl2
B.相同條件下,等物質的量濃度的溶液導電能力:HC1>NH3·H2O
C.溶液中離子結合質子(氫離子)的能力:C2O42—>HC2O4—>SO42—
D.海洋封存CO2會導致局部海洋水體酸性增強,會破壞海洋生態環境
查看答案和解析>>
科目:高中化學 來源:2017屆安徽省江淮十校高三11月質檢化學試卷(解析版) 題型:推斷題
X、Y、Z、W、M、N分別是原子序數依次遞增的短周期主族元素,其中X與W同族且可形成離子化合物P,Z與M同族且可形成兩種化合物,其中一種是大氣污染氣體Q,Y組成的單質是大氣主要成份。
(1)元素N位于周期表中的位置 。
(2)實驗室制取Y元素的最簡單氫化物的化學方程式為 。
(3)有X、Z、W、M共同參與形成的兩種化合物之間的反應離子方程式 。
(4)將N的單質通入含等物質的量FeBr2的溶液中,發生反應的離子方程式為 。
(5)P在D2O反應的化學方程式為 。
(6)將Q通入BaCl2溶液中是否產生現象(填“是”或“否”),若再通入N的單質對應的離子方程式為 。
查看答案和解析>>
科目:高中化學 來源:2017屆安徽省江淮十校高三11月質檢化學試卷(解析版) 題型:選擇題
除去下列物質中所含的雜質(括號內為雜質),選用試劑及操作正確的是
A.Al2O3(SiO2):NaOH溶液,過濾
B.CO2(SO2):飽和的Na2CO3溶液,洗氣
C.FeCl2溶液(FeCl3):Fe粉,過濾
D.NaHCO3溶液(Na2CO3):Ca(OH)2溶液,過濾
查看答案和解析>>
科目:高中化學 來源:2016-2017學年四川省高一11月月考化學卷(解析版) 題型:選擇題
已知常溫下,在溶液中發生如下反應:
①16H++10Z-+2XO4-=2X2++5Z2+8H2O
②2A2++B2===2A3++2B-
③2B-+Z2===B2+2Z
由此推斷下列說法錯誤的是( )
A.反應Z2+2A2+=2A3++2Z-可以進行
B.Z元素在反應③中被還原,在反應①中被氧化
C.氧化性由強到弱的順序是XO4-、Z2、B2、A3+
D.Z2可以置換出X2+溶液中的X
查看答案和解析>>
科目:高中化學 來源:2017屆陜西省高三上學期第三次質檢化學試卷(解析版) 題型:填空題
磷及其化合物在生產、生活中有重要的用途。回答下列問題:
(1)直鏈聚磷酸是由n個磷酸分子通過分子間脫水形成的,常用于制取阻燃劑聚磷酸銨。
①寫出磷酸主要的電離方程式 。
②直鏈低聚磷酸銨的化學式可表示為(NH4)(n+2)PnOx,x= (用n表示)。
(2)在堿性條件下,次磷酸鹽可用于化學鍍銀,完成其反應的離子方程式。
□H2PO2-+□Ag+ + □ = □PO4 3-+ □Ag +□
3-+ □Ag +□
(3)由工業白磷(含少量砷、鐵、鎂等)制備高純白磷(熔點44℃,沸點280℃),主要生產流程如下
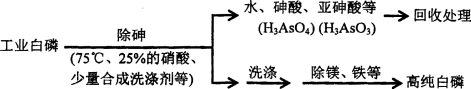
①除砷過程在75℃下進行,其合理的原因是_______(填字母)。
a.溫度不宜過高,防止硝酸分解 b.適當提高溫度,加快化學反應速率
c.使白磷熔化,并溶于水 d.降低白磷的毒性
②硝酸氧化除砷時被還原為NO,若氧化產物為等物質的量的亞砷酸與砷酸,則化學反應方程式為_______________
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com