
【題目】某研究性學習小組向一定量的NaHSO3溶液(加入少量淀粉)中加入稍過量的KIO3 溶液,一段時![]() 間后,溶液突然變藍色。為進一步研究有關因素對反應速率的影響,探究如下。
間后,溶液突然變藍色。為進一步研究有關因素對反應速率的影響,探究如下。
(1)查閱資料 知NaHSO3與過量KIO3反應分為兩步進行,且其反應速率主要由第一步反應決定。已知第一步反應的離子方程式為IO3—+3HSO3—===3SO42—+I—+3H+,則第二步反應的離子方程式為________________。
(2)通過測定溶液變藍所用時間來探究外界條件對該反應速率的影響,記錄如下。
編號 | 0.01mol/LNaHSO3溶液/mL | 0.01mol/L KIO3 溶液/mL | H2O/mL | 反應溫度 /℃ | 溶液變藍所用時間t/s |
① | 6.0 | 10.0 | 4.0 | 15 | t1 |
② | 6.0 | 14.0 | 0 | 15 | t2 |
③ | 6.0 | a | b | 25 | t3 |
實驗①②是探究_______________對反應速率的影響,表中t1___________t2(填“>”、“=”或“<”);
實驗①③是探究溫度對反應速率的影響,表中a=_____________,b=_____________。、
(3)將NaHSO3溶液與KIO3溶液在恒溫條件下混合,用速率檢測儀檢測出起始階段反應速率 逐漸增大。該小組對其原因提出如下假設,請你完成假設二。
假設一:生成的SO42—對反應起催化作用;
假設二:___________________________;……
(4)請你設計實驗驗證上述假設一,完成下表中內容。
實驗步驟(不要求寫出具體操作過程) | 預期實驗現象和結論 |
在燒杯甲中將一定量的NaHSO3溶液與KIO3溶液混合,用速率檢測儀測定起始時的反應速率v(甲) 在燒杯乙中先加入少量①_____,其他條件與甲完全相同,用速率檢測儀測定起始時的反應速率v(乙) | ②若v(甲)___v(乙),則假設一不成立 ③若v(甲)___v(乙),則假設一成立 (填“>”、“=”或“<”) |
【答案】(1)IO3—+5I—+6H+=3I2+3H2O;
(2)KIO3溶液的濃度,> ,10.0,4.0;
(3)生成的I—或H+對反應起催化作用;
(4)①Na2SO4粉末;②=;③< 。
【解析】
試題分析:(1)(1)根據信息,溶液變藍,說明產生I2,離子反應方程式為:IO3-+5I-+6H+=3I2+3H2O;(2)探究影響反應速率的因素,要求其他條件不變,通過①②對比,KIO3濃度不同,因此實驗探究KIO3溶液的濃度對反應速率的影響,濃度越高,反應速率越快,即t1>t2,a=10.0,b=4.0;(3)生成的I-或H+對反應起催化作用;(4)①研究SO42-做催化劑,因此①中加入Na2SO4粉末;②當反應速率相等,假設一不相等,若v(甲)<v(乙),假設一成立。


 全優點練單元計劃系列答案
全優點練單元計劃系列答案科目:高中化學 來源: 題型:
【題目】下列溶液中微粒的物質的量濃度關系正確的是( )
A. 濃度均為0.1 mol·L-1的氨水和鹽酸等體積混合后:c(H+)=c(OH-)+c(NH3·H2O)
B. 等濃度的碳酸鈉、碳酸氫鈉溶液混合后:c(CO![]() )<c(HCO
)<c(HCO![]() )
)
C. 在NaHB溶液中一定有:c(Na+)=c(HB-)+2c(B2-)
D. Na2CO3溶液中:2c(Na+)=c(CO![]() )+c(HCO
)+c(HCO![]() )+c(H2CO3)
)+c(H2CO3)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】溶液中的化學反應大多是離子反應。根據要求回答下列問題:
(1)鹽堿地(含較多Na2CO3、NaCl)不利于植物生長,試用化學方程式表示:
鹽堿地產生堿性的原因:__________________________________________;
(2)已知水存在如下平衡:H2O+H2O![]() H3O++OH-,向水中加入NaHSO4固體,水的電離平衡向________移動,且所得溶液顯________性。
H3O++OH-,向水中加入NaHSO4固體,水的電離平衡向________移動,且所得溶液顯________性。
(3)若取pH、體積均相等的NaOH溶液和氨水分別用水稀釋m倍、n倍,稀釋后pH仍相等,則m________(填“>”“<”或“=”)n。
(4)常溫下,在pH=6的CH3COOH與CH3COONa的混合溶液中水電離出來的c(OH-)=________。
(5)已知:常溫下,醋酸和NH3·H2O的電離平衡常數均為1.74×10-5;則 NH4HCO3溶液呈________性,NH4HCO3溶液中物質的量濃度最大的離子是________(填化學式)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在Cl2 + SO2 + 2H2O = 2HCl + H2SO4的反應中:
(1)氧化劑是______________,還原劑是__________________,
(2)若反應消耗7.1g Cl2,同時消耗標準狀況下SO2的體積約為____________L,反應生成H2SO4物質的量是___________mol。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】室溫下,用相同濃度的NaOH 溶液,分別滴定100mL濃度均為0.1mol·L-1 的三種酸(HM、HN和HR) 溶液,滴定的曲線如圖所示,下列判斷錯誤的是( )
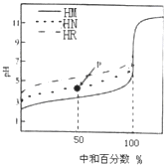
A. 三種酸的電離常數關系: KHR>KHN>KHM
B. pH=7時,三種溶液中:c (M-) >c (N-)>c (R-)
C. 滴定至P點時,溶液中:c (Na+) >c (N-) >c (HN) >c (H+) >c (OH-)
D. 當中和百分數達100%時,將三種溶液混合后:c(HM)+c(HN)+c(HR) =c(OH-)-c(H+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】燃煤煙氣中含有大量SO2和NO。某科研小組研究臭氧氧化-堿吸收法同時脫除SO2和NO工藝,氧化過程反應原理及反應熱、浯化能數據如下:
反應I: NO(g)+O3(g) ![]() NO2(g)+ O2(g) △H1=-200.9kJ/mol' Ea1=3.2 kJ/mol.
NO2(g)+ O2(g) △H1=-200.9kJ/mol' Ea1=3.2 kJ/mol.
反應Ⅱ:SO2(g))+ O3(g)![]() SO3(g)+O2(g) △H2=-241.6kJ/mol Ea2= 58 kJ/mol
SO3(g)+O2(g) △H2=-241.6kJ/mol Ea2= 58 kJ/mol
已知該體系中溫度80℃以上臭氧發生分解反應:2O3(g) ![]() 3O2(g) 請回答:
3O2(g) 請回答:
(1)已知反應I在低溫下自發進行,則該反應的熵變△S___________0(填“大于”或“小于”)。
(2)其它條件不變,每次向反應器中充入含1.0 mol NO、10 mol SO2的模擬煙氣和2.0 molO3,改變溫度,反應相同時間后體系中NO和SO2的轉化率如圖所示:
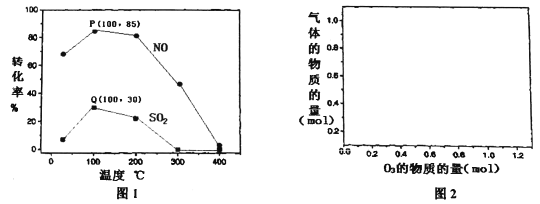
①由圖1可知相同溫度下NO的轉化率遠高于SO2,結合題中數據分析其可能原因_________。
②100℃、反應相同時間t時O3的分解率達10%,則體系中剩余O3的物質的量是______mol。
③下列說法正確的是_______。
A.P點一定為平衡狀態點
B.溫度高于200℃后,NO和SO2的轉化率隨溫度升高顯著下降、最后幾乎為零
C.其它條件不變,若縮小反應器的容積可提高NO和SO2的轉化率
D.臭氧氧化過程不能有效地脫除SO2,但后續步驟堿吸收可以有效脫硫
(3)150℃條件下,向反應器中充入含1molNO、1molSO2的模擬煙氣,在圖2中分別畫出NO和SO2的物質的量隨O3量的變化曲線。________
(4)工業上可以通過電解NO制備NH4NO3,原理如圖3所示。寫出電解過程陽極的電極反應式_______。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】1.15 g金屬鈉跟水反應后,得到100 mL溶液,試計算:
生成的氣體在標準狀況下是多少毫升?
_________________
反應后所得溶液的物質的量濃度是多少?
_________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有A、B兩種烴,含碳的質量分數相同,關于A,B的敘述中正確的是
A.A和B一定是同分異構體
B.A和B不可能是同系物
C.A和B的最簡式一定相同
D.A和B各1mol完全燃燒后生成CO2的質量一定相同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是( )
A.Na2CO3 比NaHCO3 的溶解度大
B.Na2CO3 比NaHCO3 穩定
C.物質的量相等的Na2CO3 和NaHCO3 , 前者質量大
D.物質的量相等的Na2CO3 和NaHCO3分別與足量鹽酸反應得CO2 的物質的量之比為2:1
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com