
【題目】下列氧化還原反應方程式,所標電子轉移方向與數目錯誤的是( )

A. A B. B C. C D. D
科目:高中化學 來源: 題型:
【題目】實驗室里需要純凈的NaCl溶液,但手邊只有混有Na2SO4、NH4HCO3的NaCl。某學生設計了如圖所示方案提取純凈的NaCl溶液。(已知:NH4HCO3=NH3↑+CO2↑+H2O)

(1)操作②為什么不用硝酸鋇溶液,其理由是_______________________________;
(2)進行操作②后,如何判斷SO42-已除盡,方法是___________________________;
(3)操作③的目的是____________,其中涉及到的離子方程式是_______________;
(4)往濾液中加入鹽酸的離子方程式是__________________________________;
(5)NH4HCO3在水溶液中的電離方程式_________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)鋼鐵腐蝕主要是吸氧腐蝕,該腐蝕過程中的電極反應式為__________、_______。
(2)用甲烷制取氫氣的兩步反應的能量變化如下圖所示:

甲烷和水蒸氣反應生成二氧化碳和氫氣的熱化學方程式是________________。
(3)以CO2與NH3為原料可合成化肥尿素[化學式為CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) △H=-159.5KJ/mol
②NH2CO2NH4(s)= CO(NH2)2(s) +H2O(g) △H=+116.5KJ/mol
③H2O(l)=H2O(g) △H=+44KJ/mol
寫出CO2與NH3合成尿素和液態水的熱化學方程式__________________。
(4)氨氣在純氧中燃燒,生成一種單質和水。科學家利用此原理,設計成氨氣-氧氣燃料電池,則通入氨氣的電極在堿性條件下發生反應的電極反應式為_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯化亞銅是重要的銅鹽系列化工產品,廣泛應用于石油化工、有機合成等行業。CuCl晶體呈白色,微溶于水,不溶于稀鹽酸和乙醇,露置于潮濕空氣中易水解氧化為綠色的[Cu 2(OH)3C1],見光易分解。某研究小組以CuCl2(含少量Fe2+)粗品為原料制取CuCl,設計的合成路線如下:

己知:①在較高的鹽酸濃度下,Fe3+能溶解于甲基異丁基甲酮。
②CuCl在溶液中存在:CuCl(s)+2Cl-(aq)![]() [CuCl3]2-(aq)。
[CuCl3]2-(aq)。
請回答:
(1)下列敘述正確的是__________。
A.CuCl2原料中含有的Fe2+等雜質經氧化、萃取幾乎都在有機相中被除去
B.加入萃取劑后,混合物轉移至分液漏斗中,塞上玻璃塞,如圖用力振搖![]()
C.經幾次振搖并放氣后,手持分液漏斗靜置待液體分層
D.用濃鹽酸洗滌分液后的有機相時,需在分液漏斗中進行
(2)上述合成路線中,SO2通入混合液的實驗裝置如下圖所示:

①裝置D的作用是_______________。
②C中反應的離子方程式為_____________。
(3)上述合成路線中,向混合液中加入大量去氧水的目的是________________。
(4)上述合成路線中,一系列操作包括:抽濾、洗滌、干燥。干燥時應注意密封、____________。
(5)現稱取l.200g產品,用硫酸酸化的硫酸鐵溶解,并稀釋成250mL。每次用移液管移取25.00mL溶液于錐形瓶中,用0.01000,mol·L-1KmnO4溶液滴定平均消耗24.00mL。
①用移液管吸取25.00mL溶液后,把溶液轉移到錐形瓶中的具體操作為____________。
②產品中CuCl的純度為__________(本實驗條件下,Cl-難于被MnO4-氧化)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2SO2(g) +O2(g)=2SO3(g)反應過程的能量變化如圖所示。已知1mol SO2(g)氧化為1mol SO3(g)的△H=-99KJ/mol。請回答下列問題:
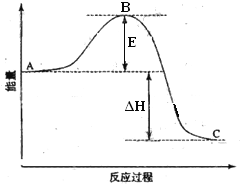
①圖中A、C分別表示________、_______;
②E表示________;E的大小對該反應的反應熱____(填“有”或“無”)影響。
③該反應通常用V2O5作催化劑,加V2O5會使圖△H______(填“變大”、“變小”或“不變”),圖中△H =______KJ/mol;
④已知單質硫的燃燒熱為296 KJ/mol,計算由S(s)生成3molSO3(g)的△H=________KJ/mol。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】兩串聯電解池,左邊放硫酸銅,右邊放一定量的某硝酸鹽溶液,電解時當左池有1.6g Cu析出時,右池析出0.45g固體,則右池溶質為:
A.AgNO3 B.NaNO3 C.Mg(NO3)2 D.Al(NO3)3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一密閉容器中加入A和B,各物質的物質的量濃度隨著反應的進行,如右圖所示。下列說法不正確的是

A. 該反應的化學方程式為5A+4B![]() 4C
4C
B. 2min前,正反應速率逐漸減小,逆反應速率逐漸增大
C. 用B的濃度變化表示2min內的速率為2mol/(L·min)
D. 2min時,該反應達到平衡,此時A、B、C的濃度比為5:4:4
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com