
隨著世界糧食需求量的增加,農業對化學肥料的需求越越大。氮肥是需求最大的一種化肥。氮肥的生產和合理施用在農業生產中起著重大作用。合成氨及化肥生產流程示意圖如下:

(1)目前,工業上用鐵觸媒作催化劑,在20~50 MPa、450℃左右用氮、氫混合氣體在
中進行合成氨。則沿X方向回去的物質是 。
(2)在侯氏制堿法中,從沉淀池中得到的母液要通人氨氣、降溫并加入 (填化學式),目的是 。
(3)沉淀池中的化學方程式是 。
(4)工業上將氨催化氧化可制硝酸。在硝酸生產中,催化劑鉑網在氨的催化氧化反應中起的作 用是 。硝酸工業尾氣對環境污染嚴重,若在催化劑存在下用甲烷將其中的一氧化氮還原為對空氣無污染的物質,其反應的化學方程式為 。
(1)(2分)合成塔(1分);H2、N2(1分)
(2)(2分)NaCl (1分);使氯化銨逐步從母液中結晶析出(1分)
(3)(2分)NH3 + CO2 + H2O +NaCl = NH4Cl + NaHCO3↓
(4)(2分)加快反應速率同時決定了氧化產物是一氧化氮(1分);
CH4 + 4NO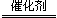 2N2 + CO2 + 2H2O (1分)
2N2 + CO2 + 2H2O (1分)
【解析】
試題分析:(1)氮氣和氫氣的反應在合成塔中進行,因為合成氨反應為可逆反應,反應后化合物中含有一定量的的氮氣和氫氣 ,分離后再作為原料進行循環利用。
(2)加入氯化鈉,利用同離子效應,降低氯化銨的溶解度,使氯化銨結晶析出。
(3)根據流程圖和題目所給信息,可知反應物有NH3 、CO2 、H2O、NaCl,產物為NH4Cl 和 NaHCO3,進而可寫出化學方程式。
(4)催化劑的作用為加快化學反應速率,同時生成NO;根據化合價的變化,甲烷將其中的一氧化氮還原為對空氣無污染的物質,生成N2、CO2、H2O ,配平可得化學方程式。
考點:本題考查化學工藝流程、化學方程式的書寫及催化劑的作用。


科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源:2011-2012學年浙江省寧波市八校高一下學期期末聯考化學試卷(帶解析) 題型:填空題
(5分)隨著世界糧食需求量的增長,農業對化學肥料的需求量越來越大,其中氮肥是需求量最大的一種化肥。而氨的合成為氮肥的生產工業奠定了基礎,其原理為:N2+3H2 2NH3
2NH3
(1)在N2+3H2 2NH3的反應中,一段時間后,NH3的濃度增加了0.9mol·L-1。用N2表示其反應速率為0.15 mol·L-1·s-1,則所經過的時間為 ;
2NH3的反應中,一段時間后,NH3的濃度增加了0.9mol·L-1。用N2表示其反應速率為0.15 mol·L-1·s-1,則所經過的時間為 ;
A.2 s B.3 s C.4 s D.6 s
(2)下列4個數據是在不同條件下測得的合成氨反應的速率,其中反應最快的是 ;
A.v(H2)=0.1 mol·L-1·min-1 B.v(N2)=0.1 mol·L-1·min-1
C.v(NH3)=0.15 mol·L-1·min-1 D.v(N2)=0.002mol·L-1·min-1
(3)在一個絕熱、容積不變的密閉容器中發生可逆反應:N2(g)+3H2(g) 2NH3(g) △H<0。下列各項能說明該反應已經達到平衡狀態的是 。
2NH3(g) △H<0。下列各項能說明該反應已經達到平衡狀態的是 。
A.容器內氣體密度保持不變
B.容器內溫度不再變化
C.斷裂1mol N≡N鍵的同時,斷裂6 mol N—H鍵
D.反應消耗N2、H2與產生NH3的速率之比1︰3︰2
查看答案和解析>>
科目:高中化學 來源:2011-2012學年內蒙古巴市一中高一下學期期末考試化學試卷(帶解析) 題型:填空題
(6分)隨著世界糧食需求量的增長,農業對化學肥料的需求量越來越大,其中氮肥是需求量最大的一種化肥。而氨的合成為氮肥的生產工業奠定了基礎,其原理為:N2+3H2 2NH3
2NH3
(1)在N2+3H2 2NH3的反應中,一段時間后,NH3的濃度增加了0.9mol·L-1。用N2表示其反應速率為0.15 mol·L-1·s-1,則所經過的時間為 ;
2NH3的反應中,一段時間后,NH3的濃度增加了0.9mol·L-1。用N2表示其反應速率為0.15 mol·L-1·s-1,則所經過的時間為 ;
A.2 s B.3 s C.4 s D.6 s
(2)下列4個數據是在不同條件下測得的合成氨反應的速率,其中反應最快的是 ;
A.v(H2)=0.1 mol·L-1·min-1 B.v(N2)=0.1 mol·L-1·min-1
C.v(NH3)=0.15 mol·L-1·min- D.v(N2)=0.002mol·L-1·min-1
(3)在一個絕熱、容積不變的密閉容器中發生可逆反應:
N2(g)+3H2(g) 2NH3(g) △H<0。下列各項能說明該反應已經達到平衡狀態的是 。
2NH3(g) △H<0。下列各項能說明該反應已經達到平衡狀態的是 。
A.容器內氣體密度保持不變
B.容器內溫度不再變化
C.斷裂1mol N≡N鍵的同時,斷裂6 mol N—H鍵
D.反應消耗N2、H2與產生NH3的速率之比1︰3︰2
查看答案和解析>>
科目:高中化學 來源:2014屆浙江省寧波市八校高一下學期期末聯考化學試卷(解析版) 題型:填空題
(5分)隨著世界糧食需求量的增長,農業對化學肥料的需求量越來越大,其中氮肥是需求量最大的一種化肥。而氨的合成為氮肥的生產工業奠定了基礎,其原理為:N2+3H2 2NH3
2NH3
(1)在N2+3H2 2NH3的反應中,一段時間后,NH3的濃度增加了0.9mol·L-1。用N2表示其反應速率為0.15 mol·L-1·s-1,則所經過的時間為
;
2NH3的反應中,一段時間后,NH3的濃度增加了0.9mol·L-1。用N2表示其反應速率為0.15 mol·L-1·s-1,則所經過的時間為
;
A.2 s B.3 s C.4 s D.6 s
(2)下列4個數據是在不同條件下測得的合成氨反應的速率,其中反應最快的是 ;
A.v(H2)=0.1 mol·L-1·min-1 B.v(N2)=0.1 mol·L-1·min-1
C.v(NH3)=0.15 mol·L-1·min-1 D.v(N2)=0.002mol·L-1·min-1
(3)在一個絕熱、容積不變的密閉容器中發生可逆反應:N2(g)+3H2(g) 2NH3(g) △H<0。下列各項能說明該反應已經達到平衡狀態的是
。
2NH3(g) △H<0。下列各項能說明該反應已經達到平衡狀態的是
。
A.容器內氣體密度保持不變
B.容器內溫度不再變化
C.斷裂1mol N≡N鍵的同時,斷裂6 mol N—H鍵
D.反應消耗N2、H2與產生NH3的速率之比1︰3︰2
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com