
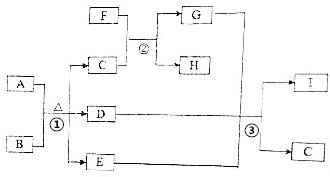
 有關物質(zhì)的轉(zhuǎn)化關系如圖所示(部分生成物與反應條件己略去).A是常見的非金屬固體單質(zhì),F(xiàn)是紫紅色的金屬單質(zhì),B、C是常見的強酸,D、G、I是常見的氣體,D與I的組成元素相同,且D的相對分子質(zhì)量比I的大16.E是最常見的無色液體.請回答下列問題:
有關物質(zhì)的轉(zhuǎn)化關系如圖所示(部分生成物與反應條件己略去).A是常見的非金屬固體單質(zhì),F(xiàn)是紫紅色的金屬單質(zhì),B、C是常見的強酸,D、G、I是常見的氣體,D與I的組成元素相同,且D的相對分子質(zhì)量比I的大16.E是最常見的無色液體.請回答下列問題: .
.分析 F是紫紅色的金屬單質(zhì),則F為Cu;B、C是常見的強酸,非金屬固體單質(zhì)與B反應得到C,且C能與Cu反應,可知A為S,B為HNO3,C為H2SO4,E為H2O,而G、D、E反應得到C,D的相對分子質(zhì)量比I的大16,則D為NO2,G為SO2,I為NO,H為CuSO4,符合轉(zhuǎn)化關系,據(jù)此解答.
解答 解:F是紫紅色的金屬單質(zhì),則F為Cu;B、C是常見的強酸,非金屬固體單質(zhì)與B反應得到C,且C能與Cu反應,可知A為S,B為HNO3,C為H2SO4,E為H2O,而G、D、E反應得到C,D的相對分子質(zhì)量比I的大16,則D為NO2,G為SO2,I為NO,H為CuSO4,符合轉(zhuǎn)化關系.
(1)E為H2O,電子式為 ,故答案為:
,故答案為: ;
;
(2)H的化學式為:CuSO4,故答案為:CuSO4;
(3)反應①的化學方程式:S+6HNO3(濃)$\frac{\underline{\;\;△\;\;}}{\;}$H2SO4+6NO2↑+2H2O,
故答案為:S+6HNO3(濃)$\frac{\underline{\;\;△\;\;}}{\;}$H2SO4+6NO2↑+2H2O;
(4)反應②的離子方程式:Cu+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$Cu2++SO42-+SO2↑+2H2O,
反應③的離子方程式:NO2+SO2+H2O=2H++SO42-+NO,
故答案為:Cu+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$Cu2++SO42-+SO2↑+2H2O;NO2+SO2+H2O=2H++SO42-+NO.
點評 本題考查無機物推斷,B、C為強酸為推斷突破口,需要學生熟練掌握元素化合物性質(zhì),難度中等.


 陽光課堂課時作業(yè)系列答案
陽光課堂課時作業(yè)系列答案科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 360 kJ/mol | B. | 263 kJ/mol | C. | 1 173 kJ/mol | D. | 391 kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 完全燃燒生成二氧化碳和水的化合物不一定是烴 | |
| B. | 相同質(zhì)量的正丁烷和異丁烷分別完全燃燒,耗氧量相等 | |
| C. | 相同物質(zhì)的量乙烯和乙醇分別完全燃燒,耗氧量相等 | |
| D. | 相同質(zhì)量的乙烷和乙炔分別完全燃燒,耗氧量相等 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. |  | B. | 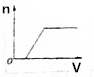 | C. | 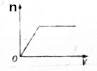 | D. |  |
查看答案和解析>>
科目:高中化學 來源:2016-2017學年浙江省高一上10月月考化學試卷(解析版) 題型:實驗題

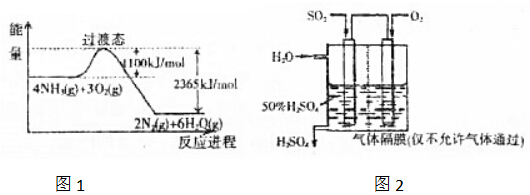
(1)該硫酸的物質(zhì)的量濃度是________mol/L。
(2)某化學興趣小組進行硫酸性質(zhì)的實驗探究時,需要490 mL 4.6 mol/L的稀硫酸,則需要取________mL的該硫酸。
(3)配制時,所需的玻璃儀器除量筒、燒杯、玻璃棒和膠頭滴管之外,還需要 (填儀器名稱);
(4)配制溶液有如下(未按順序排列):a.溶解,b.搖勻,c.洗滌,d.冷卻,e.稱量,f.將溶液移至容量瓶,g.定容等操作。 其中搖勻的前一步操作是 ;(填寫字母)
(5)在下列配制過程示意圖中,有錯誤的是(填寫序號) 。

(6)在配制4.6 mol/L的稀硫酸的過程中,下列情況會引起硫酸溶液物質(zhì)的量濃度偏高的是_________
A.未經(jīng)冷卻趁熱將溶液注入容量瓶中 | B.容量瓶洗滌后,未經(jīng)干燥處理 |
C.定容時仰視觀察液面 | D.未洗滌燒杯和玻璃棒 |
查看答案和解析>>
科目:高中化學 來源:2016-2017學年浙江省高一上10月月考化學試卷(解析版) 題型:選擇題
下列四種化學實驗操作名稱從左到右分別是
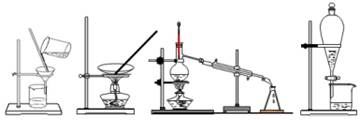
A. 過濾、蒸發(fā)、蒸餾、萃取 B. 過濾、蒸餾、蒸發(fā)、萃取
C. 蒸發(fā)、蒸餾、過濾、萃取 D. 萃取、蒸餾、蒸發(fā)、過濾
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com