
 托盤天平、容量瓶、量筒是常見的中學化學計量儀器,熟知這些儀器的使用是定量研究化學的基礎.
托盤天平、容量瓶、量筒是常見的中學化學計量儀器,熟知這些儀器的使用是定量研究化學的基礎.分析 (1)具有刻度的儀器在規定溫度下使用;
(2)容量瓶作為精密儀器,是用來配置一定物質的量濃度的溶液的主要儀器,不可用于儲存和溶解、稀釋物質,也不能測量除其規格以外容積的液體體積;
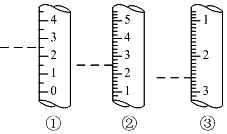
(3)量筒沒有0刻度,小數在下大數在上,精確值為0.1ml;滴定管0刻度在上,小數在上大數在下,精確值為0.01ml;
(4)配制 (濃硫酸的密度為1.84g/mL)450mL 0.1mol•L-1的硫酸,選擇500mL容量瓶,結合c=$\frac{1000ρw}{M}$及配制前后溶質的物質的量不變計算;量筒需要干燥、且不需要將量筒中洗滌液轉移到容量瓶中.
解答 解:(1)液體的體積受溫度的影響較大,使用時應在規定的溫度下測出的體積才準確,量筒、容量瓶中的液體的體積不同,導致產生誤差,
故答案為:容量瓶、量筒;
(2)容量瓶作為精密儀器,是用來配置一定物質的量濃度的溶液的主要儀器,不可用于儲存和溶解、稀釋物質,也不能測量除其規格以外容積的液體體積,所以
容量瓶不具備的功能有:BCEF;
故答案為:BCEF;
(3)從圖中給出儀器的刻度特點,可知②為量筒,讀數為2.6mL;③為滴定管,讀數為2.50mL;
故答案為:②;2.6;
(4)配制中應選用500mL的容量瓶,由0.5L×0.1mol/L=V×$\frac{1000×1.84×98%}{98}$,解得V=2.7mL,應量取2.97mL 98%的濃硫酸,
故答案為:500mL; 2.7;
②量筒在使用前已洗干凈但不干燥,量取硫酸的濃度偏低,對結果是造成影響,某同學認為將量筒內的濃硫酸倒出之后,不需要將量筒洗滌、轉移到容量瓶中,做法錯,故答案為:是; 錯.
點評 本題考查配制一定濃度的溶液,為高頻考點,把握配制溶液的儀器、步驟、操作為解答的關鍵,側重分析與實驗能力的考查,注意容量瓶的選擇及使用,題目難度不大.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 聚乙烯、植物油都是混合物,都能使溴的四氯化碳溶液褪色 | |
| B. | 向氯乙烷中加入硝酸銀溶液,可以快速鑒定其中的氯原子 | |
| C. | 將等體積的苯、汽油和水在試管中充分振蕩后靜置,現象如圖 | |
| D. | 直餾汽油和裂化汽油中分別滴加溴水可以觀察到不同現象 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 ”和“
”和“ ”分別表示不同的原子.下列對此反應的分類一定不正確的是( )
”分別表示不同的原子.下列對此反應的分類一定不正確的是( )
| A. | 化合反應 | B. | 可逆反應 | C. | 置換反應 | D. | 氧化還原反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 過濾操作中,漏斗下端要緊靠燒杯內壁,而分液操作中,無此要求 | |
| B. | 蒸餾操作時,應使溫度計水銀球插入蒸餾燒瓶的溶液中 | |
| C. | 蒸發操作時,應用玻璃棒不斷攪拌待有大量晶體出現,停止攪拌,繼續把水份蒸干 | |
| D. | 分液操作時,分液漏斗中下層液體從下口放出,上層液體從上口倒出 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
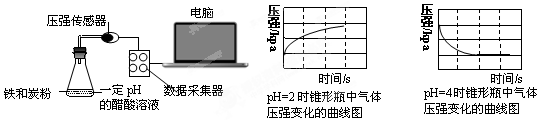
| A. | 溶液pH≤2時,生鐵發生析氫腐蝕 | |
| B. | 生鐵的腐蝕中化學腐蝕比電化學腐蝕更普遍 | |
| C. | 在酸性溶液中生鐵可能發生吸氧腐蝕 | |
| D. | 兩溶液中負極反應均為:Fe-2e-═Fe2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
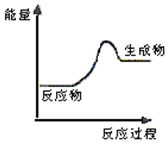
| A. | 該反應可能為吸熱反應 | |
| B. | 該反應一定有能量轉化成了生成物的化學能 | |
| C. | 反應物比生成物穩定 | |
| D. | 生成物的總能量高于反應物的總能量,反應不需要加熱 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 同主族元素形成的單質熔沸點自上而下逐漸升高 | |
| B. | 核外電子排布相同的微粒化學性質一定相同 | |
| C. | 同主族元素最高價含氧酸的酸性隨核電荷數的增加而減弱 | |
| D. | 非金屬元素的氣態氫化物的穩定性越強其沸點就越高 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
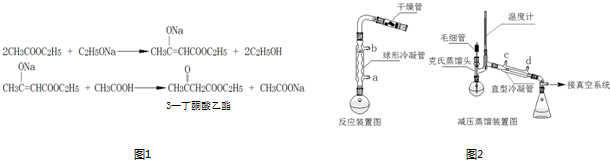
 CH3COOCH2CH3+H2O,反應類型是酯化反應.
CH3COOCH2CH3+H2O,反應類型是酯化反應.查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 平衡常數K增大 | B. | a+b<c+d | C. | X的轉化率下降 | D. | Z的體積分數增加 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com