
【題目】實驗室以有機物A、E為原料,制備聚酯纖維M和藥物中間體N的一種合成路線如下:

已知:①A的核磁共振氫譜有3組吸收峰
②
③
請回答下列問題:
(1)A的化學名稱為_______。
(2)B→C、G→H的反應類型分別為_________、_________。
(3)關于E的說法正確的是_____(填選項字母)。
A.分子中含有碳碳雙鍵 B.所有原子均在同一平面上
C.鄰二氯代物有兩種結構 D.能使酸性KMnO4溶液褪色
(4)D+I→M的化學方程式為_____________。
(5)J的結構簡式為____________。
(6)同時滿足下列條件的N(C8H12O3)的同分異構體有______種(不考慮立體異構)。
①飽和五元碳環上連有兩個取代基 ②能與NaHCO3溶液反應 ③能發生銀鏡反應
(7)參照上述合成路線和信息,以環庚醇和甲醇為有機原料(無機試劑任選),設計制備 的合成路線________。
的合成路線________。
【答案】2-丙醇 加成反應 消去反應 B nCH3CH(OH)CH2OH+nHOOC(CH2)4COOH![]()
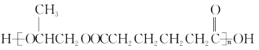 +(2n-1)H2O CH3CH2OOC(CH2)4COOCH2CH3 6
+(2n-1)H2O CH3CH2OOC(CH2)4COOCH2CH3 6 ![]()
【解析】
A的核磁共振氫譜有3組峰,A發生消去反應生成B,A為CH3CH(OH)CH3,B發生加成反應生成C為CH3CHBrCH2Br,C發生水解反應生成D為CH3CH(OH)CH2OH,E發生取代反應生成F,F發生加成反應生成G,則E為![]() 、F為
、F為![]() ,G是
,G是![]() ,G與NaOH的乙醇溶液發生消去反應生成H為
,G與NaOH的乙醇溶液發生消去反應生成H為![]() ,H發生氧化反應生成I為HOOC(CH2)4COOH,J為CH3CH2OOC(CH2)4COOCH2CH3,D、I發生酯化反應生成M,M為
,H發生氧化反應生成I為HOOC(CH2)4COOH,J為CH3CH2OOC(CH2)4COOCH2CH3,D、I發生酯化反應生成M,M為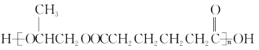 ,由題給信息可知N為
,由題給信息可知N為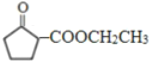 ,以此解答該題。
,以此解答該題。
(1)A的核磁共振氫譜有3組峰,A發生消去反應生成B,A為CH3CH(OH)CH3,化學名稱為2-丙醇;
(2)B是CH2=CH-CH3,B與Br2的CCl4溶液發生加成反應產生C:CH3CHBrCH2Br,所以B生成C的反應類型是加成反應生成C;G是![]() ,G與NaOH的乙醇溶液發生消去反應生成H為
,G與NaOH的乙醇溶液發生消去反應生成H為![]() ,反應類型是消去反應;
,反應類型是消去反應;
(3)E結構簡式為![]()
A.E是苯,苯分子中不含碳碳單鍵和雙鍵,其中的化學鍵是一種介于單鍵和雙鍵之間的特殊鍵,A錯誤;
B.苯是平面正六邊形結構,苯分子中所有原子都處于同一平面,B正確;
C.苯是平面正六邊形結構,所有碳碳鍵相同,因此苯的鄰二氯代物只有一種,C錯誤;
D.苯具有特殊的穩定性,不能與酸性高錳酸鉀溶液反應,因此苯不能被酸性高錳酸鉀溶液氧化,D錯誤;
故合理選項是B;
(4)D是CH3CH(OH)CH2OH,I是HOOC(CH2)4COOH,二者在濃硫酸存在條件下發生酯化反應形成聚酯M,則D+I→M的化學方程式為:nCH3CH(OH)CH2OH+nHOOC(CH2)4COOH![]()
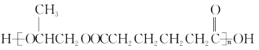 +(2n-1)H2O;
+(2n-1)H2O;
(5)根據上述分析可知J的結構簡式為
(6)N分子式為C8H12O3,其對應的同分異構體①飽和五元碳環上連有兩個取代基;②能與 NaHCO3溶液反應,說明含有羧基;③能發生銀鏡反應,說明含有醛基,則可能為![]() 、
、![]() 、
、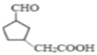 、
、![]() 、
、![]() 、
、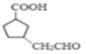 等,共6種;
等,共6種;
(7)環庚醇![]() 在濃硫酸、加熱條件下發生消去反應產生環庚烯
在濃硫酸、加熱條件下發生消去反應產生環庚烯![]() ,然后用酸性高錳酸鉀溶液氧化生成
,然后用酸性高錳酸鉀溶液氧化生成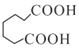 ,
,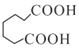 與甲醇發生酯化反應生成
與甲醇發生酯化反應生成![]() ,最后在乙醇鈉/DMF作用下生成
,最后在乙醇鈉/DMF作用下生成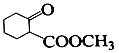 ,因此合成路線流程圖為:
,因此合成路線流程圖為:![]() 。
。


 全優點練單元計劃系列答案
全優點練單元計劃系列答案科目:高中化學 來源: 題型:
【題目】已知水在25℃和95℃時,其電離平衡曲線如圖所示:

(1)則25℃時水的電離平衡曲線應為________(填“A”或“B”),請說明理由________.
(2)95℃時,將pH=9的NaOH溶液與pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,則NaOH溶液與pH=4的H2SO4溶液的體積比為________.
(3)95℃時,若100體積pH1=a的某強酸溶液與1體積pH2=b的某強堿溶液混合后溶液呈中性,則混合前,該強酸的pH1與強堿的pH2之間應滿足的關系是________________.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將物質的量均為amol的Na 和Al一同投入mg足量水中,所得溶液的密度為ρg·cm-3,則此溶液的物質的量濃度為( )
A. 1000aρ/(46a+m)mol·L-1 B. 4ρ/(46a+m)mol·L-1
C. 1000aρ/(50a+m)mol·L-1 D. 1000aρ/(45a+m)mol·L-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗操作不能達到實驗目的的是( )
A. 用加熱的方法除去碳酸鈉固體中的碳酸氫鈉
B. 加熱蒸干溶液,可以得到CuCl2晶體
C. 放在流動的蒸餾水中可除去半透膜中蛋白質溶液里混有的(NH4)2SO4
D. 鑒別NaBr和KI溶液,可分別加新制氯水后,用CCl4萃取
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,向20mL0.05mol·L-1的某稀酸H2B溶液中滴入0.1mol·L-1氨水,溶液中由水電離出氫離子濃度隨滴入氨水體積變化如圖。下列分析正確的是( )

A. NaHB溶液可能為酸性,也可能為堿性
B. A、B、C三點溶液的pH是逐漸減小,D、E、F三點溶液的pH是逐漸增大
C. E溶液中離子濃度大小關系:c(NH4+)>c(B2-)>c(OH-)>c(H+)
D. F點溶液c(NH4+)=2c(B2-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2018年8月31日,華為公司發布AI芯片麒麟980,這標志著我國高科技企業的芯片制造技術邁入國際領先水平。組成芯片的核心物質是高純度硅。下圖是以石英砂為原料同時制備硅和金屬鋰。

已知:LiCl的熔點是605℃、沸點是1350℃;NH4Cl在100℃開始揮發,337.8℃分解完全。常溫下,Ksp[Fe(OH)3]=2.64×10-39,Ksp[Al(OH)3]=1×10-33。
(1)粗硅中常含有副產物SiC,請寫出①中生成SiC的反應方程式_______。寫出②中的反應方程式_______。
(2)請寫出操作名稱:a_____;b_______。
(3)請寫出試劑X是______。
(4)本生產工藝要求,要控制LiCl和NH4Cl溶液中的雜質離子濃度在1.0×10-6mol·L-1以下,應控制溶液的pH為_____,此時溶液中Fe3+的濃度為_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法錯誤的是
①NaHCO3溶液加水稀釋,c(Na+)/ c(HCO3-)的比值保持增大
②濃度均為0.1 mol·L-1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO![]() )+c(HCO
)+c(HCO![]() )]
)]
③在0.1 mol·L-1氨水中滴加0.lmol·L-1鹽酸,恰好完全中和時溶液的pH=a,則由水電離產生的c(OH-)=l0-amol·L-1
④向0.1mol/LNa2SO3溶液中加入少量NaOH固體,c(Na+)、c(SO32-)均增大
⑤在Na2S稀溶液中,c(H+)=c(OH-)+c(H2S)+c(HS-)
A. ①④ B. ②⑤ C. ①③ D. ②④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】目前手機屏幕主要由保護玻璃、觸控層以及下面的液晶顯示屏三部分組成。下面是工業上用丙烯(A)和有機物C(C7H6O3)為原料合成液晶顯示器材料(F)的主要流程:

(1)化合物C的結構簡式為_____。B的官能團名稱_____。
(2)上述轉化過程中屬于取代反應的有______(填反應序號)。
(3)寫出B與NaOH水溶液反應的化學方程式_________。
(4)下列關于化合物D的說法正確的是_____(填字母)。
a.屬于酯類化合物 b.1molD最多能與4molH2發生加成反應
c.一定條件下發生加聚反應 d.核磁共振氫譜有5組峰
(5)寫出符合下列條件下的化合物C的同分異構體的結構簡式______。
①苯環上一溴代物只有2種 ②能發生銀鏡反應 ③苯環上有3個取代基
(6)請參照上述制備流程,寫出以有機物C和乙烯為原料制備 的合成路線流程圖(無機試劑任用)_______。
的合成路線流程圖(無機試劑任用)_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關2個電化學裝置的敘述正確的是

A. 裝置①中,電子移動的路徑是:Zn→Cu→CuSO4溶液→KCl鹽橋→ZnSO4溶液
B. 在不改變總反應的前提下,裝置①可用Na2SO4替換ZnSO4,用石墨替換Cu棒
C. 裝置②中采用石墨電極,通電后,由于OH-向陽極遷移,導致陽極附近pH升高
D. 若裝置②用于鐵棒鍍銅,則N極為鐵棒
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com