
2012年,IUPAC正式命名了116號元素,下列關于![]() 和
和![]() 的說法中,錯誤的是
的說法中,錯誤的是
A.這是兩種原子 B.兩者電子數相差1
C.兩種原子中中子數分別為177和178 D.兩者互為同位素
科目:高中化學 來源: 題型:
293 116 |
291 116 |
| A、這是兩種原子 |
| B、兩者電子數相差1 |
| C、兩種原子中中子數分別為177和178 |
| D、兩者互為同位素 |
查看答案和解析>>
科目:高中化學 來源:2012-2013學年上海市松江區高三上學期期末考試化學試卷(解析版) 題型:選擇題
2012年,IUPAC正式命名了116號元素,但117號元素尚未被正式認定。下列關于 的說法,錯誤的是
的說法,錯誤的是
A.是兩種原子 B.互為同位素
C.中子數分別為176和177 D.電子數相差1
查看答案和解析>>
科目:高中化學 來源:2012-2013學年四川省涼山州高三第三次診斷理綜化學試卷(解析版) 題型:填空題
2012年冬季,我國城市空氣污染狀況受到人們的強烈關注,其中NOx、CO、SO2是主要污染性氣體。
I.汽車內燃機工作時發生的反應 是導致汽車尾 氣中含有NO的重要原因之一。
是導致汽車尾 氣中含有NO的重要原因之一。
(1)有人欲選用合適的催化劑,使反應2NO(g)=N2(g)+O2(g)能較快進行以達到除去NO的目的。你認為該反應能否自發進行 (填“能”或“不能”)。
(2)利用催化技術可將汽車尾氣中的NO氣體轉化成無毒氣體,相關反應的平衡常數可表示為
 ,此反應為放熱反應。在一定溫度下,10L某密閉容器中發生上述反應,各物質的物質的量的變化情況如下表
,此反應為放熱反應。在一定溫度下,10L某密閉容器中發生上述反應,各物質的物質的量的變化情況如下表

①根據土表數據計算0~4s間用NO表示的平均速率v(NO)= ;達到化學平衡時兩種反應物的轉化率是否相等 (填“相等”或“不相等”)。
②在5~6s時,若K增大,5s后正反應速率 (填“增大”或“減小”)
③在5~6s時,若K不變,以上各物質的物質的量變化原因可能是 。
A.選用更有效的催化劑 B.縮小容器的體積
C.降低CO2濃度 D.升高溫度
II為探究硫在氧氣中燃燒的產物里是否有SO3,某化學興趣小組在絕熱環境下進行了定量實驗探究。探究實驗的相關數據如下
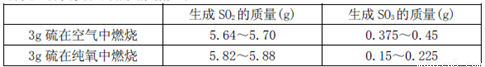
(3)對數據進行分析可知,等質量的硫在純氧中燃燒產生的SO3比在空氣中燃燒產生的SO3 (填“多”或“少”),原因可能是 。
A.純氧中氧氣濃度高,有利于化學平衡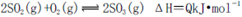 向右移動
向右移動
B.化學反應
C.純氧中氧氣濃度高,單位時間內發熱量大,致使反應體系的溫度較高,不利于化學平衡
 向右移動
向右移動
D.3g硫在純氧中燃燒比3g硫在空氣中燃燒放出的熱量多,不利于化學平衡
 向右移動
向右移動
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
2009年12月7日~18日在丹麥首都哥本哈根召開了世界氣候大會,商討《京都議定書》一期承諾到期后的后續方案,即2012年至2020年的全球減排協議,大會倡導“節能減排” 和“低碳經濟”,降低大氣中CO2的含量及有效地開發利用CO2,引起了各國的普遍重視。過渡排放CO2會造成“溫室效應”,科學家正在研究如何將CO2轉化為可利用的資源。目前工業上有一種方法是用CO2來生產燃料甲醇。一定條件下發生反應:
 CO2(g)+3H2(g)
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),下圖表示該反應過程中能量(單位為kJ·mol-1)的變化:
CH3OH(g)+H2O(g),下圖表示該反應過程中能量(單位為kJ·mol-1)的變化:

(1)關于該反應的下列說法中,正確的是____________(填字母)。
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)為探究反應原理,現進行如下實驗,在體積為l L的密閉容器中,充入l mol CO2和3 mol H2,一定條件下發生反應:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),經測得CO2和CH3OH(g)的濃度隨時間變化如圖所示。
CH3OH(g)+H2O(g),經測得CO2和CH3OH(g)的濃度隨時間變化如圖所示。

從反應開始到平衡,CO2的平均反應速率v(CO2) = 。
② 該反應的平衡常數表達式K= 。
③ 下列措施中能使化學平衡向正反應方向移動的是 (填字母)。
A.升高溫度
B.將CH3OH(g)及時液化抽出
C.選擇高效催化劑
D.再充入l molCO2和3 molH2
(3)25℃,1.01×105Pa時,16g 液態甲醇完全燃燒,當恢復到原狀態時,放出369.2kJ的熱量,寫出該反應的熱化學方程式:___________________________________________。
(4)選用合適的合金為電極,以氫氧化鈉、甲醇、水、氧氣為原料,可以制成一種以甲醇為原料的燃料電池,此電池的負極應加入或通入的物質有__________ _____;其正極的電極反應式是:_____________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com