
今有室溫下四種溶液,有關敘述正確的是
| | ① | ② | ③ | ④ |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | 氫氧化鈉溶液 | 醋酸 | 鹽酸 |
AB
解析試題分析:A、氨水為弱堿,pH=11的氨水稀釋10倍,pH大于10,NaOH為強堿,pH=11的NaOH溶液稀釋10倍,pH變為10,pH=3的醋酸(弱酸)稀釋10倍pH大于3小于4,pH=3的HCl(強酸)稀釋10倍變為4,故稀釋后四種溶液的pH ①>②>④>③,正確;B、加入NH4Cl晶體,氨水的電離平衡左移,pH減小,在NaOH溶液中加入NH4Cl,銨根與氫氧根結合,使OH-濃度減小,pH減小,正確;C、①、④兩溶液等體積混合因氨水為弱電解質,濃度大于鹽酸,故溶液呈堿性,c(H+)<c(OH-),錯誤;D、VaL④與VbL②溶液混合有:Va×10-3-Vb×10-3=(Va+Vb)×10-4,則Va:Vb=11:9,錯誤。
考點:考查溶液的酸堿性與pH計算、離子濃度大小比較。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案 目標測試系列答案
目標測試系列答案科目:高中化學 來源: 題型:單選題
T ℃時,某NaOH溶液中c(H+)=10-amol·L-1,c(OH-)=10-bmol·L-1,已知a+b=12。向該溶液中逐滴加入pH=c的鹽酸(T ℃),測得混合溶液的部分pH如表中所示:
| 序號 | NaOH溶液的體積/mL | 鹽酸的體積/mL | 溶液的pH |
| ① | 20.00 | 0.00 | 8 |
| ② | 20.00 | 20.00 | 6 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
常溫下,0.2mol/L一元酸HA與等濃度的NaOH溶液等體積混合后,所得溶液中部分微粒組分及濃度如圖所示,下列說法正確的是
| A.HA是強酸 |
| B.該混合液pH=7 |
| C.圖中x表示HA,Y表示OH-,Z表示H+ |
| D.該混合溶液中:c(A-)+c(Y)=c(Na+) |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列實驗能達到預期目的的是 ( )
| 編號 | 實驗內容 | 實驗目的 |
| A | 室溫下,用pH試紙分別測定濃度為0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH | 比較HClO和CH3COOH的酸性強弱 |
| B | 向含有酚酞的Na2CO3溶液中加入少量BaC12固體,溶液紅色變淺 | 證明Na2CO3溶液中存在水解平衡 |
| C | 向10mL 0.2 mol/L NaOH溶液中滴入2滴0.1 mol/L MgCl2溶液,產生白色沉淀后,再滴加2滴0.1 mol/LFeCl3溶液,又生成紅褐色沉淀 | 證明在相同溫度下的Ksp: Mg(OH)2 >Fe(OH)3 |
| D | 分別測定室溫下等物質的量濃度的Na2SO3與Na2CO3溶液的pH,后者較大 | 證明非金屬性S>C |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
25℃時,0.1mol Na2CO3與鹽酸混合所得的一組體積為1 L的溶液,溶液中部分微粒與pH的關系如圖所示。下列有關溶液中離子濃度關系敘述正確的是 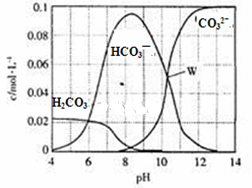
| A.W點所示的溶液中:c (Na+)+c (H+)=2c(CO32- )+c (OH-)+c (Cl-) |
| B.pH= 4的溶液中:c (H2CO3)+c (HCO3-)+c (CO32-)<0.1mol·L-1 |
| C.pH=8的溶液中:c (H+)+c (H2CO3)+c (HCO3-)= c (OH-)+c (Cl- ) |
| D.pH=11的溶液中:c (Na+)>c (Cl-)>c (CO32- )>c (HCO3- )>c (H2CO3) |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列敘述正確的是
| A.FeCl3溶液中加入鎂粉有氣泡產生 |
| B.C12、SO2均能使品紅溶液褪色,說明二者均有漂白性 |
| C.鉛蓄電池在放電過程中,負極質量減小,正極質量增加 |
| D.向飽和NaC1溶液中先通入足量CO2,再通入足量NH3,可析出NaHCO3晶體 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在不同溫度下,水溶液中c(H+)與c(OH-)有如圖所示關系,下列說法正確的是( )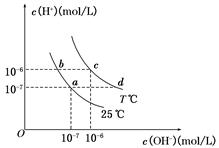
A.a點對應的溶液和c點對應的溶液pH值大小:
pH(c)>pH(a)
B.d點對應的溶液中大量存在:K+、Ba2+、NO3-、I-
C.25℃時,Ka(HF)=3.6×10-4,Ka(CH3COOH)=1.75×10-5,
0.1mol/L的NaF溶液與0.1mol/L 的CH3COOK溶液相比:
c(Na+)-c(F-)>c(K+)-c(CH3COO-)
D.如b點對應的溶液中只含NaHA,則溶液中粒子濃度大小:
c(HA-)>c(H2A)>c(H+)>c(A2-)
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
已知在比較酸的強弱時,必須考慮兩方面:一是電離出氫離子的能力,二是溶劑接受氫離子的能力。比如HCl在水中是強酸,在冰醋酸中就是弱酸;而HAc在水中是弱酸,在液氨中卻是強酸,就是因為接受氫離子的能力:NH3>H2O>HAc。下列關于酸性強弱的說法正確的是( )
| A.在A溶劑中,甲的酸性大于乙;在B的溶劑中,甲的酸性可能小于乙 |
| B.比較HCl、H2SO4、HClO4、HNO3酸性的強弱,用水肯定不可以,用冰醋酸可能可以 |
| C.HNO3在HClO4中是酸,在H2SO4中可能是堿 |
| D.比較HCN與HAc酸性的強弱,用水肯定可以,用液氨肯定也可以 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在0.1mol·L-1CH3COOH溶液中存在如下電離平衡: CH3COOH CH3COO-+H+,對于該平衡,下列敘述正確的是
CH3COO-+H+,對于該平衡,下列敘述正確的是
| A.加入水時,平衡向生成CH3COOH的方向移動 |
| B.加入少量NaOH固體,平衡向電離的方向移動 |
| C.加入少量0.1mol·L-1HCl溶液,溶液中c(H+)減小 |
| D.加入少量CH3COONa固體,平衡向電離的方向移動 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com