
| A. | 3.12g | B. | 4.18g | C. | 4.68g | D. | 5.08g |
分析 硝酸被還原為NO氣體且標準狀況下體積為0.896L,即物質的量為0.04mol,根據氮元素的化合價變化計算轉移電子物質的量.最后沉淀為Cu(OH)2、Mg(OH)2,金屬提供的電子的物質的量等于氫氧根離子的物質的量,故最后沉淀質量等于金屬的質量加氫氧根離子的質量.
解答 解:硝酸被還原為NO氣體且標準狀況下體積為0.896L,即物質的量為:$\frac{0.896L}{22.4L/mol}$=0.04mol,所以轉移的電子的物質的量為:0.04mol×(5-2)=0.12mol,
最后沉淀為Cu(OH)2、Mg(OH)2,金屬提供的電子的物質的量等于氫氧根離子的物質的量,
所以最后沉淀質量為:2.14g+0.12mol×17g/mol=4.18g,
故選:B.
點評 本題考查混合物的計算,題目難度中等,解題關鍵是判斷沉淀質量為金屬與金屬離子結合氫氧根離子的質量之和,根據氫氧化鈉計算沉淀中氫氧根的物質的量更簡單,試題培養了學生的化學計算能力.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該反應中的還原劑為KNO3 | |
| B. | 該反應中C被還原 | |
| C. | 若消耗32gS,轉移電子數為10mol | |
| D. | 若生成標準狀況下氣體22.4L,則有0.75 mol物質被還原 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
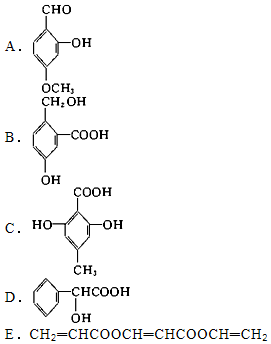
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 化合物都是電解質 | |
| B. | 電解質一定是化合物 | |
| C. | SO2溶于水形的溶液能導電,所以SO2是電解質 | |
| D. | NaCl固體不導電,所以NaCl不是電解質 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 對不可回收垃圾常用的處理方法有衛生填埋、堆肥和焚燒 | |
| B. | 制造玻璃是復雜的物理變化,玻璃的組成不同,性能不同 | |
| C. | BaSO4在醫學上用作鋇餐 | |
| D. | 固體煤經處理變為氣體燃料后,可以減少SO2和煙塵的污染,且燃燒效率高 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com