
| A. | 達到化學平衡時,將完全轉化為NH3 | |
| B. | 達到化學平衡時,N2、H2和NH3的物質的量濃度一定相等 | |
| C. | 達到化學平衡時,N2、H2和NH3的物質的量濃度不再變化 | |
| D. | 達到化學平衡時,正反應速率和逆反應速率都為零 |
分析 可逆反應反應物不能完全反應,達到平衡狀態時,正逆反應速率相等(同種物質)或正逆反應速率之比等于系數之比(不同物質),平衡時各種物質的物質的量、濃度等不再發生變化,由此衍生的一些物理量不變,以此分析.
解答 解:A.該反應是可逆反應,N2不可能完全轉化為NH3,故A錯誤;
B.達到平衡時,N2、H2、NH3的物質的量濃度不再發生變化而不是一定相等,反應平衡時各物質的濃度是否相等取決于起始時各物質的量的關系和轉化的程度,N2、H2按1:3混合,化學計量數為1:3,所以轉化率相等,平衡時,N2、H2的物質的量濃度一定為1:3,故B錯誤;
C.隨反應進行,N2、H2和NH3的物質的量濃度發生變化,N2、H2和NH3的物質的量濃度不再變化,說明到達平衡狀態,故C正確;
D.可逆反應時動態平衡,達到化學平衡時,正反應和逆反應的速率相同但不為零,故D錯誤;
故選C.
點評 本題考查平衡狀態的判斷,選擇判斷的標準應隨反應進行變化,當該標準不再變化說明到達平衡狀態,題目難度中等.


 英語小英雄天天默寫系列答案
英語小英雄天天默寫系列答案 暑假作業安徽少年兒童出版社系列答案
暑假作業安徽少年兒童出版社系列答案科目:高中化學 來源: 題型:選擇題
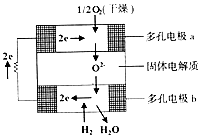 固體氧化物燃料電池是由美國西屋(West-inghouse)公司研制開發的.它以固體氧化鋯一氧化釔為電解質,這種固體電解質在高溫下允許氧離子(O2-)在其間通過.該電池的工作原理如圖所示,其中多孔電極a、b均不參與電極反應.下列判斷正確的是( )
固體氧化物燃料電池是由美國西屋(West-inghouse)公司研制開發的.它以固體氧化鋯一氧化釔為電解質,這種固體電解質在高溫下允許氧離子(O2-)在其間通過.該電池的工作原理如圖所示,其中多孔電極a、b均不參與電極反應.下列判斷正確的是( )| A. | O2-向電池的正極移動 | |
| B. | 有H2放電的b極為電池的正極 | |
| C. | a極對應的電極反應為O2+2H2O+4e-=4OH- | |
| D. | 該電池的總反應方程式為2H2+O2=2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鋅錳電池和堿性鋅錳電池的正極材料均是鋅 | |
| B. | 鋅錳電池中電解質主要是NH4Cl,而堿性鋅錳電池中的電解質主要是KOH | |
| C. | 堿性鋅錳電池不如鋅錳電池的壽命長 | |
| D. | 干電池放電之后還可再充電 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
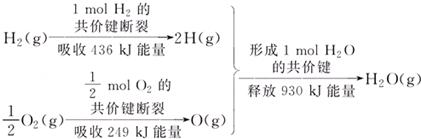
| A. | 1 mol H2的共價鍵形成放出436 kJ能量 | |
| B. | 氫氣跟氧氣反應生成水的同時吸收能量 | |
| C. | 1 mol H2(g)跟0.5mol O2(g)反應生成1 mol H2O(g)釋放能量245 KJ | |
| D. | 1 mol H2(g)與0.5mol O2(g)的總能量大于1 mol H2O(g)的能量 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
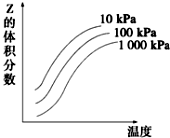 圖是溫度和壓強對X+Y?2Z反應影響的示意圖.圖中橫坐標表示溫度,縱坐標表示平衡時混合氣體中Z的體積分數.下列敘述正確的是( )
圖是溫度和壓強對X+Y?2Z反應影響的示意圖.圖中橫坐標表示溫度,縱坐標表示平衡時混合氣體中Z的體積分數.下列敘述正確的是( )| A. | 上述可逆反應的正反應為放熱反應 | B. | X、Y、Z均為氣態 | ||
| C. | 增大壓強平衡向正反應方向移動 | D. | 上述反應的逆反應的△H<0 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 重氫原子:${\;}_{1}^{2}$D | |
| B. | S2-的結構示意圖: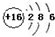 | |
| C. | 質子數為53,中子數為78的碘原子:${\;}_{53}^{131}$I | |
| D. | N2的電子式: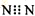 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 需要加熱才能發生的反應一定是吸熱反應 | |
| B. | 天然氣、太陽能、生物質能、風能、氫能均屬于新能源 | |
| C. | 自發反應的熵一定增大,非自發反應的熵一定減小 | |
| D. | 常溫下,反應C(s)+CO2(g)?2CO(g)不能自發進行,則該反應的△H>0 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com